Реакция на бензоаты с FeCl3 розовато-желтый осадок, растворимый в эфире:
 | |||||
 |  | ||||


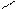
 COONa COO-
COONa COO-
 + FeCl3 → Fe · Fe(OH)3 · 7H2O
+ FeCl3 → Fe · Fe(OH)3 · 7H2O
Реакция на натрий (окрашивание пламени).
Определение температуры плавления чистой бензойной кислоты (122-124,5˚С). Более сильной азотной кислотой вытесняют ароматическую кислоту из соли, она выпадает в осадок
 | |||
 | |||
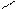

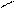 СООNa COOH
СООNa COOH

 +HNO3 → + NaNO3
+HNO3 → + NaNO3
Чистота. Прозрачность и цветность раствора, щелочность и кислотность, хлориды, сульфаты, тяжелые металлы – допустимы. Потеря в массе при высушивании (не более 3%). В натрия бензоате для инъекций дополнительно нормируется содержание железа.
Количественное определение. (как в перекиси водорода)
Ацидиметрия вариант вытеснения, прямое титрование. Метод основан на вытеснении более слабой кислоты из ее соли более сильной минеральной кислотой. Определение проводят в присутствии органического растворителя – эфир, который извлекает образующуюся кислоту и препятствует ее диссоциации. Индикатор м\о и м\с, титруют 0,5н раствором кислоты соляной до сиреневого окрашивания водного слоя.


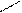
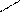

 СООNa COOH
СООNa COOH
+ HCl → + NaCl
Э = Мм
Содержание в препарате должно быть не менее 99,0% в перерасчете на сухое вещество.
 2015-08-21
2015-08-21 519
519








