Химические реакции высокомолекулярных соединений в принципе не отличаются от реакций классической органической химии, но большие размеры и сложность строения макромолекул обусловливают специфические особенности этих реакций. В отличие от реакций низкомолекулярных соединений, при которых конечные и промежуточные продукты реакции можно отделить от исходных, звенья, по-разному затронутые данной химической реакцией, входят в состав одной и той же макромолекулы и при одном и том же их среднем содержании в образце могут располагаться по цепи различным образом.
Основные отличия в хим поведении макромолекул:
1.Конфигурационные эффекты, включающие6 изменение направленности и степени завершенности реакции благодаря наличию соседнего звена той же или иной химической или пространственной конфигурации и создаваемым из-за этого стерическим затруднениям; изменение кинетики и механизма реакции с ннзкомолекулярным реагентом из-за различного окружения данной функциональной группы или звена в начале и в
конце реакции и связанного с этим изменения реакционной способности функциональных групп с конверсией (так называемый «эффект соседа»).
2. Конформационные эффекты, связанные с изменением конформации макромолекулы в процессе превращения. 3. Изменение локальной концентрации реагирующих групп вблизи макромолекулы в растворе по сравнению со средней концентрацией в объеме и связанное с этим изменение скорости реакции.
4. Эффекты, связанные с электростатическим взаимодействием заряженной макромолекулы с реагирующими частицами; оно может изменяться с глубиной конверсии, приводя к изменению конформации макромолекулы и скорости реакции.
5. Надмолекулярные эффекты, связанные с ассоциацией и агрегацией реагирующих частиц и приводящие к композиционной неоднородности и изменению химического строения продуктов реакции и скорости процесса
Растворы высокомолекулярных соединений (ВМС). Строение растворов, взаимодействие ВМС с растворителем (набухание), вязкость ВМС (приведенная, характеристическая), уравнение Марка-Хаувинка
В настоящее время растворы высокомолекулярных соединений рассматриваются как разновидность истинных растворов. Как и другие истинные растворы, растворы высокомолекулярных соединений являются гомогенными (однофазными) молекулярно- или ионнодисперсными системами. Элементарными структурными единицами в этих системах являются гигантские молекулы - макромолекулы высокомолекулярных соединений: или их ионы. Степень дисперсности в растворах высокомолекулярных соединений имеет порядок 106-107 см-1.
Растворы высокомолекулярных соединений обычно получают путем постепенного неограниченного набухания исходного вещества в подходящем растворителе.
 Набухание – поглощение полимером жидкости или газа, приводящее к увеличению его объёма или массы. Макромолекулы в полимере перепутаны. Растворитель, накапливаясь в полимере, увеличивает подвижность сегментов и уменьшает их межмолекулярное взаимодействие. Возникающая вследствие этого сегментальная диффузия способствует распутыванию клубков и последующему их разделению. Набухание может быть ограниченным и неограниченным. Неограниченное обычно сопровождается растворением.
Набухание – поглощение полимером жидкости или газа, приводящее к увеличению его объёма или массы. Макромолекулы в полимере перепутаны. Растворитель, накапливаясь в полимере, увеличивает подвижность сегментов и уменьшает их межмолекулярное взаимодействие. Возникающая вследствие этого сегментальная диффузия способствует распутыванию клубков и последующему их разделению. Набухание может быть ограниченным и неограниченным. Неограниченное обычно сопровождается растворением.
Количественно набухание характеризуется степенью набухания: 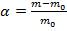 или
или 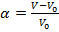 . Для гибкоцепных полимеров с очень большой ММ величина α может достигать порядка 100.
. Для гибкоцепных полимеров с очень большой ММ величина α может достигать порядка 100.
Явление набухания используется для определения величины параметра растворимости, плотности сшивки, степени ориентации.
Факторы, влияющие на набухание:
Природа полимера и растворителя (подобное в подобном); гибкость цепи (с увеличением гибкости повышается растворимость); ММ полимера; поперечные связи (чем их больше, тем хуже растворимость); температура неоднозначно.
Вязкость растворов ВМС зависит от концентрации вещества в растворе. В отличие от других растворов незначительная концентрация ВМС порой приводит к значительному увеличению вязкости раствора.
Вязкость растворов ВМС зависит от условий определения, в частности, от давления. Это объясняется тем, что одни и те же макромолекулы могут находиться в различных конформационных состояниях: от линейных до глобул, поэтому вязкость растворов ВМС может быть неодинакова в различных направлениях. Вязкость макромолекул с выпрямленными хаотично расположенными звеньями выше, чем вязкость макромолекул, которые имеют форму клубка.
Если вязкий полимер или его раствор продавить через капилляр, то молекулы будет выпрямляться и располагаться ориентированно, а вязкость будет снижаться.
Вязкость растворов ВМС зависит также от свойств и температуры растворителя.
Для растворов ВМС различают относительную, удельную, приведенную и характеристическую вязкости.
Относительная вязкость - отношение вязкости раствора hр к вязкости растворителя h0:
hотн = hр/ h0 = tр/ t0 (15.3)
tр время истечения раствора ВМС, t0 - время истечения растворителя(эти величины определяются с помощью вискозиметра).
Удельная вязкость - показывает, насколько увеличилась вязкость раствора ВМС по сравнению с вязкостью растворителя:
hуд = (hр - h0)/ h0 = (tр - t0)/ t0 =hотн - 1 (15.4)
Приведенная вязкость - отношение удельной вязкости к концентрации:
hпр = hуд/с (15.5)
Обычно приведенная вязкость линейно зависит от концентрации (рис.15.2).При экстраполяции прямой до пересечения с осью ординат получают величину /h/, которую называют характеристической вязкостью:
/h/ = lim hуд/с (15.6)
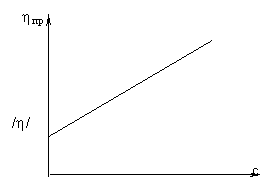
Рис.15.2.Изменение приведенной вязкости в зависимости от концентрации ВМС.
Характеристическую вязкость определяют на основании вискозиметрических измерений, используя значение относительной, удельной и приведенной вязкостей.
Характеристическая вязкость для данной пары веществ является величиной условной, но постоянной, она не зависит от концентрации растворителя и состояния макромолекул, кроме того, она связана с молекулярной массой макромолекул.
/h/ = kМа, lg/h/ = lg k + аlg М (15.7)
М - средняя молекулярная масса ВМС, а, k - коэффициенты.
Уравнение 15.7 - уравнение Марка-Куна-Хаувинка.
Для растворов полимеров с короткими и жесткими цепями а = 1 и уравнение 15.7 упрощается:
/h/ = kМ, lg /h/ = lg k + lgМ (15.8)
Коэффициент a зависит от формы молекул. Значение коэффициентов определяют экспериментально, это позволяет по значению характеристической вязкости рассчитать молекулярную массу макромолекул. Зная массу, можно определить средний размер r макромолекул:
М = 4/3pr3NАr (15.9)
 2015-08-12
2015-08-12 3266
3266