 1-й способ (через систему уравнений с двумя неизвестными).
1-й способ (через систему уравнений с двумя неизвестными).
Определяем массу соли Na2CO3 в 540 г 15%-го раствора:
100 г 15%-го р-ра – 15 г соли,
540 г 15%-го р-ра – z г соли,
z = 540•15/100 = 81 г.
Cоставляем систему уравнений:
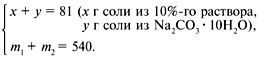
Находим молярную массу:
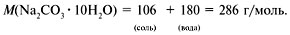
Избавляемся от лишних неизвестных:
m 2 = 286 y /106;
100 г 10%-го р-ра – 10 г соли,
m 1 г 10%-го р-ра – х г соли,
m 1 = 100 х /10 = 10 х.
Подставляем m 2 и m 1 в систему уравнений:

С учетом того, что х = 81 – y, избавляемся от второго неизвестного:
10(81 – y) + 286 y /106 = 540.
Отсюда
y = 270/7,3 = 37 г.
Тогда m 2 = 286 y /106 = 2,7•37 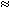 100 г – это масса необходимого количества кристаллогидрата Na2СО3•10H2O.
100 г – это масса необходимого количества кристаллогидрата Na2СО3•10H2O.
Далее находим: х = 81 – y = 81 – 37 = 44 г – это масса соли из 10%-го раствора.
Находим массу 10%-го раствора:
100 г 10%-го р-ра – 10 г соли,
m 1 г 10%-го р-ра – 44 г соли,
m 1 = 100•44/10 = 440 г.
Видно, что так можно решить данную задачу – способ надежный, но, к сожалению, достаточно длинный, громоздкий и сложный. Им успешно могут воспользоваться учащиеся с достаточно развитым логическим мышлением. Для других он будет сложноват.
 2-й способ (правило креста).
2-й способ (правило креста).
Допустим, что Na2СО3•10H2O – это «сухой раствор» (ведь он же содержит воду). Тогда найдем его «концентрацию»:
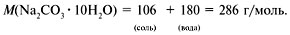
286 г – 106 г соли,
100 г – х г соли,
х = 100•106/286 = 37 г, или 37%.
Применяем правило креста.
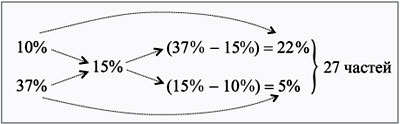
Находим массу одной части и массы веществ:
540/27 = 20 г,
m 1 = 20•22 = 440 г, m 2 = 20•5 = 100 г.
Ответ. Для приготовления 540 г раствора Na2CO3 15%-й концентрации необходимо взять 440 г 10%-го раствора и 100 г кристаллогидрата.
Таким образом, применение правила креста удобнее и проще при решении подобных задач. Этот способ более экономичен по времени и менее трудоемок.
Правило креста можно применять и в тех случаях, когда нужно получить раствор меньшей концентрации путем разбавления водой более концентрированного раствора или получить более концентрированный раствор путем добавления к исходному раствору сухой смеси. Рассмотрим это на примерах.
 2015-09-06
2015-09-06 889
889








