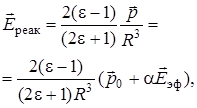 (6.56)
(6.56)
где R – радиус полости, 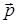 – результирующий дипольный момент молекулы. Реактивное поле, так как и поле внутри полости, можно выразить через показатель преломления среды:
– результирующий дипольный момент молекулы. Реактивное поле, так как и поле внутри полости, можно выразить через показатель преломления среды:
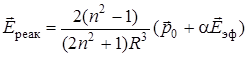 . (6.57)
. (6.57)
Таким образом, эффективное поле, действующее на молекулу в озагеровской полости равно
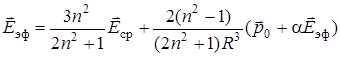
или
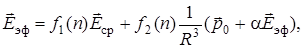 (6.58)
(6.58)
где 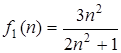 и
и 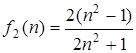 – функции от показателя преломления среды n (в общем случае n может быть комплексным), R – параметр теории, характеризующий объем полости.
– функции от показателя преломления среды n (в общем случае n может быть комплексным), R – параметр теории, характеризующий объем полости.
Из формулы (6.58) видно, что свойства эффективного поля в области примесной молекулы существенно зависят от ее поляризуемости и параметра теории R. Если в единице объема находится N молекул, которые занимают объем 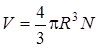 , то R3 определяет эффективный объем, приходящийся на одну молекулу. Этот объем может быть рассчитан по известным значениям плотности и молекулярного веса для однокомпонентной среды.
, то R3 определяет эффективный объем, приходящийся на одну молекулу. Этот объем может быть рассчитан по известным значениям плотности и молекулярного веса для однокомпонентной среды.
Известно, что объем молекул очень тесно связан с ее поляризуемостью 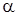 , входящей в формулу Лоренц – Лоренца. Анализ этой зависимости приводит к простому выражению
, входящей в формулу Лоренц – Лоренца. Анализ этой зависимости приводит к простому выражению 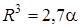 .
.
Следовательно, онзагеровский радиус может быть оценен независимыми способами на основании различных характеристик вещества: показателей преломления или соответствующей величины рефракции, значения которых приведены в справочной литературе. Указанные способы применяются и к двухкомпонентным растворам, если радиусы молекулы и растворителя близки. Если радиус примесной молекулы больше, чем радиус молекулы растворителя, то онзагеровкий радиус для такой системы может быть выбран исходя из ван–дер–ваальсова радиуса исследуемой молекулы.
Модель Онзагера не лишена и некоторых недостатков:
1. модель шара с точечным диполем в центре не отражает реальных свойств молекулы, обладающей сложным расположением зарядов
2. нельзя рассматривать ближайшее окружение молекулы как сплошную среду с диэлектрической проницаемостью 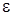 .
.
Недостаточно считать, что и связь данной молекулы с ее окружением выражается реактивным полем, имеющим то же направление, что и дипольный момент рассматриваемой молекулы. Логично предположить, что ориентация данной молекулы связана с ориентацией соседних молекул и, следовательно, зависит от их расположения.
Несмотря на отмеченные недостатки с помощью этой модели можно рассчитывать взаимодействие растворенной молекулы с окружающей средой и определять положение ее электронно-колебательных уровней. Уровень энергии при переходе от газовой фазы к раствору смещается на величину так называемой энергии стабилизации W ст, под которой будем понимать энергию уровня, которая установится после осуществления всех релаксационных процессов в молекуле после акта поглощения или испускания. Разность энергий стабилизации Δ W ст = W' ст + W'' ст основного и возбужденного уровней молекулы в растворе характеризует смещения спектра поглощения или испускания (см. рис. 6.26)
 Величина сдвига спектра может быть записана в следующем виде:
Величина сдвига спектра может быть записана в следующем виде:
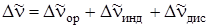 ,
,
где 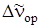 ,
, 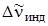 и
и 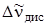 – изменения энергии молекулы в растворе, обусловленные взаимодействиями ориентационного, индукционного и дисперсионного характера. Энергия взаимодействия растворенной молекулы со средой определяется значениями ее дипольного момента
– изменения энергии молекулы в растворе, обусловленные взаимодействиями ориентационного, индукционного и дисперсионного характера. Энергия взаимодействия растворенной молекулы со средой определяется значениями ее дипольного момента 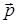 , поляризуемости
, поляризуемости 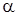 , а также величиной эффективного электрического поля
, а также величиной эффективного электрического поля 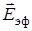 , действующего на молекулу в растворе. Однако преимущества метода локального поля проявились еще и в том, что на его основе были рассчитаны динамические сдвиги полос в электронных спектрах поглощения. Влияние динамических индуктивно-резонансных взаимодействий на сдвиг частот максимумов полос спектров растворов был рассмотрен Бахшиевым в рамках описания общих закономерностей влияния растворителя на смещение электронных спектров при переходах от газовой фазы к раствору. Величина сдвига оценивается по формуле
, действующего на молекулу в растворе. Однако преимущества метода локального поля проявились еще и в том, что на его основе были рассчитаны динамические сдвиги полос в электронных спектрах поглощения. Влияние динамических индуктивно-резонансных взаимодействий на сдвиг частот максимумов полос спектров растворов был рассмотрен Бахшиевым в рамках описания общих закономерностей влияния растворителя на смещение электронных спектров при переходах от газовой фазы к раствору. Величина сдвига оценивается по формуле
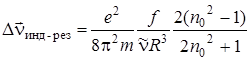 , (6.59)
, (6.59)
где e и m – заряд и масса электрона; f – сила осциллятора полосы; n 0 –показатель преломления растворителя; R – онзагеровский радиус молекулы; 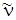 – частота максимума полосы
– частота максимума полосы
Принципиальное отличие динамических сдвигов от статических, рассматриваемых в теории Дебая, состоит в том, что динамические взаимодействия в конечном итоге определяются дипольным моментом перехода между квантовыми состояниями растворенной молекулы.
Итак, полный сдвиг частоты чисто электронного перехода для поглощения выразится в виде суммы
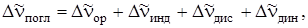 (6.60)
(6.60)
где 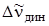 – динамический сдвиг полосы, обусловленной возникновением у молекулы наведенного дипольного момента под действием электрического вектора световой волны.
– динамический сдвиг полосы, обусловленной возникновением у молекулы наведенного дипольного момента под действием электрического вектора световой волны.
В электронных спектрах поглощения смещение полос может достигать весьма значительной величины, равной тысячам см–1. Причем полосы поглощения для одной и той же молекулы по разному сдвигаются в зависимости от растворителя. Например, спектр поглощения для молекулы 3-аминофталимида смещается в красную сторону в н-гептане на 1400 см–1, а в этиловом спирте и воде – до 2300 см–1.
В настоящее время установлены многие закономерности проявления межмолекулярных взаимодействий, имеющих самую разнообразную природу. Создан даже отдельный отдел спектроскопии межмолекулярных взаимодействий, который интенсивно развивается санкт-петербургской школой физиков (Бахшиев Н.Г., Либов В.С. и др.).
Источником информации в спектроскопии межмолекулярных взаимодействий о свойствах отдельных молекул служит не спектр молекулы как таковой, а изменение спектра при помещении молекулы в конденсированную среду.
6.8. Электронные спектры поглощения
растворов бензола и его производных
 2015-09-06
2015-09-06 1008
1008








