На свойствах аминокислот основаны методы их разделения из смеси. С практической точки зрения разделение аминокислот является необходимой процедурой в выяснении аминокислотного состава белков и пептидов. Наиболее популярными являются хроматографические методы.
Сам термин "хроматография" (греч. сhroma - цвет, graphein - писать) был введен в 1903г. русским ботаником Михаилом Цветом. Ему удалось разделить смесь пигментов листьев растений, используя твердые сорбенты. Современные методы разделения многих соединений базируются на хроматографии. При этом смесь веществ, подлежащих разделению, растворяется в жидкости или газовой среде, составляя "мобильную фазу". Она фильтруется через колонку, заполненную поросодержащим твердым матриксом, получившим название "стационарная фаза". Последний в некоторых типах хроматографии может быть ассоциирован с жидкостью.
Взаимодействие со стационарной фазой каждого из растворенных веществ приводит к задержке его прохождения через матрикс. Сила этой задержки зависит от свойств растворенного вещества. Поэтому если смесь, подлежащая фракционированию, начинает двигаться через колонку, на каждое из находящихся в ней соединений будут действовать задерживающие силы разной интенсивности. В результате такого воздействия постепенно смесь разделится на зоны, содержащие чистые вещества. Разделенные компоненты можно собрать в отдельные фракции для анализа или последующего фракционирования.
В зависимости от мобильной и стационарной фаз различают газожидкостную хроматографию (мобильная фаза - газ, стационарная - жидкость), жидкостно-жидкостную хроматографию (мобильная и стационарная фазы - несмешивающиеся жидкости, одна из которых связана с инертной твердой подложкой). Дальнейшая классификация хроматографических методов основана на природе преобладающего взаимодействия между стационарной фазой и разделяемыми веществами. К примеру, если сила, замедляющая продвижение вещества в твердой фазе, ионная по характеру, хроматография называется ионообменной; если же она является результатом адсорбции растворенных веществ на твердой стационарной фазе - хроматография будет адсорбционной.
Ионообменная хроматография. В процессе ионного обмена ионы, которые электростатически связаны с нерастворимым и химически инертным матриксом, обратимо замещаются ионами из раствора:
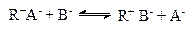
где R+A- - анионообменник, а В- - анионы из раствора. Соответственно катионообменник представляет отрицательно заряженные группы, которые обратимо связывают катионы.
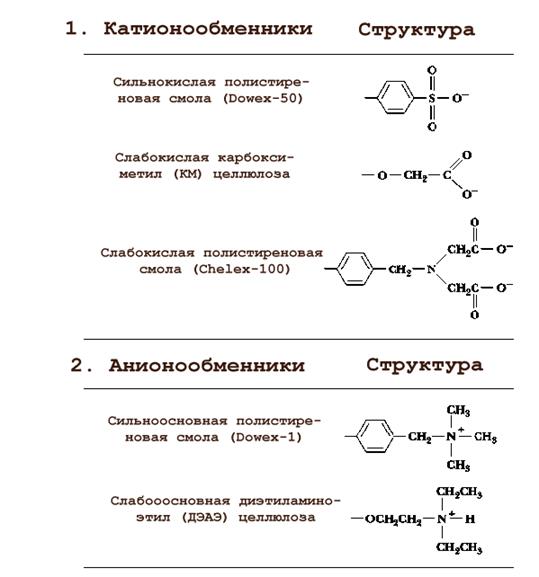
Аминокислоты относятся к полиэлектролитам, поскольку они имеют положительный и отрицательный заряд. За счет этого они могут присоединяться к анионо- и катионообменникам в зависимости от суммарного электрического заряда. Принцип разделения аминокислот ионообменной хроматографией представлен на рис. 1.4.
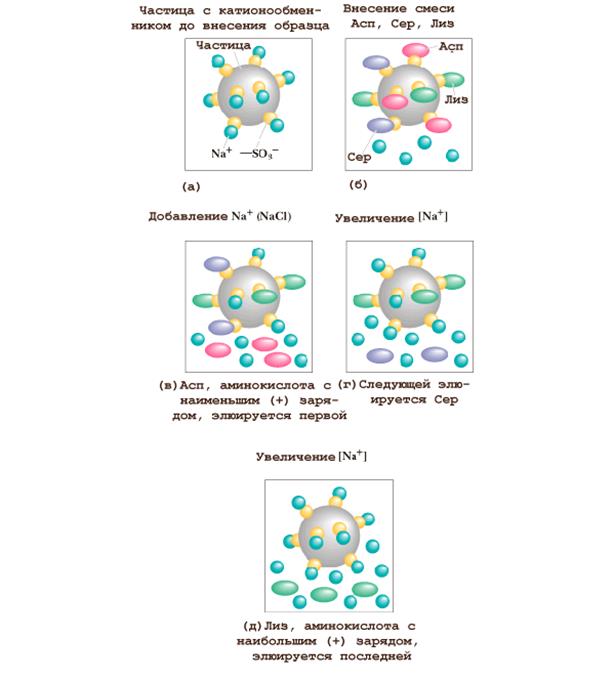
Рис.1.4. Принцип разделения аминокислот ионообменной хроматографией
Различные аминокислоты взаимодействуют и связываются с ионообменниками с различной силой. Колонку промывают, постоянно добавляя жидкость (обычно, буферный раствор) на поверхность сорбента; соответственно, пройдя через твердую фазу, она вытекает из колонки. Этот процесс получил название "элюция". При этом те аминокислоты, у которых низкая связывающая способность к данному ионообменнику, будут продвигаться через колонку быстрее аминокислот с более высокой связывающей способностью (рис.1.5).
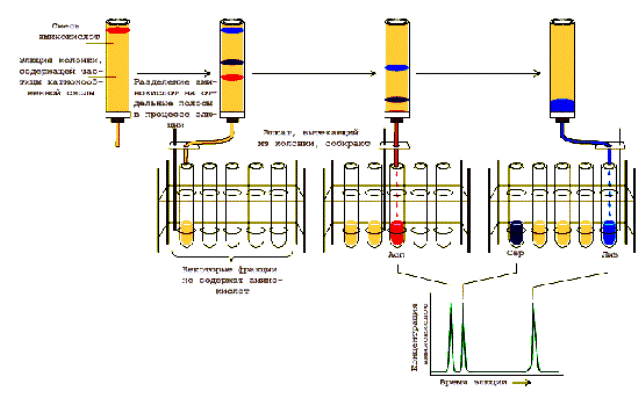
Рис.1.5. Сбор аминокислот, разделенных ионообменной хроматографией
Аминокислоты, которые более сильно связаны с ионообменником, можно вымыть, заменив элюирующий буфер на буфер с другим рН или с более высокой концентрацией соли. Такой процесс называется "этапной элюцией" (рис.1.6).
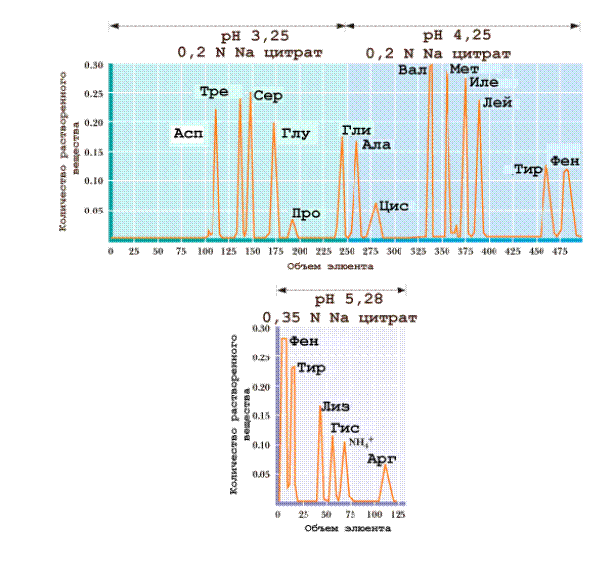
Рис. 1.6. Принцип этапной элюции при проведении ионообменной хроматографии
Весь этот процесс сейчас полностью автоматизирован так, что отдельные его стадии - элюирование, сбор фракций, их анализ и запись данных анализа - осуществляются по заданной программе в специальном приборе - аминокислотном анализаторе.
Прибор был предложен в 1958г. американскими учеными С. Муром и У. Стейном. Принцип его работы заключается в разделении смеси аминокислот ионообменной хроматографией на колонке, заполненной сульфированной полистирольной смолой. Колонка промывается буферными растворами с последовательным повышением их рН и концентрации. Время удержания каждой аминокислоты строго определенно и зависит от степени её ионизации. Выходящий из колонки элюат смешивается с раствором нингидрина и в специальной ячейке нагревается до 1000С. Аминокислоты, реагируя с нингидрином, превращаются в аммиак, СО2 и альдегид. Освобождающийся аммиак взаимодействует с другой молекулой нингидрина и дает окрашенное в фиолетовый цвет производное. Интенсивность окраски получающихся в результате реакции продуктов пропорциональна содержанию аминокислот в смеси. Она измеряется с помощью спектрофотометра, показания которого регистрируются самописцем.
Высокоэффективная жидкостная хроматография. В последние годы для разделения аминокислот используют метод высокоэффективной жидкостной хроматографии. С этой целью аминокислоты предварительно дансилируют (взаимодействием с дансилхлоридом). Разделение дансилпроизводных аминокислот проводится на силикагеле с ковалентно присоединенными углеводородами с помощью специального жидкостного хроматографа. В его состав входят особым образом упакованные колонки, насос, позволяющий создавать давление до 200 атм, градиентный смеситель, работающий с высокой степенью воспроизводимости и высокочувствительный флюоресцентный детектор. К достоинствам метода следует отнести исключительно высокую скорость разделения (менее 1 ч), воспроизводимость результатов и возможность проводить аналитические опыты на микрограммовых количествах вещества.
 2015-10-16
2015-10-16 5775
5775








