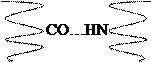
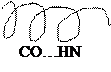
В формировании вторичной структуры участвуют водородные связи, возникающие между электроотрицательными атомами. Водородные связи сами по себе слабые, но в формировании вторичной структуры принимают участие довольно большое их количество; между водородными связями возникает так называемый кооперативный эффект действия, заключающийся в том, что суммарный эффект их совместного действия значительно выше суммы действия водородных связей порознь. Таким образом, водородные связи обеспечивают достаточную стабильность и прочность вторичной структуры.
Третичная структура возникает в результате укладки вторичной структуры в глобулу или клубок. В её формировании участвуют ковалентные дисульфидные связи (-S-S-), которые обуславливают изменение направления  полипептидной цепи, скрепляют её отдельные участки; электростатические взаимодействия – ионные связи (солевые мостики -СОО-×××NH3), возникают между N- и С-концевыми аминокислотами кислотами; водородные связи; ван-дер-ваальсовские силы, ответственные за окончательное свертывание полипептидной цепи; гидрофобные взаимодействия – это, например, -СН2-СН3, между циклическими радикалами и т.д. Гидрофобные взаимодействия не способны притягивать молекулы воды.
полипептидной цепи, скрепляют её отдельные участки; электростатические взаимодействия – ионные связи (солевые мостики -СОО-×××NH3), возникают между N- и С-концевыми аминокислотами кислотами; водородные связи; ван-дер-ваальсовские силы, ответственные за окончательное свертывание полипептидной цепи; гидрофобные взаимодействия – это, например, -СН2-СН3, между циклическими радикалами и т.д. Гидрофобные взаимодействия не способны притягивать молекулы воды.
 Четвертичная структура – ассоциация нескольких полипептидных цепей, которая образуется за счет нековалетных связей (водородных, ионных, гидрофобных взаимодействий, электростатического притяжения) представляет собой агрегат, состоящий из двух или более мономеров. Каждая полипептидная цепь, участвующая в образовании четвертичной структуры, называется субъединицей или протомером.
Четвертичная структура – ассоциация нескольких полипептидных цепей, которая образуется за счет нековалетных связей (водородных, ионных, гидрофобных взаимодействий, электростатического притяжения) представляет собой агрегат, состоящий из двух или более мономеров. Каждая полипептидная цепь, участвующая в образовании четвертичной структуры, называется субъединицей или протомером.
Белки разделяются на две большие группы: простые (протеины) и сложные (протеиды). Протеины делятся на:
- Альбумины – белки, растворимые в воде. К ним относятся белок куриного яйца – овальбумин, белок молочной сыворотки - лактальбумин;
- Глобулины – белки, нерастворимые в воде, но растворимые в солевых растворах (10% NaCl). Они составляют большую часть масличных культур;
- Проламины – белки, нерастворимые ни в воде и в солевых растворах, но растворимые в водно-спиртовых растворах, содержащих примерно 70-90% спирта;
- Глютелины – белки, нерастворимые ни в воде, ни в солевых, ни в спиртовых растворах, но растворимые лишь в щелочных растворах (0,2% растворе щелочи);
- Протамины – белки небольшой молекулярной массы, состоящие на 80% из щелочных аминокислот и не содержащие серы. Эти белки обнаружены только в сперме (молоке) рыб. По величине молекул протамины – самые малые белки.
- Гистоны – низкомолекулярные белки также основного характера, содержатся в хромосомах клеточных ядер и играют важную роль в образовании структуры хроматина. Гистоны – настоящие белки в их состав входят почти все белковые аминокислоты.
- Протеноиды – подгруппа фибриллярных белков, содержащихся в опорных тканях животных. Они не растворимы ни в воде, ни в солевых растворах, ни в разбавленных кислотах и щелочах. Они плохо поддаются гидролизу протеолитическими ферментами. К ним относятся, например, коллаген соединительной ткани, кератин волос, шерсти, перьев, копыт, эластин сухожилий и связок, фибрион шелка.
Сложные белки кроме аминокислотных остатков содержат также небелковую или простетическую, группу. Они разделяются на:
- Липопротеины, представляющие собой соединение белка с каким-либо жироподобным веществом;
- Гликопротеины, состоящие из белка и какого-либо углевода;
- Нуклеопротеины – соединение белка с нуклеиновыми кислотами;
- Металлопротеины – соединение атомов металлов с белком;
- Фосфопротеины - состоят из белка и остатка фосфорной кислоты и т.д.
 2015-10-16
2015-10-16 942
942







