Анализ основан на использовании группового реагента NaOH в присутствии H2O2; способности ионов Cr (III), мышьяка (III) и олова (II) вступать в реакции окисления; различной способности ионов взаимодействовать с солями аммония; а также на различной гидролитической активности.
| Операция | Реагенты и техника выполнения | Наблюдаемые явления |
| Осаждение гидроксидов катионов IV группы и растворение их в избытке щелочи | 10-15 капель исследуемого раствора + 2-5 капель 3 % H2O2 + 6 моль/л раствор NaOH до полного растворения осадка (нагревание в фарфоровой чашке до удаления избытка Н2О2) | Раствор 1: [Al(OH)6]3– , [Sn(OH)6]2–; CrO 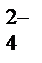 ; [Zn(OH)4]2–; AsO ; [Zn(OH)4]2–; AsO 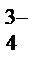 (желтый раствор в присутствии Cr3+, бесцветный раствор в отсутствии Cr3+) (желтый раствор в присутствии Cr3+, бесцветный раствор в отсутствии Cr3+)
|
| Осаждение Al(OH)3 и Sn(OH)4 | К раствору 1 + крист. NH4Cl до запаха NH3 и упаривают до небольшого объема | Осадок 1: Al(OH)3 Sn(OH)4
Раствор 2: [Zn(NH3)4]2+, CrO 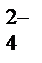 , AsO , AsO 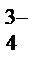
|
| Растворение осадка 1 | Осадок 1 растворяют в 2 моль/л HCl | Раствор 3: Al3+; [SnCl6]2– |
| Обнаружение ионов алюминия и олова | В растворе 3 обнаруживают Al3+ реакцией с ализарином. Раствор 3 кипятят с железными опилками. После охлаждения отделяют опилки фильтрованием. К фильтрату + избыток 6 моль/л раствора NaOH (рН>10) и после удаления Fe(OH)2 обнаруживают Sn (II) реакцией с Bi3+ | Розовое пятно на фильтровальной бумаге Черный осадок Bi |
| Осаждение гидроксокарбоната цинка | Раствор 2 нагревают при добавлении Na2CO3 (кр.) до полного удаления NH3 | Осадок 2: (ZnOH)2CO3
Раствор 4: CrO 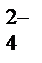 ; AsO ; AsO 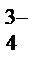
|
| Растворение осадка 2 | Осадок 2 растворяют в 2 моль/л растворе HCl | Раствор 5: Zn2+ |
| Обнаружение ионов Zn2+ в растворе 5 | В растворе 5 обнаруживают ионы Zn2+ реакциями с дитизоном или с [Hg(SCN)4]2– | Малиново-красное окрашивание хлороформного слоя с дитизоном или кристаллы характерной формы с [Hg(SCN)4]2– |
Обнаружение ионов CrO 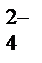 и AsO и AsO 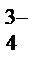 в растворе 4 в растворе 4
| В растворе 4 обнаруживают CrO 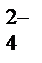 реакцией образования надхромовых кислот и AsO реакцией образования надхромовых кислот и AsO 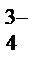 (качественные реакции AsO (качественные реакции AsO 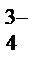 ) )
| Синий цвет слоя органического растворителя за счет H2CrO6 |
 2015-10-13
2015-10-13 475
475








