Очистку газов от твердых взвешенных в них частиц, например, пыли, проводят путем фильтрования через толстый слой ваты или другого материала, на который газ не действует.
В качестве фильтрующих материалов для газов можно применять стекловолокно, стеклянную или кварцевую вату, многие синтетические материалы, пластинки из пористого стекла. Газы, нагретые до высокой температуры, можно фильтровать через минеральные волокнистые материалы, стеклянную или кварцевую вату, а также через пластинки из пористого стекла.
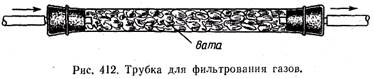 Для фильтрования газов очень удобно применять поглотительную колонку Фрезениуса, наполненную ватой, или же U-образные хлоркальциевые трубки. Газ можно фильтровать также через широкую стеклянную трубку (рис.412), наполненную ватой или асбестом.
Для фильтрования газов очень удобно применять поглотительную колонку Фрезениуса, наполненную ватой, или же U-образные хлоркальциевые трубки. Газ можно фильтровать также через широкую стеклянную трубку (рис.412), наполненную ватой или асбестом.
Если фильтруемый газ идет под небольшим давлением, пробки должны быть прикреплены к концам трубки. Для фильтрования газов, идущих под значительным давлением, такую трубку применять нельзя.
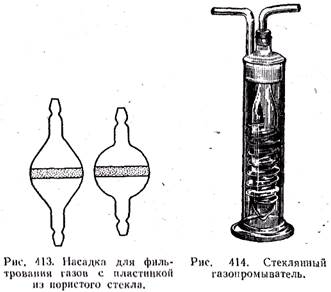
Очень удобны специальные насадки с перегородкой из вплавленной фильтрующей пластинки из пористого стекла (рис.413). Они устойчивы к влажным и корродирующим газам, однако их можно применять только в том случае, если газовая струя идет с давлением, не превышающим 1 кг/см2.
Для промывки газов и очистки их от твердых частиц очень хорошо применять стеклянный газопромыватель (рис.414). Его заполняют водой или серной кислотой.
 Кроме того, для промывания газов применяют описанные выше склянки Дрекселя, Тищенко и Вульфа. Для этих же целей можно использовать колбу Бунзена. В ее горло вставляют резиновую пробку, снабженную стеклянной трубкой. Эта трубка должна доходить почти до дна колбы и выступать наружу примерно на 5 см.
Кроме того, для промывания газов применяют описанные выше склянки Дрекселя, Тищенко и Вульфа. Для этих же целей можно использовать колбу Бунзена. В ее горло вставляют резиновую пробку, снабженную стеклянной трубкой. Эта трубка должна доходить почти до дна колбы и выступать наружу примерно на 5 см.
Для разделения смеси газов ее пропускают через растворы, поглоща-ющие те или иные газы. Так, для отделения кислорода применяют влаж-ный фосфор, пирогаллол (пользую-щийся наибольшим распространением), гидросульфит натрия, аммиачный раствор закиси меди и др.
Для получения поглотительного раствора пирогаллола отдельно приготовляют 25%-ный раствор пирогаллола и 60%-ный раствор едкого кали; затем берут на 1 объем раствора пирогаллола 5 объемов раствора едкого кали и смешивают, избегая окисления смеси кислородом воздуха. Лучше всего смешивание проводить в том сосуде, в котором будет происходить поглощение кислорода (пипетки для поглощения, склянки Дрекселя и пр.); 1 мл такого раствора поглощает 13 мл кислорода.
Хорошим поглотителем является также раствор пирогаллола, рекомендуемый Гофманом. Растворяют 40 г пирогаллола в 90 мл воды и этот раствор смешивают с 70 г (45 мл) концентрированного раствора едкого кали (d420 = 1,55) при соблюдении указанных выше условий.
При изготовлении поглотительных растворов пирогаллола нужно брать именно едкое кали, а не едкий натр, так как с последним поглощение идет хуже и медленнее.
Обычно бывает достаточно одного прибора с раствором пирогаллола; нужно следить, чтобы газ пропускался не очень сильной струей. Для большей уверенности в том, что кислород поглощается полностью, иногда берут два поглотительных прибора и соединяют их последовательно.
Для поглощения кислорода вместо обычного пирогаллола применяют так называемый пирогаллол А. Он представляет собой триацетат оксигидрохинона (1,2,4-триоксибензол); поглотительная способность пирогаллола А такая же, как и у пирогаллола.
Преимущество пирогаллола А перед обычным пирогаллолом состоит в том, что при поглощении им кислорода не выделяется окись углерода.
Вместо раствора пирогаллола можно пользоваться раствором CrCl2. Для получения раствора CrCl2 сначала растворяют 40 г Cr(ОН)3 в 100 мл 2 н. раствора HCl или же 193 г хромовых квасцов в 1 л воды и осаждают гидроокись хрома концентрированным раствором NH4OH. Осадок Cr(ОН)3 промывают водой до отрицательной реакции на ионы SO42‾; 40 г гидроокиси хрома растворяют в 200 мл 2н. раствора HCl. В растворе образуется CrCl3, который восстанавливают до CrCl2 амальгамой цинка. Для изготовления последней к 100 г металлической ртути прибавляюn 5 г гранулированного цинка, несколько миллилитров 2н. раствора HCl и при помешивании нагревают на водяной бане до полного растворения цинка. Охлажденную амальгаму промывают водой с применением декантации, добавляют солянокислый раствор CrCl3 и взбалтывают до изменения зеленой окраски в голубую. Полученным раствором CrCl2 заполняют поглотительную пипетку газоанализатора, предназначенную для поглощения кислорода; 1 мл 20%-ного раствора CrCl2 поглощает 9 мл кислорода.
Отработанный раствор регенерируют взбалтыванием его с амальгамой цинка, как описано выше. Поглощение кислорода протекает по уравнению:
4 CrCl2 + О2 + 4HCl → 4 CrCl3 + 2Н2О
Для поглощения азота можно применять металлический кальций при красном калении, когда он жадно поглощает азот, или же смесь, состоящую из 1 части магниевого порошка и 5 частей СаО (свежеобожженного) в виде зерен c размером макового зерна. Перед употреблением следует добавить 0,25 части тонко нарезанного металлического натрия. Поглощение азота проводят при светло-красном калении этой смеси.
В качестве поглотителя кислорода при газовом анализе используют также кальциевую соль гидрохинон. С кислородом она очень активно реагирует как в твердом, слегка увлажненном состоянии, так и в водных растворах.
Для этой же цели применяют щелочной раствор таннина. Для приготовления этого раствора 24 г таннина (галлотаннин или скумпиевый таннин) растворяют в 150 мл 17,5-18%-ного раствора КОН.
А.С. Садыков и А. Исмаилов (АН КазССР) предложили заменять пирогаллол госсиполом, получаемым из коры корней хлопчатника. По эффекту поглощения кислорода госсипол аналогичен пирогаллолу и поэтому с успехом может заменять последний.
Для связывания кислорода, растворенного в воде, иногда применяют сульфит натрия. Для этих же целей хорошие результаты дает применение гидразина.
Для очистки инертных и восстановительных газов от следов кислорода рекомендуется использовать промывалку, заполненную амальгамой алюминия. Применение амальгамы позволяет снизить содержание кислорода в пробе до ничтожно малого. Для этой цели используют также амальгамы магния и кальция. Для облегчения соприкосновения газа с амальгамой промывалку непрерывно встряхивают или используют магнитную мешалку.
Для отделения СО газовую смесь обычно пропускают через раствор CuCl2, приготовляемый растворением 1 г Cu2Cl2 в 20%-ной HCl.
Окись углерода поглощают раствором CuCl2. Для этого взбалтывают 200 г CuCl2 с раствором 250 г NH4Cl в 750 мл воды в закупоренной склянке, в которую потом вставляют доходящую до шейки медную спираль. Перед наполнением поглотительного сосуда 3 объема этого раствора смешивают с 1 объемом водного раствора аммиака (d420 = 0,903). 1 мл этого раствора поглощает 16 мл СО.
Раствор следует часто менять, так как он может отдавать СО более бедному этим соединением газу. Он поглощает также кислород и применим лишь после предварительного удаления кислорода из газовой смеси.
Для поглощения СО из газовых смесей рекомендованы также аммиачные растворы однохлористой меди примерно следующего состава: Cu2Cl2 – 11-12 частей, NH3 – 13-14 частей, вода – 74-76 частей, т. е. навеску Cu2Cl2 растворяют приблизительно в 90 мл раствора NH3 (d420 = 0,940); 1мл этого раствора поглощает 31 мл СО.
Для стабилизации раствора рекомендуется добавлять NH4C1 в количестве 10% по массе от количества Cu2Cl2.
Аммиачные растворы Cu2Cl2 выделяют NH3. Поэтому после прибора ставят газопромыватель с 86%-ной серной кислотой для поглощения аммиака. Следует отметить, что растворы однохлористой меди не полностью поглощают СО, и поэтому дли абсорбции остатков СО газовую смесь необходимо пропускать через газовую пипетку с β-нафтолом.
 2015-10-22
2015-10-22 1347
1347