(№ 221 – 246)
221−224. Укажите, с какими из перечисленных растворов стандартной концентрации будет взаимодействовать приведенный в таблице металл? Ответ обоснуйте, используя стандартные значения электродных потенциалов металлов. Приведите ионно-электронные уравнения возможных процессов.
| № задачи | Металл | Стандартные растворы солей |
| Zn | Na2SO4, MgCl2, CuSO4, AlCl3, AuCl3 | |
| Mg | CuCl2, K2SO4, MnSO4, NaNO3 | |
| Al | MgCl2, CuSO4, Na2SO4, AgNO3 | |
| Ni | FeCl2, CoCl2, SnCl2, CuCl2, K2SO4 | |
| Fe | СuSO4, МgSO4, Рb(NO3)2, MnCl2, AgNO3 | |
| Cu | MnSO4, SnSO4, AgNO3, Hg2(NO3)2, ZnCl2 |
227–232. Вычислите электродный потенциал металла (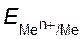 ), находящегося в растворах солей, содержащих собственные ионы, с концентрацией ионов металла [Men+] моль/л. Укажите, на какую величину изменится электродный потенциал, если увеличить концентрацию раствора соли в 10 раз?
), находящегося в растворах солей, содержащих собственные ионы, с концентрацией ионов металла [Men+] моль/л. Укажите, на какую величину изменится электродный потенциал, если увеличить концентрацию раствора соли в 10 раз?
| № задачи | Металл | Раствор соли | Концентрация ионов металла [Men+], моль/л |
| Mn | MnCl2 | 0,01 | |
| Zn | ZnSO4 | 0,1 | |
| Ni | Ni(NO3)2 | 0,001 | |
| Cr | Cr2(SO4)2 | 0,1 | |
| Cu | CuSO4 | 0,01 | |
| Fe | FeSO4 | 0,1 |
233–237. Вычислите электродвижущую силу гальванического элемента. Определите направление движения электронов во внешней цепи:
233. Sn/Sn2+ (0,01моль/л) || (0,1моль/л) Sn2+/ Sn.
234. Cu/Cu2+ (1 моль/л) || (0,01моль/л) Cu2+/Cu.
235. Cr/Cr3+ (0,1 моль/л) || (0,01 моль/л) Fe2+/Fe.
236. Al/Al3+ (0,1 моль/л) || (0,01 моль/л) Mg2+/Mg.
237. Ni/Ni2+ (0,01 моль/л) || (0,01 моль/л) Sn2+/Sn.
238–242. Какие окислительно-восстановительные процессы протекают на электродах данных гальванических элементов? На основании стандартных электродных потенциалов выберите гальванический элемент с наибольшей электродвижущей силой и рассчитайте ее величину:
238. Cu/Cu(NO3)2 || Pb(NO3)2/Pb; Cr/CrCl3 || CuCl2/Cu.
239. Ni/NiCl2 || AlCl3/Al; Co/CoCl2 || AlCl3/Al; Zn/ZnCl2 || AlCl3/Al.
240. Cr/CrCl3 II NiCl2/Ni; Cr/CrCl3 II CoCl2/Co; Cr/CrCl3 II CuCl2/Cu.
241. Zn/Zn(NO3)2 || AgNO3/Ag; Zn/Zn(NO3)2 || Cu(NO3)2/Cu.
242. Pb/Pb(NO3)2 || Fe(NO3)2/Fe; Pb/Pb(NO3)2 || Ni(NO3)2/Ni.
243–246. Какие окислительно-восстановительные процессы протекают на электродах предложенных гальванических элементов? Укажите, какой из них является поляризующимся? Составьте схему работы этого элемента:
243. Zn/H2SO4 || CuSO4/Cu; Zn/ZnSO4 || CuSO4/Cu.
244. Ni/H2SO4 ||CuSO4/Cu; Ni/NiSO4 || H2SO4/Cu.
245. Ni/NiCl2 || HCl/Sn; Ni/HCl ||CuCl2/Cu; Ni/NiCl2 || SnCl2/Sn.
246. Fe/FeCl2|| CuCl2/Cu; Fe/HCl || CuCl2/Cu; Fe/FeCl2 || HCl/Cu.
ЭЛЕКТРОЛИЗ
(№ 247 – 270)
247. Рассмотрите процессы, протекающие на электродах при электролизе расплава и водного раствора СаСl2.
248. Рассмотрите процессы, протекающие на электродах при электролизе расплава и водного раствора NaОН.
249. Вычислите объемы водорода и кислорода при н.у., выделившихся на электродах при электролизе водного раствора КОН при силе тока 10 А в течение 1,5 ч.
250. Вычислите коэффициенты выхода по току веществ, если при электролизе водного раствора NaJ током 5 А в течение 2 ч на катоде и аноде выделилось соответственно 0,30 и 46 г веществ.
251. Рассчитайте, какое количество электричества должно пройти через раствор в электролизере, чтобы получить 100 г NaOH? Коэффициент выхода по току считать равным единице.
252. Рассчитайте, какое количество электричества должно пройти через раствор в электролизере, чтобы получить 100 г Na2SO4? Коэффициент выхода по току считать равным единице.
253. При электролизе соли некоторого металла в течение 1,5 ч при силе тока 1,8 А на катоде выделилось 1,75 г металла. Вычислите эквивалентную массу металла.
254. При электролизе водного раствора CuSO4 на аноде выделилось 168 мл газа (н.у.). Составьте электронные уравнения процессов, происходящих на электродах, и вычислите, какое количество меди выделилось на катоде.
255. Электролиз водного раствора K2SO4 проводили при силе тока 5 А в течение 3 ч. Составьте электронные уравнения процессов, происходящих на электродах. Рассчитайте объем газов (н.у.), выделившихся на электродах?
256. Электролиз водного раствора нитрата серебра проводили при силе тока 2 А в течение 4 ч. Составьте электронные уравнения процессов, происходящих на электродах. Какой объем газа (н.у.) выделился на аноде?
257. Электролиз водного раствора сульфата цинка проводили в течение 5 ч, в результате чего выделилось 6 л кислорода (н.у.). Составьте уравнения электродных процессов, происходящих на угольных электродах, и вычислите силу тока.
258. Электролиз водного раствора CuSO4 проводили в течение 3 ч при силе тока 5 А с растворимым медным анодом. В процессе электролиза выделилось 224 г меди. Вычислите выход по току. Составьте уравнения процессов, происходящих на электродах.
259. Электролиз водного раствора NaJ проводили при силе тока 6 А в течение 2,5 ч. Составьте электронные уравнения процессов, происходящих на угольных электродах, и вычислите массу вещества, выделившегося на катоде и аноде.
260. Электролиз водного раствора CuSO4 проводили в течение 3 ч при силе тока 5 А в течение 15 мин. В процессе электролиза выделилось 0,72 г меди. Составьте уравнения процессов, происходящих на электродах в случае медного и угольного анодов. Вычислите выход по току.
261. Составьте электронные уравнения процессов, происходящих на графитовых электродах при электролизе водного раствора KOH. Сколько литров (н.у.) газа выделится при электролизе водного раствора гидроксида калия, если электролиз проводить в течение 30 мин при силе тока 0,5 А.
262. Составьте электронные уравнения процессов, происходящих на графитовых электродах при электролизе водного раствора KBr. Какая масса вещества выделяется на катоде и аноде, если электролиз проводить в течение 1 ч 35 мин при силе тока 15 А.
263. Составьте электронные уравнения процессов, происходящих на угольных электродах при электролизе водного раствора СuСl2. Определите, какая масса меди выделилась на катоде, если на аноде выделилось 500 мл газа (н.у.).
264. Приведите анодные и катодные процессы при рафинировании чернового никеля, содержащего примеси цинка и меди. Укажите последовательность выделения катодных и анодных процессов?
265. Составьте электронные уравнения процессов, происходящих на угольных электродах при электролизе водного раствора Na2SO4. Вычислите массу вещества, выделенного на катоде, если на аноде выделилось 1,12 л газа (н.у.).
266. При электролизе раствора соли кадмия израсходовано 3434 Кл электричества. При этом выделилось 2 г кадмия. Вычислите эквивалентную массу кадмия.
267. Составьте электронные уравнения процессов, происходящих на угольных электродах при электролизе раствора КОН. Чему равна сила тока, если в течение 1 ч 15 мин 20 с на аноде выделилось 6,4 г газа. Рассчитайте, сколько литров газа (н.у.) выделилось при этом на катоде?
268. Рассмотрите анодные и катодные процессы, происходящие при анодировании алюминия. Приведите уравнения электродных процессов
269. Приведите анодные и катодные процессы при рафинировании черновой меди, содержащей примеси цинка, никеля, железа. Укажите последовательность выделения катодных и анодных процессов?
270. Определите толщину слоя цинка, выделившегося в течение 10 мин на железном катоде площадью 500 см2 при электролизе водного раствора ZnCl2 с растворимым анодом силой тока, равной 2 А, и приведите уравнения процессов, ппоисходящих на электродах. Коэффициент выхода по току составил 0,9. Плотность цинка равна 7,15 г/см3.
КОРРОЗИЯ МЕТАЛЛОВ
(№ 271 – 300)
271−280. Какие окислительно-восстановительные процессы происходят при контакте железного изделия (Fe) с представленными в табл. металлами (Me)? Укажите, какой металл при этом окисляется? Приведите уравнения электродных процессов. Составьте схемы работы гальванических элементов, образующихся при коррозии металлов в данных условиях.
| № задачи | Металлы, контактирующие с железным изделием (Fe/Me) | Коррозионная среда |
| Zn, Cr | раствор H2SO4 | |
| Zn, Cu | влажная атмосфера (Н2О+О2) | |
| Ni, Cr | влажная промышленная атмосфера (H2O, SO2, HCl, CO2) | |
| Sn, Al | пресная вода | |
| Ag, Cr | pН <7 (отсутствие кислорода) | |
| Co, Mg | влажная атмосфера (Н2О+О2) | |
| Zn, Sn | морская вода (Н2О+Cl-) | |
| Cd, Ni | раствор электролита (рН > 7) | |
| Mg, Sn | влажная промышленная атмосфера (H2O, SO2, HCl, CO2) | |
| Pb, Cd | влажная атмосфера (Н2О+О2) |
281−285. Железная пластина (Fe) имеет покрытие из другого металла. Какой из металлов (железо или металл покрытия) будет разрушаться в случае нарушения поверхностного слоя покрытия? Составьте схемы процессов, происходящих на электродах образующихся гальванических элементов в указанных средах.
| № задачи | Металл покрытия | Коррозионная среда |
| Cu, Mg | пресная вода | |
| Zn, Sn | морская вода (Cl−) | |
| Sn, Al | кислая среда | |
| Ag, Zn | влажная атмосфера (Н2О+О2) | |
| Ni, Ag | влажная промышленная атмосфера (H2O, SO2, HCl, CO2) |
286–290. Металл (Ме1) находится в контакте с другим металлом (Ме2). Укажите, какой из металлов будет подвергаться коррозии? Приведите уравнения электродных процессов, схемы образующихся микрогальванических элементов и рассчитайте ЭДС при стандартных условиях.
| № задачи | Ме1/Ме2 | Коррозионная среда |
| Al/Cu | влажная атмосфера (Н2О+О2) | |
| Al/Cu | кислый водный раствор (предполагается отсутствие О2) | |
| Sn/Fe | влажная промышленная атмосфера | |
| Sn/Fe | влажная атмосфера (Н2О+О2) | |
| Cu/Zn | морская вода |
291–294. Укажите, какой металл можно использовать в качестве протектора для защиты изделия от коррозии в водных растворах в контакте с воздухом? Приведите уравнения электродных процессов и схемы образующихся микрогальванических элементов.
| № задачи | Изделие | № задачи | Изделие |
| Fe | Zn | ||
| Sn | Ni |
295–298. Рассмотрите коррозию изделия в электролите, содержащем соляную кислоту. Приведите уравнения электродных процессов и схемы образующихся гальванических элементов.
| № задачи | Изделие | № задачи | Изделие |
| оловянистая бронза (Cu/Sn 8…10%) | cплав Sn/Ag | ||
| сплав Cu/Ag | луженое железо |
299–300. Рассмотрите коррозию изделия во влажной атмосфере. Приведите уравнения электродных процессов, состав продуктов коррозии и схемы образующихся коррозионных гальванических элементов.
| № задачи | Изделие | № задачи | Изделие |
| латунь (сплав Cu/Zn) | алюминиевая бронза (Cu/Al) |
ПРИЛОЖЕНИЕ
Таблица 1
Основные физико-химические константы
| Величина | Обозначение | Численное значение |
| Заряд электрона и протона (элементарный электрический заряд) | e | 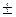 1,6022 · 10 −19 Кл 1,6022 · 10 −19 Кл |
| Масса электрона | me | 9,1094 ·10 −31 кг |
| Масса протона и нейтрона | mp, mn | 1,6726 · 10 −27 кг |
| Постоянная (число) Авогадро | NA | 6,0221 · 10 23 моль−1 |
| Газовая постоянная | R | 8,31 Дж · моль−1· K–1; 8,31 Вт · с · моль−1· K–1; 2,31 кВт · ч · моль−1· K–1; 0,0821 л · атм · моль−1· K –1 |
| Постоянная Больцмана k = R / NA | k | 1,3807·10 −23 Дж · К−1 |
| Постоянная (число) Фарадея F = N А · е | F | 96485,3 Кл · моль−1 |
| Постоянная Планка | h | 6,6261 ·10 –34 Дж · с |
| Электрон-вольт | эВ | 1,6022 ·10 −19 Дж |
| Нормальные условия | н.у. | ро = 101,3 кПа; То = 273,15 К |
| Нормальный молярный объем газа | Vо | 22,4 л/моль |
| Стандартные термодинамические условия | р = 101,3 кПа; Т = 298,15 К | |
| Скорость света в вакууме | С | 2,9979 · 10 8 м · с−1 |
Таблица 2
 2015-10-22
2015-10-22 2783
2783
