При электролизе в водном растворе серной кислоты с инертными (платиновыми, свинцовыми или графитовыми) электродами электрический ток переносится ионами H3O+ и SO42-. Ионы SO42- из катодного пространства перемещаются к аноду, однако окисляются на аноде молекулы воды с выделением O2:
2H2O – 4 e- ® O2 + 4H+. (21)
Ионы H3O+ перемещаются к катоду и восстанавливаются на нем с выделением водорода:
2H3O+ + 2 e - ® H2 + 2H2O. (22)
Таким образом, при электролизе в водном растворе серной кислоты с инертными электродами происходит разложение воды и разрядка ионов H+.
В этом случае количество эквивалентов ионов SO42- в анодном и катодном пространствах изменяется только за счет переноса электричества.
Количество эквивалентов ионов водорода: в катодном пространстве – убывает из-за разрядки на электроде, но прибывает переносом электрического тока; в анодном пространстве прибывает за счет разложения воды при электролизе и убывает переносом электрического тока.
В результате количество эквивалентов H2SO4 у анода возрастает, а у катода происходит их уменьшение.
Число переноса аниона находят по отношению изменения количества эквивалентов кислоты у анода (или катода) к общему количеству эквивалентов разложившегося электролита:
 (23)
(23)
Изменение состава раствора серной кислоты после электролиза представлено в таблице 3.
Таблица 3 – Изменение состава раствора серной кислоты
| Катодное пространство (К) | Анодное пространство (А) |
Убыль катионов Н+:  Убыль анионов SO42-: Убыль анионов SO42-:  Соблюдается равенство: Соблюдается равенство:  | Прибыль катионов Н+: 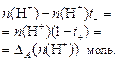 Прибыль анионов SO42-: Прибыль анионов SO42-:  Соблюдается равенство: Соблюдается равенство:  |
 2015-10-22
2015-10-22 5916
5916
