Характеристика ячейки зависит от площади платиновых электродов и расстояния между ними. Для ячейки ее значение постоянное и называется постоянной ячейки K:
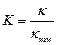 , (110)
, (110)
где k – удельная электропроводность раствора, См×см-1;
k изм– измеренное значение электропроводности раствора, См×см-1.
Оценку значения постоянной ячейки проводят, используя раствор хлорида калия. Значения удельной электропроводности раствора хлорида калия приведены в таблице 8.2.
Измеряют электропроводность двух растворов хлорида калия (с (KCl) = 0.01 моль/дм3 и с (KCl) = 0.02 моль/дм3 ) при комнатной температуре, помещая их последовательно в специальную проточную ячейку или стакан, выполняющий роль ячейки.
Рассчитывают:
– значение K, измеренное с использованием каждого из двух растворов хлорида калия;
– среднее двух значений постоянной ячейки – 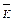 ;
;
– стандартное отклонение постоянной ячейки –  .
.
Таблица 8.2 – Удельная электропроводность раствора хлорида калия при различной температуре
| Молярная концентрация с (KCl), моль/дм3 | Температура, Т, °С | ||||||||||
| Удельная электропроводность, k, мСм×см-1 | |||||||||||
| 0.01 | 1.15 | 1.17 | 1.20 | 1.22 | 1.25 | 1.28 | 1.30 | 1.33 | 1.36 | 1.39 | 1.41 |
| 0.02 | 2.24 | 2.29 | 2.34 | 2.40 | 2.45 | 2.50 | 2.55 | 2.61 | 2.66 | 2.71 | 2.76 |
1 Измерение 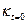
Готовят 400 см3 раствора гидроксида натрия (с (OH-) выбирают в таблице 8.3).
В стакан мерной пипеткой отбирают рассчитанный объем раствора гидроксида натрия (с (OH-) = 1 моль/дм3) и мерным цилиндром дистиллированной воды.
В колбу для титрования помещают мерной пипеткой аликвотную часть (Va = 25 см3) приготовленного раствора гидроксида натрия и титруют раствором хлороводородной или серной кислот
(с (H+) = 0.05 моль/дм3) в присутствии фенолфталеина. Повторяют титрование еще один раз.
Рассчитывают молярную концентрацию гидроксида натрия в приготовленном растворе:  ,моль/дм3.
,моль/дм3.
В сухую ячейку наливают раствор гидроксида натрия и измеряют его удельную электропроводность – kt =0 при комнатной температуре.
 2015-10-22
2015-10-22 905
905








