Рассмотрим теперь влияние внешнего силового поля, например, силы тяжести на поведение молекул идеального газа. Если бы отсутствовало тепловое движение, то все молекулы под действием силы тяжести скопились бы у поверхности Земли, и, наоборот, в отсутствие силы тяжести все молекулы разлетелись бы по всему пространству. Одновременное действие обоих процессов и приводит к установлению определенного распределения молекул по высоте, соответственно чему распределяется и давление газа. Рассмотрим вертикальный столб газа (Рис. 8.3). При изменении высоты на  давление меняется на
давление меняется на  . На некоторой высоте оно равно давлению столба газа:
. На некоторой высоте оно равно давлению столба газа:
 (8.7)
(8.7)
 где
где  - плотность газа,
- плотность газа, 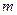 - масса молекулы,
- масса молекулы,  - концентрация молекул. Из формулы (7.10). находим
- концентрация молекул. Из формулы (7.10). находим  и
и 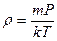 . Подставив это в (8.7), получим:
. Подставив это в (8.7), получим:  , откуда находим:
, откуда находим:
 (8.8)
(8.8)
Так как 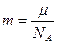 ,
,  , то вместо (8.8) получим:
, то вместо (8.8) получим:
 (8.9)
(8.9)
Формулы (8.8) и (8.9), устанавливающие закон убывания давления с высотой, называют барометрической формулой.
Так как давление газа пропорционально числу молекул, то (8.8) и (8.9) выражают также и закон убывания концентраций молекул:
 (8.10)
(8.10)
Эта формула была использована Перроном (1909 г.) для опытней проверки барометрической формулы и числа Авогадро. В формуле (8.10)  есть потенциальная энергия молекулы на высоте, то есть эта формула определяет число молекул (частиц) с энергией
есть потенциальная энергия молекулы на высоте, то есть эта формула определяет число молекул (частиц) с энергией  при нулевом уровне потенциальной энергии.
при нулевом уровне потенциальной энергии.
Если газ находится в другом силовом поле, так что его потенциальная энергия  , то число частиц с такой энергией определится формулой:
, то число частиц с такой энергией определится формулой:
 (8.11)
(8.11)
Эту формулу называют формулой Больцмана.
 2015-10-22
2015-10-22 350
350








