Внутренняя энергия реального газа будет состоять из кинетической энергии молекул - внутренней энергии идеального газа  , которая для 1 моля равна
, которая для 1 моля равна  , и потенциальной энергии взаимодействия между молекулами
, и потенциальной энергии взаимодействия между молекулами 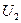 так что:
так что:

При расширении газа силы молекулярного давления 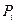 совершают работу, равную изменению потенциальной энергии:
совершают работу, равную изменению потенциальной энергии:
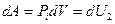 , откуда
, откуда  и
и 
При  , поэтому
, поэтому 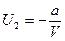 , а
, а
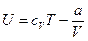 (11.5)
(11.5)
Наличие потенциальной энергии взаимодействия между молекулами у реального, газа приводит к изменению его температуры при адиабатическом расширении эффект Джоуля-Томпсона.
Например, если осуществить адиабатное расширение реального газа без совершения внешней работы (расширение в вакуум), то на оснований первого закона термодинамики при 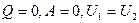 или
или  ,
,
откуда:
 ,
,
т.к. при расширении  , то
, то  - реальный газ при атом охлаждается.
- реальный газ при атом охлаждается.
В процессе Джоуля-Томпсона осуществлялось расширение газа без теплообмена при постоянных давлениях. Для этого газ пропускался через пористую перегородку, чем обеспечивалась медленность процесса. При этой было установлено, что знак  зависит от природы газа, его начальной температуры
зависит от природы газа, его начальной температуры  , плотности.
, плотности.
Если температура газа понижается,  , то эффект считается положительный, если
, то эффект считается положительный, если  - эффект отрицательный.
- эффект отрицательный.
Знак эффекта зависит от относительной роли поправок 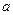 и
и  в уравнении Ван-дер-Ваальса. При высоких температурах эффект отрицательный, при низких - положительный. Температура, при которой эффект Джоуля-Томпсона меняет знак, называется температурой (точкой) инверсии. Выше этой температуре эффект всегда отрицательный. Так, для гелия точка инверсии - 40, водорода - 200, кислорода - 1063, углекислого газа - 2073 К и т.п.
в уравнении Ван-дер-Ваальса. При высоких температурах эффект отрицательный, при низких - положительный. Температура, при которой эффект Джоуля-Томпсона меняет знак, называется температурой (точкой) инверсии. Выше этой температуре эффект всегда отрицательный. Так, для гелия точка инверсии - 40, водорода - 200, кислорода - 1063, углекислого газа - 2073 К и т.п.
Охлаждение газов в процессе Джоуля-Томпсона может быть значительным. Так, воздух при расширении от 200 до 1 атм охлаждается на 40 К. Поэтому положительный эффект Джоуля-Томпсона используется для снижения газов.
| Лекция 19 | Жидкости, их строение. Диффузия и вязкость. |
| Поверхностное натяжение, смачивание и капиллярные явления. Поверхностно –активные вещества. |
ЖИДКОСТИ.
Жидкость представляет собой агрегатное состояние вещества, в котором проявляются как свойства твердого состояния - занимать определенный ограниченный объем, сохранять прочность отрыву частиц, так и газообразного - изменчивость формы.
Одним из основных физических свойств жидкости является вязкость. Вязкость или внутреннее трение - свойство газов и жидкостей, характеризующее сопротивление действию внешних сил вызывающих их течение. Она оценивается коэффициентом вязкости  , от которого зависит сила внутреннего трения между двумя слоями жидкости при их относительном движении. В отличие от газов, где вязкость возрастает о увеличением температуры, в жидкостях вязкость с увеличением температуры резко убывает по закону:
, от которого зависит сила внутреннего трения между двумя слоями жидкости при их относительном движении. В отличие от газов, где вязкость возрастает о увеличением температуры, в жидкостях вязкость с увеличением температуры резко убывает по закону:
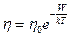 (12.1)
(12.1)
где 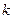 - постоянная Больцмана,
- постоянная Больцмана, 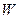 - энергия перехода молекулы жидкости из одного положения в другое.
- энергия перехода молекулы жидкости из одного положения в другое.
Для жидкостей имеет место ближний порядок в расположении частиц и малое различие в кинетической энергии теплового движения молекул и потенциальной энергии их взаимодействия. Тепловое движений молекул жидкости состоит из колебательного движения молекул около положения равновесия и пароходов от одного равновесного положения в другое. С этим связана текучесть жидкости, которая, оценивается величиной 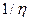 . Таким образом, в отличие от твердых тел жидкость имеет "рыхлую" структуру. В то же время молекулы жидкости находятся на таких же расстояниях друг от друга, как и в твердом теле. На это указывает тот факт, что плотности вещества в твердом и жидком состоянии примерно одинаковы, а, например, для воды наоборот: плотность льда меньше.
. Таким образом, в отличие от твердых тел жидкость имеет "рыхлую" структуру. В то же время молекулы жидкости находятся на таких же расстояниях друг от друга, как и в твердом теле. На это указывает тот факт, что плотности вещества в твердом и жидком состоянии примерно одинаковы, а, например, для воды наоборот: плотность льда меньше.
Термодинамические величины, характеризующие такие свойства жидкости, как плотность теплоемкость и т.д. не имеют простой и одновременно строгой температурной зависимости как у газов, т.е. вследствие проявления сил межмолекулярного взаимодействия найти простое уравнение состояния для жидкостей как для газов не представляется возможным.
 2015-10-22
2015-10-22 648
648








