Уравнение состояния идеального газа (Менделеева-Клапейрона) является приближенным. Оно выполняется при достаточно малых плотностях и давлениях (до 100 атм). Так, например, для одного моля азота при  С и
С и  атм
атм 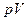 отличается от теоретического более чем на
отличается от теоретического более чем на  , а при
, а при  атм - на
атм - на  . При дальнейшем увеличении давления это отклонение еще больше.
. При дальнейшем увеличении давления это отклонение еще больше.
 Таким образом, опыт показывает, что реальные газы значительно отличаются по своим свойствам от идеальных. Такие отклонения связаны с межмолекулярным взаимодействием и размерами самих молекул, чем нельзя пренебрегать при больших плотностях газа. Между молекулами действую силы электрического происхождения - притягивания и отталкивания. Характер этих сил показан на рис. 11.1, где приведена зависимость потенциальной энергии взаимодействия от расстояния. На расстоянии
Таким образом, опыт показывает, что реальные газы значительно отличаются по своим свойствам от идеальных. Такие отклонения связаны с межмолекулярным взаимодействием и размерами самих молекул, чем нельзя пренебрегать при больших плотностях газа. Между молекулами действую силы электрического происхождения - притягивания и отталкивания. Характер этих сил показан на рис. 11.1, где приведена зависимость потенциальной энергии взаимодействия от расстояния. На расстоянии  силы притяжения уравновешиваются силами отталкивания. Действие сил притяжения приводит к тому, что молекулы газа занимают определенный объем, дальше которого газ не может быть сжат.
силы притяжения уравновешиваются силами отталкивания. Действие сил притяжения приводит к тому, что молекулы газа занимают определенный объем, дальше которого газ не может быть сжат.
Поэтому уравнение Менделеева-Клапейрона, справедливое для идеальных газов, необходимо уточнить с учетом размера молекул и сил взаимодействия между ними.
 2015-10-22
2015-10-22 1983
1983








