Согласно квантовой механике, область пространства в электронном облаке, в которой вероятность нахождения электрона наибольшая, называется орбиталью.
Формы электронных облаков:
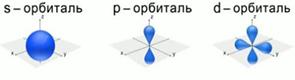
f-орбиталь имеет более сложную форму.
1. s -форма электронного облака (s – «sharp» - резкая, отчётливая) (s -орбиталь) – «шарообразного» вида.
2. p форма электронного облака (p – «principal» - главная) (p -орбиталь) – вида «объёмной симметричной восьмерки».
3. d -форма электронного облака (d – «diffuse» - диффузная, размытая) (d -орбиталь) – вида «простого цветка».
4. f -форма электронного облака (f – «fundamental» - основная) (f -орбиталь) – вида «сложного цветка».
Положение электронных облаков в пространстве.
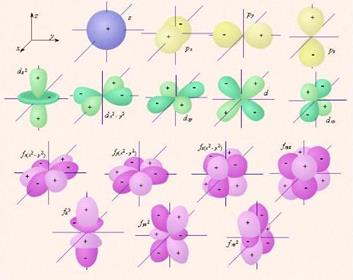


 s-орбиталь имеет одно положение в пространстве.
s-орбиталь имеет одно положение в пространстве.
| | |
| | |
p-орбиталь имеет три положения в пространстве.
d-орбиталь имеет пять положений в пространстве.
| | |
f-орбиталь имеет семь положений в пространстве.
| | |


 Правило 1: На одной орбитале может быть не более двух электронов и, обязательно, с противоположными спинами.
Правило 1: На одной орбитале может быть не более двух электронов и, обязательно, с противоположными спинами.
| ↑↓ |
s-орбиталь, максимум - 2e-
| ↑↓ | ↑↓ | ↑↓ |
p-орбиталь, максимум - 6e-
| ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ |
d-орбиталь, максимум - 10e-
| ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ | ↑↓ |
f-орбиталь, максимум - 14e-
Обозначения:
- свободная орбиталь (без электронов),
| ↑ |
- орбиталь с неспаренным электроном,
| ↑↓ |
- орбиталь с электронной парой (с двумя электронами).
↑↑ нельзя ↑↑↑
 2017-10-25
2017-10-25 783
783








