Оксалат аммония с ионами щелочноземельных металлов образует белые кристаллические осадки оксалатов: ВаС2О4, SrC2О4 и СаС2О4:
Са2+ + С2О42- g СаС2О4
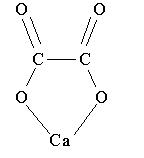
Аналогично протекают реакции с ионами Ва2+ и Sr2+.
Оксалаты всех щелочноземельных металлов растворяются в 2н растворе НС1 и HNO3 и не растворяются на холоду в 2н растворе СН3СООН.
В кипящей уксусной кислоте растворяются оксалаты бария и стронция и не растворяется оксалат кальция. В виду незначительной растворимости оксалата кальция в воде, реакция ионов Са2+ с ионами С2О42- очень чувствительна. Даже раствор сульфата кальция (гипсовая вода), содержащий незначительное количество ионов Са2+, выделяет с оксалат-ионом осадок СаС2О4, произведение растворимости которого (2·10-9) значительно меньше произведения растворимости CaSО4 (2,4 10-5).
Выполнение опыта:
Получить осадки оксалатов кальция и бария взаимодействием растворов соответствующих хлоридов (3-4 капли) с таким же объемом раствора оксалата аммония (NН4)2С2О4. Испытать действие соляной и уксусной кислот на осадки оксалатов.
Написать уравнения соответствующих реакций в ионной и молекулярной формах.
Примечание: реакции образования оксалата кальция применяется для осаждения ионов Са2+ при определении их содержания в моче и крови.
 2017-11-30
2017-11-30 1999
1999
