Теплотехника – наука, которая изучает методы получения, преобразования, передачи и использования теплоты, а также принципы действия и конструктивные особенности тепловых машин, аппаратов и устройств. Теплота используется во всех областях деятельности человека. Для установления наиболее рациональных способов его использования, анализа экономичности рабочих процессов тепловых установок и создания новых, наиболее совершенных типов тепловых агрегатов необходима разработка теоретических основ теплотехники. Различают два принципиально различных направления использования теплоты – энергетическое и технологическое. При энергетическом использовании, теплота преобразуется в механическую работу, с помощью которой в генераторах создается электрическая энергия, удобная для передачи на расстояние. Теплоту при этом получают сжиганием топлива в котельных установках или непосредственно в двигателях внутреннего сгорания. При технологическом - теплота используется для направленного изменения свойств различных тел (расплавления, затвердевания, изменения структуры, механических, физических, химических свойств).
Техническая термодинамика (т/д) рассматривает закономерности взаимного превращения теплоты в работу. Она устанавливает взаимосвязь между тепловыми, механическими и химическими процессами, которые совершаются в тепловых и холодильных машинах, изучает процессы, происходящие в газах и парах, а также свойства этих тел при различных физических условиях.
Термодинамика базируется на двух основных законах (началах) термодинамики:
I закон термодинамики - закон превращения и сохранения энергии;
II закон термодинамики – устанавливает условия протекания и направленность макроскопических процессов в системах, состоящих из большого количества частиц.
Техническая т/д, применяя основные законы к процессам превращения теплоты в механическую работу и обратно, дает возможность разрабатывать теории тепловых двигателей, исследовать процессы, протекающие в них и т.п.
Объектом исследования является термодинамическая система, которой могут быть группа тел, тело или часть тела. То что находится вне системы называется окружающей средой. Т/д система это совокупность макроскопических тел, обменивающиеся энергией друг с другом и окружающей средой. Например: т/д система – газ, находящейся в цилиндре с поршнем, а окружающая среда – цилиндр, поршень, воздух, стены помещения.
Изолированная система - т/д система не взаимодействующая с окружающей средой.
Адиабатная (теплоизолированная) система – система имеет адиабатную оболочку, которая исключает обмен теплотой (теплообмен) с окружающей средой.
Однородная система – система, имеющая во всех своих частях одинаковый состав и физические свойства.
Гомогенная система – однородная система по составу и физическому строению, внутри которой нет поверхностей раздела (лед, вода, газы).
Гетерогенная система – система, состоящая из нескольких гомогенных частей (фаз) с различными физическими свойствами, отделенных одна от другой видимыми поверхностями раздела (лед и вода, вода и пар).
В тепловых машинах (двигателях) механическая работа совершается с помощью рабочих тел – газ, пар.
Величины, которые характеризуют физическое состояние тела называются термодинамическими параметрами состояния. Такими параметрами являются удельный объем, абсолютное давление, абсолютная температура, внутренняя энергия, энтальпия, энтропия, концентрация, теплоемкость и т.д. При отсутствии внешних силовых полей (гравитационного, электромагнитного и др.) термодинамическое состояние однофазного тела можно однозначно определить 3-мя параметрами – уд. объемом (υ), температурой (Т), давлением (Р).
Удельный объем – величина, определяемая отношением объема вещества к его массе.υ = V / m, [м3/кг], (1.1)Плотность вещества – величина, определяемая отношением массы к объему вещества.ρ = m / V, [кг/м3], (1.2)
υ = 1 / ρ; ρ = 1 / υ; υ • ρ = 1. (1.3)Давление – с точки зрения молекулярно-кинетической теории есть средний результат ударов молекул газа, находящихся в непрерывном хаотическом движении, о стенку сосуда, в котором заключен газ.Р = F / S; [Па] = [Н/м2] (1.4)Внесистемные единицы давления:
1 кгс/м2 = 9,81 Па = 1 мм.водн.ст.
1 ат. (техн.атмосфера) = 1 кгс/см2 = 98,1 кПа.
1 атм. (физическая атмосфера) = 101,325 кПа = 760 мм.рт.ст.
1 ат. = 0,968 атм.
1 мм.рт.ст. = 133,32 Па.
1 бар = 0,1 МПа = 100 кПа = 105 Па.
Различают избыточное и абсолютное давление.
Избыточное давление (Ри)– разность между давлением жидкости или газа и давлением окружающей среды.
Абсолютное давление (Р)– давление отсчитываемое от абсолютного нуля давления или от абсолютного вакуума. Это давление является т/д параметром состояния.
Абсолютное давление определяется:
1). При давлении сосуда больше атмосферного:Р = Ри + Ро; (1.5)2). При давлении сосуда меньше атмосферного:Р = Ро + Рв; (1.6)где Ро – атмосферное давление;
Рв – давление вакуума.
Температура – характеризует степень нагретости тел, представляет собой меру средней кинетической энергии поступательного движения его молекул. Чем больше средняя скорость движения, тем вышетемпература тела.
За т/д параметр состояния системы принимают термодинамическую температуру (Т), т.е. абсолютную температуру. Она всегда положительна, При температуре абсолютного нуля (Т=0) тепловые движения прекращаются и эта температура является началом отсчета абсолютной температуры.
^ Уравнение состояния и термодинамический процесс
Основные т/д параметры состояния Р, υ, Т однородного тела зависят друг от друга и взаимно связаня между собой определенным математическим уравнением, который называется уравнением состояния:f (Р, υ, Т) = 0. (1.7)
Равновесным состоянием называется состояние тела, при котором во всех его точках объема Р, υ и Т и все другие физические свойства одинаковы.
Совокупность изменений состояния т/д системы при переходе из одного состояния в другое называется т/д процессом. Т/д процессы бывают равновесные и неравновесные. Если процес проходит через равновесные состояния, то он называется равновесным. В реальных случаях все процессы являются неравновесными.
Если при любом т/д процессе изменение параметра состояния не зависит от вида процесса, а определяется начальным и конечным состоянием, то параметры состояния называются функцией состояния. Такими параметрами являются внутренняя энергия, энтальпия, энтропия и т.д.
Интенсивные параметры – это параметры не зависящие от массы системы (давление, температура).
Аддитивные (экстенсивные) параметры – параметры, значения которых пропорциональны массе системы (Объем, энергия, энтропия и т.д.).
^ 2.Первый закон термодинамики. Работа, теплота, внутренняя энергия, энтальпия
Теплота и работа
Тела, участвующие при протекании т/д процесса обмениваются энергией. Передача энергии от одного тела к другому происходит двумя способами.
1-й способ реализуется при непосредственном контакте тел, имеющих различную температуру, путем обмена кинетической энергией между молекулами соприкасающихся тел либо лучистым переносом внутренней энергии излучающих тел путем э/м волн. При этом энергия передается от более нагретого к менее нагретому.
Количество энергии, переданной 1-м способом от одного тела к другому, называется количеством теплоты – Q [Дж], а способ – передача энергии в форме теплоты.
2-й способ связан с наличием силовых полей или внешнего давления. Для передачи энергии этим способом тело должно либо передвигаться в силовом поле, либо изменять свой объем под действием внешнего давления, То есть передачи энергии происходит при условии перемещения всего тела или его части в пространстве. При этом количество переданной энергии называется работой – L [Дж], а способ передача энергии в форме работы.
Количество энергии, полученное телом в форме работы называется работой совершенной над телом, а отданную энергию – затраченной телом работой.
Количество теплоты, полученное (отданное) телом и работа, совершенная (затраченная) над телом, зависят от условий перехода тела из начального состояния в конечное, т.е. зависят от характера т/д процесса.
^ Внутренняя энергия
В общем случае внутренней энергией называется совокупность всех видов энергий, заключенной в теле или системе тел. Эту энергию можно представить как сумму отдельных видов энергий: кинетической энергии молекул (поступательного и вращательного движения молекул); колебательного движения атомов в самой молекуле; энергии электронов; внутриядерной энергии; энергии взаимодействия между ядром молекулы и электронами; потенциальной энергии молекул.
В технической термодинамике рассматриваются только такие процессы, в которых изменяются кинетическая и потенциальная составляющие внутренней энергии. При этом знание абсолютных значений внутренней энергии не требуется. Поэтому внутренней энергией для идеальных газов называют кинетическую энергию движения молекул и энергию колебательных движений атомов в молекуле, а для реальных газов дополнительно включают потенциальную энергию молекул.
Внутренняя энергия (U) является функцией двух основных параметров состояния газа, т.е. U = f (P,T), U = f (υ,T) U= f (P,υ). Κаждому состоянию рабочего тела (системы) соответствует вполне определенное значение параметров состояния, то для каждого состояния газа будет характерна своя однозначная, вполне определенная величина внутренней энергии U. То есть U является функцией состояния газа. И разность внутренних энергий для двух каких-либо состояний рабочего тела или системы тел не будет зависит от пути перехода от первого состояния во второе.
^ Первый закон термодинамики
Первый закон термодинамики является основой термодинамической теории и имеет огромное прикладное значение при исследовании термодинамических процессов. Этот закон является законом сохранения и превращения энергии:
¦"Энергия не исчезает и не возникает вновь, она лишь переходит
¦из одного вида в другой в различных физических процессах".
^ Для термодинамических процессов закон устанавливает взаимосвязь между теплотой, работой и изменением внутренней энергии т/д системы:
¦"Теплота, подведенная к системе, расходутся на изменение энергии ¦системы и совершение работы".
^ Уравнение первого закона термодинамики имеет следующий вид: Q = (U2 – U1) + L, (2.1)где Q - количества теплоты подведенная (отведенная) к системе;
L - работа, совершенная системой (над системой);
(U2 – U1) - изменение внутренней энергии в данном процессе.
Если:
Q > 0 – теплота подводится к системе;
Q < 0 – теплота отводится от системы;
L > 0 –работа совершается системой;
L < 0 – работа совершается над системой.
Для единицы массы вещества уравнение первого закона термодинамики имеет вид:q = Q /m = (u2 – u1) + l. (2.2)
В дальнейшем все формулы и уравнения будут даны в основном для единицы массы вещества.
1-й закон т/д указывает, что для получения полезной работы (L) в непрерывно действующем тепловом двигателе надо подводить (затрачивать) теплоту (Q).
Двигатель, постоянно производящий работу и не потребляющий никакой энергии называется вечным двигателем I рода."
Из этого можно высказать следующее определение 1-го закона термодинамики:
" Вечный двигатель первого рода невозможен".
Энтальпия
Рассмотрим полную энергию газа, находящегося под давлением Р, создаваемым грузом массой. В этом случае полная энергия системы состоит из внутренней энергии газа U и потенциальной энергии груза, равной,  где
где 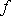 - площадь поперечного сечения поршня. Т. е.
- площадь поперечного сечения поршня. Т. е.  . Величина
. Величина  , зависящая от сил, действующих на поршень, получила название потенциальной энергии давления.
, зависящая от сил, действующих на поршень, получила название потенциальной энергии давления.
Таким образом, если газ находится в среде с давлением P, то с любым состоянием его связана некоторая энергия  , получившая название энтальпии газа в данном состоянии. Выражение энтальпии для 1 кг газа (т. е. удельной энтальпии) имеет вид.
, получившая название энтальпии газа в данном состоянии. Выражение энтальпии для 1 кг газа (т. е. удельной энтальпии) имеет вид. 
Следовательно, удельная энтальпия, будучи зависимой от параметров состояния u,p, и v, также является параметром состояния. Поэтому изменение  , как и изменение
, как и изменение  , не зависит от характера процесса, а определяется только начальным и конечным состояниями, т. е..
, не зависит от характера процесса, а определяется только начальным и конечным состояниями, т. е..

Как однозначная функция состояния удельная энтальпия может быть представлена в виде функции любой пары основных параметров состояния.
Удельная энтальпия идеального газа, как и его удельная внутренняя энергия, является функцией только температуры. Действительно:. 
Удельная энтальпия, как и удельная внутренняя энергия, выражается в джоулях на килограмм (Дж/кг).
^ 3 Вывод 1закона через энтальпию, через энтропию
Энтальпия
Ранее была приведена так называемая интегральная форма записи первого закона (1), согласно которой для произвольного количества вещест 
Для 1 кг вещества: 
Дифференциальная форма записи уравнения первого закона при анализе термодинамических процессов часто оказывается более удобной. Уравнение первого закона термодинамики можно представить в другом виде. К выражению 
прибавим и вычтем слагаемое Vdp: 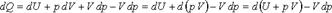 Последнее слагаемое представляет собой элементарную располагаемую работу. Функцию
Последнее слагаемое представляет собой элементарную располагаемую работу. Функцию  измеряемую в Дж, в термодинамике называют энтальпией. Энтальпия, отнесенная к 1 кг
измеряемую в Дж, в термодинамике называют энтальпией. Энтальпия, отнесенная к 1 кг  называется удельной энтальпией. Входящие в выражение (19) величины u, p, υ являются параметрами состояния, поэтому и сама энтальпия также будет параметром (функцией) состояния. Тогда аналитические выражения для первого закона примут вид:
называется удельной энтальпией. Входящие в выражение (19) величины u, p, υ являются параметрами состояния, поэтому и сама энтальпия также будет параметром (функцией) состояния. Тогда аналитические выражения для первого закона примут вид: 

 Записывая последнее выражение для изобарного процесса p=const, получаем:
Записывая последнее выражение для изобарного процесса p=const, получаем:  т.е. изменение энтальпии численно равно количеству теплоты, подводимому к системе в изобарном процессе. Тогда можно записать:
т.е. изменение энтальпии численно равно количеству теплоты, подводимому к системе в изобарном процессе. Тогда можно записать:  В заключение следует отметить, что общее уравнение первого закона термодинамики
В заключение следует отметить, что общее уравнение первого закона термодинамики 
 2017-12-14
2017-12-14 2093
2093
