Первый закон термодинамики (закон сохранения энергии для тепловых процессов) определяет количественное соотношение между изменением внутренней энергии системы дельта U, количеством теплоты Q, подведенным к ней, и суммарной работой внешних сил A, действующих на систему. Изменение внутренней энергии системы при ее переходе из одного состояния в другое равно сумме количества теплоты, подведенного к системе извне, и работы внешних сил, действующих на нее: 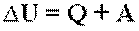 Первый закон термодинамики - количество теплоты, подведенное к системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами:
Первый закон термодинамики - количество теплоты, подведенное к системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами: 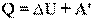 Частные случаи первого закона термодинамики для изопроцессов: При изохорном процессе объем газа остается постоянным, поэтому газ не совершает работу. Изменение внутренней энергии газа происходит благодаря теплообмену с окружающими телами:
Частные случаи первого закона термодинамики для изопроцессов: При изохорном процессе объем газа остается постоянным, поэтому газ не совершает работу. Изменение внутренней энергии газа происходит благодаря теплообмену с окружающими телами: 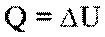 . При изотермическом процессе количество теплоты, переданное газу от нагревателя, полностью расходуется на совершение работы:
. При изотермическом процессе количество теплоты, переданное газу от нагревателя, полностью расходуется на совершение работы: 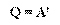 . При изобарном расширении газа подведенное к нему количество теплоты расходуется как на увеличение его внутренней энергии и на совершение работы газом:
. При изобарном расширении газа подведенное к нему количество теплоты расходуется как на увеличение его внутренней энергии и на совершение работы газом: 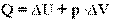 . Адиабатный процесс - термодинамический процесс в теплоизолированной системе.
. Адиабатный процесс - термодинамический процесс в теплоизолированной системе. 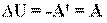 Теплоизолированная система - система, не обменивающаяся энергией с окружающими телами. Внутренняя энергия термодинамическая функция состояния системы, ее энергия, определяемая внутренним состоянием. Внутренняя энергия складывается в основном из кинетической энергии движения частиц (атомов, молекул, ионов, электронов) и энергии взаимодействия между ними (внутри- и межмолекулярной). На внутреннюю энергию влияет изменение внутреннего состояния системы под действием внешнего поля; во внутреннюю энергию входит, в частности, энергия, связанная с поляризацией диэлектрика во внешнем электрическом поле и намагничиванием парамагнетика во внешнем магнитном поле. Кинетическая энергия системы как целого и потенциальная энергия, обусловленная пространственным расположением системы, во внутреннюю энергию не включаются. В термодинамике определяется лишь изменение внутренней энергии в различных процессах. Поэтому внутреннюю энергию задают с точностью до некоторого постоянного слагаемого, зависящего от энергии, принятой за нуль отсчета. Внутренняя энергия U как функция состояния вводится первым началом термодинамики, согласно которому разность между теплотой Q, переданной системе, и работой W, совершаемой системой, зависит только от начального и конечного состояний системы и не зависит от пути перехода, т.е. представляет изменение фуникции состояния Δ U
Теплоизолированная система - система, не обменивающаяся энергией с окружающими телами. Внутренняя энергия термодинамическая функция состояния системы, ее энергия, определяемая внутренним состоянием. Внутренняя энергия складывается в основном из кинетической энергии движения частиц (атомов, молекул, ионов, электронов) и энергии взаимодействия между ними (внутри- и межмолекулярной). На внутреннюю энергию влияет изменение внутреннего состояния системы под действием внешнего поля; во внутреннюю энергию входит, в частности, энергия, связанная с поляризацией диэлектрика во внешнем электрическом поле и намагничиванием парамагнетика во внешнем магнитном поле. Кинетическая энергия системы как целого и потенциальная энергия, обусловленная пространственным расположением системы, во внутреннюю энергию не включаются. В термодинамике определяется лишь изменение внутренней энергии в различных процессах. Поэтому внутреннюю энергию задают с точностью до некоторого постоянного слагаемого, зависящего от энергии, принятой за нуль отсчета. Внутренняя энергия U как функция состояния вводится первым началом термодинамики, согласно которому разность между теплотой Q, переданной системе, и работой W, совершаемой системой, зависит только от начального и конечного состояний системы и не зависит от пути перехода, т.е. представляет изменение фуникции состояния Δ U 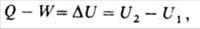 где U1 и U2 - внутренняя энергия системы в начальном и конечном состояниях соответственно. Уравнение (1) выражает закон сохранения энергии в применении к термодинамическим процессам, т.е. процессам, в которых происходит передача теплоты. Для циклического процесса, возвращающего систему в начальное состояние, Δ U =0. В изохорных процессах, т.е. процессах при постоянном объеме, система не совершает работы за счет расширения, W =0 и теплота, переданная системе, равна приращению внутренней энергии: Qv =Δ U. Для адиабатических процессов, когда Q =0, Δ U =- W. Внутренняя энергия системы как функция ее энтропии S, объема V и числа молей mi i-того компонента представляет собой термодинамический потенциал. Это является следствием первого и второго начал термодинамики и выражается соотношением:
где U1 и U2 - внутренняя энергия системы в начальном и конечном состояниях соответственно. Уравнение (1) выражает закон сохранения энергии в применении к термодинамическим процессам, т.е. процессам, в которых происходит передача теплоты. Для циклического процесса, возвращающего систему в начальное состояние, Δ U =0. В изохорных процессах, т.е. процессах при постоянном объеме, система не совершает работы за счет расширения, W =0 и теплота, переданная системе, равна приращению внутренней энергии: Qv =Δ U. Для адиабатических процессов, когда Q =0, Δ U =- W. Внутренняя энергия системы как функция ее энтропии S, объема V и числа молей mi i-того компонента представляет собой термодинамический потенциал. Это является следствием первого и второго начал термодинамики и выражается соотношением: 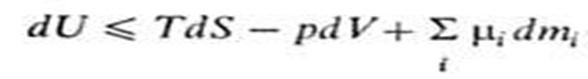 где Т - абсолютная температура, р - давление, μi - химический потенциал i-того компонента. Знак равенства относится к равновесным процессам, знак неравенства - к неравновесным. Для системы с заданными значениями S, V, mi (закрытая система в жесткой адиабатной оболочке) внутренняя энергия при равновесии минимальна. Убыль внутренней энергии в обратимых процессах при постоянных V и S равна максимальной полезной работе (см. Максимальная работа реакции). Зависимость внутренней энергии равновесной системы от температуры и объема U=f(T, V) называется калорическим уравнением состояния. Производная внутренней энергии по температуре при постоянном объеме равна изохорной теплоемкости.
где Т - абсолютная температура, р - давление, μi - химический потенциал i-того компонента. Знак равенства относится к равновесным процессам, знак неравенства - к неравновесным. Для системы с заданными значениями S, V, mi (закрытая система в жесткой адиабатной оболочке) внутренняя энергия при равновесии минимальна. Убыль внутренней энергии в обратимых процессах при постоянных V и S равна максимальной полезной работе (см. Максимальная работа реакции). Зависимость внутренней энергии равновесной системы от температуры и объема U=f(T, V) называется калорическим уравнением состояния. Производная внутренней энергии по температуре при постоянном объеме равна изохорной теплоемкости. 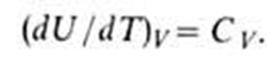 Для рассмотрения конкретных процессов найдем в общем виде внешнюю работу, совершаемую газом при изменении его объема. Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние d l, то производит над ним работу
Для рассмотрения конкретных процессов найдем в общем виде внешнюю работу, совершаемую газом при изменении его объема. Если газ, расширяясь, передвигает поршень на бесконечно малое расстояние d l, то производит над ним работу 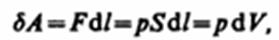 где S — площадь поршня, S d l=dV— изменение объема системы. Таким образом,
где S — площадь поршня, S d l=dV— изменение объема системы. Таким образом, 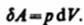 Полную работу А, совершаемую газом при изменении его объема от V 1 до V 2, найдем интегрированием формулы:
Полную работу А, совершаемую газом при изменении его объема от V 1 до V 2, найдем интегрированием формулы: 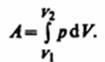 Результат интегрирования определяется характером зависимости между давлением и объемом газа. Найденное для работы выражение справедливо при любых изменениях объема твердых, жидких и газообразных тел.
Результат интегрирования определяется характером зависимости между давлением и объемом газа. Найденное для работы выражение справедливо при любых изменениях объема твердых, жидких и газообразных тел.
Первый закон термодинамики. Внутренняя энергия системы. Работа, совершаемая газом
|
|

Сейчас читают про:
 2018-01-08
2018-01-08 1018
1018







