Основное уравнение МКТ позволяет вычислить давление газа, если известны масса молекулы, среднее значение квадрата скорости и концентрация молекул.
Давление идеального газа заключается в том, что молекулы при столкновениях со стенками сосуда взаимодействуют с ними по законам механики как упругие тела.
Во время столкновения, согласно третьему закону Ньютона, молекула действует на стенку с силой F2, равной по модулю силе F1 и направленной противоположно.
Молекул много, и каждая передает стенке при столкновении такой же импульс. Учитывая, что не все молекулы имеют одинаковую скорость, сила, действующая на стенку будет пропорциональна среднему квадрату скорости. Так как молекулы движутся во всех направлениях, средние значения квадратов проекций скорости равны. Следовательно, средний квадрат проекции скорости:  ;
;  . Тогда давление газа на стенку сосуда равно:
. Тогда давление газа на стенку сосуда равно:  - основное уравнение МКТ. Обозначив среднее значение кинетической энергии поступательного движения молекул идеального газа:
- основное уравнение МКТ. Обозначив среднее значение кинетической энергии поступательного движения молекул идеального газа:  , получим
, получим 
|
|
|
Основное уравнение МКТ для идеального газа устанавливает связь легко измеряемого макроскопического параметра – давления – с такими микроскопическими параметрами газа, как средняя кинетическая энергия и концентрация молекул. Но, измерив только давление, мы не можем узнать ни среднее значение кинетической энергии молекул в отдельности, ни их концентрацию. Следовательно, для нахождения микроскопических параметров газа нужны измерения еще какой-то физической величины, связанной со средней кинетической энергией молекул. Такой величиной является температура.Любое макроскопическое тело или группа макроскопических тел при неизменных внешних условиях самопроизвольно переходит в состояние теплового равновесия. Тепловое равновесие – это такое состояние, при котором все макроскопические параметры сколь угодно долго остаются неизменными. Температура характеризует состояние теплового равновесия системы тел: все тела системы, находящиеся друг с другом в тепловом равновесии, имеют одну и ту же температуру. Для измерения температуры можно воспользоваться изменением любой макроскопической величины в зависимости от температуры: объема, давления, электрического сопротивления и т.д. В отличие от жидкостей все разреженные газы расширяются при нагревании одинаково и одинаково меняют свое давление при изменении температуры. Поэтому в физике для установления рациональной температурной шкалы используют изменение давления определенного количества разреженного газа при постоянном объеме или изменение объема газа при постоянном давлении. Такую шкалу иногда называют идеальной газовой шкалой температур.
|
|
|
При тепловом равновесии средняя кинетическая энергия поступательного движения молекул всех газов одинакова. Давление прямо пропорционально средней кинетической энергии поступательного движения молекул: 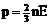 . При тепловом равновесии, если давление газа данной массы и его объем фиксированы, средняя кинетическая энергия молекул газа должна иметь строго определенное значение, как и температура. Т.к.
. При тепловом равновесии, если давление газа данной массы и его объем фиксированы, средняя кинетическая энергия молекул газа должна иметь строго определенное значение, как и температура. Т.к. 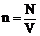 , то
, то 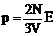 , или
, или  .Обозначим
.Обозначим  . Величина
. Величина  растет с повышением температуры и ни от чего, кроме температуры не зависит. Следовательно, ее можно считать естественной мерой температуры. Будем считать величину
растет с повышением температуры и ни от чего, кроме температуры не зависит. Следовательно, ее можно считать естественной мерой температуры. Будем считать величину  , измеряемую в энергетических единицах, прямо пропорциональной температуре
, измеряемую в энергетических единицах, прямо пропорциональной температуре  , выражаемой в градусах:
, выражаемой в градусах:  , где
, где  - коэффициент пропорциональности. Коэффициент
- коэффициент пропорциональности. Коэффициент  , в честь австрийского физика Л. Больцмана называется постоянной Больцмана. Следовательно,
, в честь австрийского физика Л. Больцмана называется постоянной Больцмана. Следовательно,  . Температура, определяемая этой формулой, не может быть отрицательной. Следовательно, наименьшим возможным значением температуры является 0, если давление или объем равны нулю. Предельную температуру, при которой давление идеального газа обращается в нуль при фиксированном объеме или объем идеального газа стремится к нулю при неизменном давлении, называют абсолютным нулем температуры. Английский ученый У. Кельвин ввел абсолютную шкалу температур. Нулевая температура по шкале Кельвина соответствует абсолютному нулю, а каждая единица температуры по этой шкале равна градусу по шкале Цельсия. Единица абсолютной температуры в СИ называется Кельвином.
. Температура, определяемая этой формулой, не может быть отрицательной. Следовательно, наименьшим возможным значением температуры является 0, если давление или объем равны нулю. Предельную температуру, при которой давление идеального газа обращается в нуль при фиксированном объеме или объем идеального газа стремится к нулю при неизменном давлении, называют абсолютным нулем температуры. Английский ученый У. Кельвин ввел абсолютную шкалу температур. Нулевая температура по шкале Кельвина соответствует абсолютному нулю, а каждая единица температуры по этой шкале равна градусу по шкале Цельсия. Единица абсолютной температуры в СИ называется Кельвином.  . Следовательно, абсолютная температура есть мера средней кинетической энергии движения молекул.
. Следовательно, абсолютная температура есть мера средней кинетической энергии движения молекул. 

Распределение молекул газа по скоростям (распределение Максвелла). Смысл функции распределения Наиболее вероятная, средняя арифметическая и средняя квадратическая скорость молекул. Зависимость функции распределения от температуры.
Зная абсолютную температуру, можно найти среднюю кинетическую энергию молекул газа, а, следовательно, и средний квадрат их скорости.

Квадратный корень из этой величины называется средней квадратичной скоростью: 
Опыты по определению скоростей молекул доказали справедливость этой формулы. Одни из опытов был предложен О. Штерном в 1920 году.
 2018-01-08
2018-01-08 1784
1784
