энергия электрона может принимать только следующие дозволенные дискретные значения: 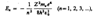 где знак минус означает, что электрон находится в связанном состоянии.
где знак минус означает, что электрон находится в связанном состоянии.
энергетические состояния атома образуют последовательность энергетических уровней, изменяющихся в зависимости от значения n. Целое число n в выражении определяющее энергетические уровни атома, называется главным квантовым числом. Энергетическое состояние с n =1 является основным (нормальным) состоянием; состояния с n > 1 являются возбужденными. Энергетический уровень, соответствующий основному состоянию атома, называется основным (нормальным) уровнем; все остальные уровни являются возбужденными. Энергия атома водорода с увеличением n возрастает и энергетические уровни сближаются к границе, соответствующей значению n = ¥. Атом водорода обладает, таким образом, минимальной энергией (E 1 = –13,55 эВ) при n = 1 и максимальной (Е ¥ = 0) при n = ¥. Следовательно, значение Е ¥ = 0 соответствует ионизации атома (отрыву от него электрона). Согласно второму постулату Бора при переходе атома водорода (Z= 1) из стационарного состояния л в стационарное состояние т с меньшей энергией испускается квант 

 2018-01-08
2018-01-08 1779
1779
