Стереоизомерия. Молекулы моносахаридов содержат несколько центров хиральности, что служит причиной существования большого числа стереоизомеров, соответствующих одной и той же структурной формуле. Например, в альдогексозе имеются четыре хиральных атома углерода НОСН2-(СНОН)4-СНО и ей соответствуют 16 стереоизомеров, т. е. 8 пар энантиомеров. Кетогексозы НОСН2-(СНОН)З-С(О)-СН2ОН содержат по сравнению с соответствующими альдозами на один хиральный атом углерода меньше, поэтому число стереоизомеров уменьшается до 8 (4 пары энантиомеров). Открытые (незамкнутые) формы моносахаридов изображают в виде проекционных формул Фишера. Углеродная цель в них записывается вертикально. У альдоз наверху помещают альдегидную группу, у кетоз — соседнюю с карбонильной первичноспиртовую группу, с этих групп начинают нумерацию цепи. Диастереомеры моносахаридов, различающиеся конфигурацией только одного асимметрического атома углерода, называются эпимерами. Эпимеры — частный случай диастереомеров. Например, D-глюкоза и D-галактоза отличаются друг от друга только конфигурацией С-4, т. е. являются эпимерами по С-4. Аналогично D-глюкоза и D-манноза — эпимеры по С-2. 
|
|
|

Относительная конфигурация моносахаридов определяется по конфигурационному стандарту — глицериновому альдегиду. С конфигурацией его хирального центра сравнивается конфигурация наиболее удаленного от карбонильной группы (концевого) асимметрического атома углерода, имеющего наибольший номер. В альдопентозах таким атомом будет С-4, в альдогексозах — С-5, в кетогексозах — С-4 и т. п. При совпадении конфигурации этого атома углерода с конфигурацией D-глицеринового альдегида моносахарид в целом относят к D-ряду И наоборот, при совпадении с конфигурацией L-глицеринового альдегида считают, что моносахарид принадлежит к L-ряду.
Химическая сущность мутаротации состоит в способности моносахаридов (или моносахаридных звеньев в составе олиго- и полисахаридов) к существованию в виде равновесной смеси таутомеров — открытой и циклических форм. Такой вид таутомерии называется цикло-оксо-таутомерией (ранее еще называли кольчатоцепной). В растворах установление равновесия между четырьмя циклическими таутомерами моносахаридов протекает через открытую форму — оксоформу. Взаимопревращение альфа- и бета-аномеров друг в друга через промежуточную оксоформу называется аномеризацией. Таким образом, в растворе D-глюкоза существует в виде пяти таутомеров альфа- и бета-аномеров пиранозных и фуранозных циклических форм и оксоформы.
В результате внутримолекулярного взаимодействия образуются термодинамически более устойчивые пятичленные — фуранозные — и шестичленные — пиранозные — ци 
|
|
|
Методом рентгеноструктурного анализа установлено, что из двух кресловидных конформаций пиранозного цикла в D-глюкопиранозе осуществляется та, в которой все большие по объему заместители, например первичноспиртовая и гидроксильная группы, занимают экваториальные положения. При этом полуацетальная группа у бета-аномера находится в экваториальном, у альфа-аномера — в аксиальном положениях. Таким образом, у бета-аномера все заместители находятся в более выгодном экваториальном положении, в связи с чем он преобладает в смеси таутомеров D-глюкозы.

Возникновение нового хирального центра приводит к появлению 2-х стереоизомеров для каждой из циклической форм - a- и b- аномеров.
Аномеры – это эпимеры, которые различаются по конфигурации аномерного атома углерода.
У a-аномера конфигурация аномерного центра совпадает с конфигурацией концевого хирального атома С, у b-аномера она противоположна.
Циклические формы моносахаридов изображают с помощью формул Хеуорса. Молекулу представляют в виде плоского цикла, перпендикулярного плоскости рисунка. Заместители, находившиеся в формуле Фишера слева, располагают над плоскостью цикла, справа – под плоскостью. Для определения положения группы СН2ОН в формуле Фишера предварительно делают две перестановки.

В кристаллическом состоянии моносахариды находятся в одной из циклических форм. При растворении образуется равновесная смесь линейной и циклических форм. Их относительное содержание определяется термодинамической стабильностью. Циклические, особенно пиранозные формы, энергетически более выгодны для большинства моносахаридов. Например, в растворе D-глюкозы преобладает b-D-глюкопираноза:

Аномеры D-глюкозы:

D- иL-изомеры глюкозы:

Строение наиболее важных представителей пентоз (рибоза, ксилоза, рибулоза), гексоз (глюкоза, галактоза, манноза, фруктоза), дисахаров (2-дезоксирибоза), 2-аминосахаров (глюкозамин, маннозамин, галактозамин).
Пентозы (формула C5Н10O5) — группа моносахаридов, молекулы которых содержат пять атомов углерода, например рибоза, дезоксирибоза. Некоторые пентозы входят в состав ряда биологически важных соединений, например нуклеиновых кислот, нуклеотидов, дыхательных ферментов и др., участвуют в обмене веществ и процессах фотосинтеза.
Рибоза — моносахарид из группы пентоз, бесцветные кристаллы, легко растворимые в воде и имеющие сладкий вкус. Эпимер арабинозы. Открыта в 1905 году. 
Ксилоза — «древесный сахар», моносахарид из группы пентоз с эмпирической формулой C5H10O5, принадлежит к альдозам.

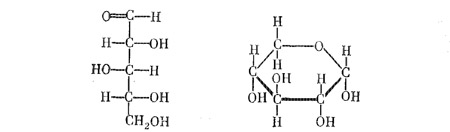
Рибулоза, эритро-пентулоза — моносахарид, относящийся к группе пентоз (кетопентоз).
 D-рибулоза
D-рибулоза
Гексозы, C6H12O6, простые сахара — моносахариды, содержащие 6 атомов углерода; в природе встречаются в свободном виде - в виде глюкозидов входят в состав ди- и полисахаридов,эфиров фосфорной кислоты, гликопротеинов.
Глюко́за (от др.-греч. γλυκύς сладкий) (C6H12O6), или виноградный сахар, или декстроза встречается в соке многих фруктов и ягод, в том числе и винограда, от чего и произошло название этого видасахара. Является шестиатомным сахаром (гексозой). Глюкозное звено входит в состав полисахаридов (целлюлоза, крахмал, гликоген) и ряда дисахаридов (мальтозы, лактозы и сахарозы), к примеру, в пищеварительном тракте быстро расщепляющихся на глюкозу и фруктозу.


Галактоза (galactose) - Шестиуглеродный моносахарид; D-галактоза входит в состав лактозы, некоторых полисахаридов, мукопротеидов и др. соединений.


Манноза — моносахарид с общей формулой C6H12O6 (Изомер глюкозы); компонент многих полисахаридов и смешанных биополимеров растительного, животного и бактериального происхождения.
|
|
|


Фруктоза (арабино-гексулоза, левулёза, фруктовый сахар) — моносахарид, кетогексоза, в живых организмах присутствует исключительно D-изомер, в свободном виде — почти во всех сладких ягодах и плодах— в качестве моносахаридного звена входит в состав сахарозы и лактулозы.


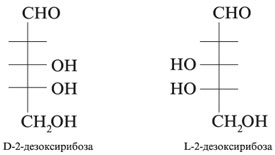

ДЕЗОКСИСАХАРА — моносахариды, в которых одна или несколько гидроксильных групп замещены атомами водорода; в соответствии с этим различают монодезокси-, дидезокси-тридезоксисахара и т. д.
Дезоксисахара редко встречаются в свободном виде и обычно являются компонентами гликозидов, олиго- и полисахаридов.
Важнейший представитель 2-дез-оксисахаров — 2-дезокси-D-рибоза, входящая в состав дезоксирибонуклеиновых кислот (ДНК).
АМИНОСАХАРА (аминодезоксисахара), моносахариды, в молекулах к-рых вместо одной или неск. гидроксильных групп (кроме полуацетальной в альдозах или полукетальной в кетозах) содержатся незамещенные и замещенные аминогруппы. К аминосахарам относят также моносахариды, содержащие иминогруппу вместо атома кислорода в пятичленном (пирролидинозы) или шестичленном (пиперидинозы) углеводных циклах.
Глюкозами́н — вещество, вырабатываемое хрящевой тканью суставов, является компонентом хондроитина и входит в состав синовиальной жидкости.
Галактозамин (син. хондрозамин) — органическое соединение из группы аминосахаров; структурный компонент хондроитинсерной кислоты, входящей в состав соединительной ткани (особенно хрящевой), и ряда других гликопротеинов.



Химические свойства моносахаридов: окисление (образование оновых, ановых, уроновых кислот), восстановление (образование ксилита, сорбита, маннита), реакции этерефикации по спиртовой группе с образованием фосфорных эфиров, реакции изомеризации: превращение глю-6-фосфата во фруктозу-6-фосфат, глюкозу-1-фосфат, рибулозы-5-фосфата в ксилулозу-5-фосфат; образование O-N-гликозидов, условия их гидролиза.
1. Окисление в нейтральной и кислой средах. Окисление альдоз без деструкции (разрушения) углеродного скелета проводят в нейтральной или кислой среде и получают различные кислоты. С помощью сильного окислителя — разбавленной азотной кислоты — концевые группы альдоз (альдегидная и первичноспиртовая) одновременно окисляются в карбоксильные группы, образуя альдаровые кислоты (называемые также сахарными). D-Глюкоза превращается при этом в глюкаровую кислоту.
|
|
|

Получающаяся из галактозы галактаровая (слизевая) кислота трудно растворима в воде, что используется для обнаружения галактозы методом окисления ее азотной кислотой. Мягкими окислителями (бромная вода) можно окислить альдегидную группу в карбоксильную не затрагивая других групп. При этом получаются альдоновые кислоты.

Альдоновые кислоты, являясь гидроксикислотами, выделяются в виде гамма- или дельта-лактонов, При окислении глюкозы бромной водой с высоким выходом получается глюконовая кислота, легко отщепляющая молекулу воды с образованием лактонов. В медицине используется кальциевая соль этой кислоты (глюконат кальция).

При окислении первичноспиртовой группы без затрагивания весьма склонной к окислению альдегидной группы получаются уроновые кислоты, синтез которых представляет собой сложную задачу. Обычно окислению подвергают моносахарид с защищенной альдегидной группой, например в виде гликозида. Уроновые кислоты, как и альдоновые, легко образуют лактоны. Уроновые кислоты при нагревании их солей с металлами (никель, магний) подвергаются декарбоксилированию. При этом из гексуроновых кислот образуются пентозы. В организме за счет ферментативной реакции декарбоксилирования глюкуроновой кислоты получается ксилоза.

2. Восстановление. При восстановлении моносахаридов (их альдегидной или кетонной групп) образуются многоатомные спирты (полиолы) называемые альдитами. Эти кристаллические легко растворимые в воде вещества обладают сладким вкусом и часто используются как заменители сахара при сахарном диабете (ксилит, сорбит).

Восстановление моносахаридов проводят водородом в присутствии металлических катализаторов (палладий, никель). Шестиатомные спирты — глюцит (сорбит), дульцит и маннит — получаются при восстановлении соответственно глюкозы, галактозы и маннозы. Восстановление глюкозы в сорбит является одной из стадий промышленного синтеза аскорбиновой кислоты.
При восстановлении альдоз получается лишь один полиол, кетоз — смесь двух полиолов, например, при восстановлении фруктозы
борогидридом натрия NaВН4 образуются глюцит (сорбит) и маннит.

3. Образование сложных эфиров при взаимодействии с карбоновыми кислотами — реакция этерификации. Например, взаимодействие глюкозы с уксусной кислотой или ее хлорангидридом:

4. ГЛИКОЗИДЫ (от греч. glykys-сладкий и eidos-вид), соед., в к-рых остаток циклич. формы моно- или олигосахарида (гликозильный, или углеводный, остаток) связан с др. орг. остатком (агликоном) через гетероатом; соотв. различают О-, N-, S-гликозиды и др. Связь между гликозильным остатком и агликоном наз. гликозидной. При образовании гликозидов возникает новый асимметрич. гликозидный центр. Его конфигурацию обозначаютили в зависимости от того, совпадает она или нет с конфигурацией того углеродного атома моносахарида, к-рый определяет принадлежность последнего к D- или L-ряду. Напр., в изомерных метил-О-глюкопиранозидах конфигурация отражается ф-лой I, конфигурация-ф-лой II:
Образование N-гликозидов (гликозиламинов)
При обработке пентоз и гексоз аминами, не являющимися сильными основаниями (сильные основания вызывают эпимеризацию), происходит образование соответствующих N-гликозидов. 1.Гликозидные связи в полисахаридах гидролизуются под действием кислот или ферментов.
2. Гликозидные связи устойчивы к действию щелочей, о если олиго - или полисахарид содержит восстанавливающий сахар, происходит деструкция углеводной цепи, начиная с этого восстанавливающего остатка.
3. Гликозидные связи, как правило, устойчивы к действию оснований (см. гл. Такой распад протекает путем разрушения восстанавливающего звена по обычной схеме щелочной деструкции моносахаридов.
4. Гликозидные связи в полисахаридах могут значительно различаться по устойчивости в кислой среде (см. гл. Кроме этого, на выбор условий гидролиза влияет растворимость исходного полисахарида и устойчивость к кислотам освобождающихся при гидролизе моносахаридов.
5. Гликозидные связи в нейтральных полисахаридах различаются по чувствительности к кислотному гидролизу. Аналогичные условия могут быть использованы для полного или частичного гидролиза других гексозанов или пентозанов. Маннаны обычно гидролизуются в течение более длительного времени.
Дисахариды: классификация (редуцирующие- мальтоза, целлобиоза, лактоза) и нередуцирующие (сахароза, трегалоза). Строение, химические свойства: гидролиз, окисление редуцирующих сахаров.
Дисахариды состоят из двух остатков моносахаридов, соединенных между собой О -гликозидной связью. Если один полуацетальный гидроксил остается свободным, а дисахариды проявляют альдегидные свойства, то такие дисахариды называются восстанавливающими. Если же связь между двумя остатками моносахаридов осуществляется посредством обоих полуацетальных гидроксилов, то для таких дисахаридов альдегидные свойства не характерны и они называются невосстанавливающими.
Мальтоза. Этот дисахарид называют еще солодовым сахаром. Он является основным продуктом расщепления крахмала под действием фермента амилазы, выделяемого слюнной железой. Мальтоза имеет в З раза менее сладкий вкус, чем сахароза.
В мальтозе остатки двух молекул D-глюкопиранозы связаны альфа-(1-4)-гликозидной связью. Аномерный атом углерода, участвующий в образовании этой связи, имеет конфигурацию, а аномерный атом с полуацетальной гидроксильной группой может иметь как альфа- (альфа-мальтоза) так и бета-конфигурацию (бета-мальтоза). Молекула глюкозы, поставляющего для связи полуацетальную гидроксильную группу, рассматривается как заместитель при С-4 второй молекулы глюкозы. Вназвании дисахарида первая молекула приобретает суффикс -озил, а у второй сохраняется суффикс -оза. Кроме того, в полном названии указывается конфигурации обоих аномерных атомов углерода. Мальтоза восстанавливает реактив Фелинга.
Целлобиоза. Этот дисахарид получается при неполном гидролизе полисахарида целлюлозы. В целлобиозы остатки двух молекул D-глюкопиранозы связаны бета-(1-4)-гликозидной связью. Отличие целлобиозы от мальтозы состоит в том, что аномерный атом углерода, участвующий в образовании гликозидной связи, имеет бета-конфигурацию. Растворы целлобиозы мутаротируют. Конфигурацинное различие между мальтозой и целлобиозой влечет за собой и конформационное отличие: альфа-гликозидная связь в мальтозе расположена аксиально, а бета-гликозидная связь в целлобиозе — экваториально. Конформационное состояние дисахаридов служит первопричиной линейного строения целлюлозы, в состав которой входит целлобиоза, и клубкообразного строения амилозы (крахмал), построенной из мальтозных единиц.
Лактоза. Содержится в молоке (4—5%) и получается в сыроваренной промышленности из молочной сыворотки после отделения творога (отсюда ее название молочный сахар). Лактоза построена из остатков D-галактопиранозы и D-глюкопиранозы, связанных бета-(1,4)—гликозидной связью. Участвующий в образовании этой связи аномерный атом углерода D-галактопиранозы имеет бета-конфигурацию. Аномерный атом глюкопиранозного фрагмента может иметь как альфа-, так и бета-конфигурацию.
Сахароза C12H22O11, или свекловичный сахар, тростниковый сахар, в быту просто сахар — дисахарид из группы олигосахаридов, состоящий из двух моносахаридов — α-глюкозы и β-фруктозы.
Сахароза является весьма распространённым в природе дисахаридом, она встречается во многих фруктах, плодах и ягодах. Особенно велико содержание сахарозы в сахарной свёкле и сахарном тростнике, которые и используются для промышленного производства пищевого сахара.
Трегалóза или микóза — углевод из группы невосстанавливающих дисахаридов. В природной трегалозе 2 остатка D-глюкозы связаны α-1,1-гликозидной связью.
Дисахариды, как и моносахариды, представляют собой кристаллические вещества, хорошо растворимые в воде, плохо – в спирте и практически нерастворимы в неполярных органических растворителях.
Гидролиз
Гидролиз дисахаридов протекает достаточно легко в связи с тем, что связь между моносахаридными звеньями ацетальная.
Окисление
Как уже отмечалось ранее, для восстанавливающих дисахаридов в качестве окислителей можно использовать реактив Толленса, Фелинга, бром и другие вещества, окисляющие альдегиды.
 2018-01-21
2018-01-21 19026
19026








