С чистым растворителем равно молярной доле растворенного вещества.
Для неэлектролитов: 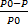 =
= 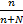
для электролитов и веществ, образующих ассоциаты: 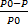 =
= 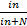
Где Р0- давление пара чистого растворителя,
Р - давление пара растворителя над раствором,
N - число молей растворенного вещества,
N - число молей растворителя,
I-изотонический коэффициент (тот же, что и в уравнении Вант-Гоффа),
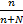 - молярная доля растворенного вещества.
- молярная доля растворенного вещества.
Понижение давления пара растворителя над раствором влияет на
температуру кипения и замерзания раствора. При температуре кипения
давление пара над жидкостью должно быть равно внешнему давлению, а при
температуре замерзания - давлению пара над затвердевшей жидкостью.
Снижение давления пара приводит к необходимости нагревать раствор до более
высокой температуры, чтобы достигнуть давления, при котором закипает
чистая жидкость, и наоборот, охлаждать до более низкой температуры.
Й закон Рауля.
Повышение температуры кипения и понижение температуры
Замерзания раствора по сравнению с чистым растворителем прямо
 2018-01-21
2018-01-21 299
299








