Чистый (элементарный) азот сам по себе не обладает какой-либо биологической ролью. Биологическая роль азота обусловлена его соединениями. Так в составе аминокислот он образует пептиды и белки (наиболее важный компонент всех живых организмов); в составе нуклеотидов образует ДНК и РНК (посредством которых передается вся информация внутри клетки и по наследству); в составе гемоглобина участвует в транспорте кислорода от легких по органам и тканей.
Некоторые гормоны также представляют собой производные аминокислот, а, следовательно, также содержат азот (инсулин, глюкагон, тироксин, адреналин и пр.). Некоторые медиаторы, при помощи которых «общаются» нервные клетки также имеют в своем составе атом азота (ацетилхолин).
Такое соединения как оксид азота (II) и его источники (например, нитроглицерин – лекарственное средство для снижения давления) воздействуют на гладкую мускулатуру кровеносных сосудов, обеспечивая ее расслабление и расширение сосудов в целом (приводит к снижению давления).
Азотистаякислота HNO2 имеет слабый характер. Весьма неустойчива, может быть только в разбавленных растворах:
2HNO2 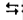 NO+NO2+H2O.
NO+NO2+H2O.
Соли азотистой кислоты называются нитритами или азотистокислыми. Нитриты гораздо более устойчивы, чем HNO2, все они токсичны.
Атом азота в азотистой кислоте имеет промежуточную степень окисления +3 и в связи с этим он может быть и окислителем, и проявлять восстановительные свойства:
2HNO2+ 2HI = I2+ 2NO + 2H2O,
HNO2+ H2O2= HNO3+ H2O,
5KNO2+ 2KMnO4+ 3H2SO4= 5KNO3+ K2SO4+ 2MnSO4+ 3H2O.
Строение азотистой кислоты.
В газовой фазе планарная молекула азотистой кислоты существует в виде двух конфигураций цис- и транс-
При комнатной температуре преобладает транс-изомер: эта структура является более устойчивой. Так, для цис - HNO2 (г) DG°f = −42,59 кДж/моль, а для транс- HNO2 (г) DG = −44,65 кДж/моль.
 2018-01-21
2018-01-21 450
450








