Чистая вода очень плохо проводит электрический ток, но все же обладает измеримой электропроводностью, которая объясняется небольшой диссоциацией воды на ионы водорода и гидроксид-ионы: Н2О↔Н+ +ОН-.
По величине электропроводности чистой воды можно вычислить концентрацию ионов водорода и гидроксид-ионов в воде. При 250С она равна 10-7 моль/л.
Напишем выражение для константы диссоциации воды:
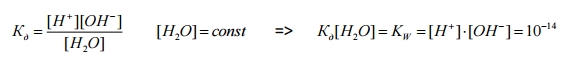
Полученное уравнение показывает, что для воды и разбавленных водных растворов при неизменной температуре произведение концентрации ионов водорода и гидроксид-ионов есть величина постоянная.
Эта величина называется ионным произведением воды.
Выражение степени кислотности и степени щелочности раствора
Растворы, в которых концентрация ионов водорода и гидроксид-ионов одинаковы называются нейтральными растворами. В кислых растворах больше концентрация ионов водорода, в щелочных – концентрация гидроксид-ионов.
Но какова бы не была реакция раствора, произведение концентраций ионов водорода и гидроксид-ионов остается постоянным. Степень кислотности и степень щелочности раствора можно охарактеризовать концентрацией ионов водорода:
Нейтральный раствор [Н + ]=10^-7 моль/л.
Кислый раствор [Н + ]>10^-7 моль/л.
Щелочной раствор [Н + ]<10^-7

 2018-01-21
2018-01-21 998
998








