На рисунке молекула глюкозы представлена в виде «открытой цепи» и в виде циклической структуры. Открытая цепь может быть прямолинейной цепочкой, но углы связей между атомами углерода допускают у пентоз и гексоз образование стабильных циклических структур.
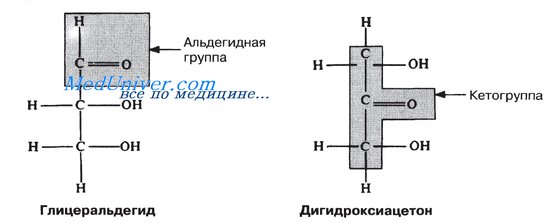
У гексоз типа глюкозы первый атом углерода соединяется с кислородом при пятом углеродном атоме, что приводит к образованию шестичленного кольца. Обратите внимание на то, что атом кислорода включается в кольцо, а шестой углеродный атом оказывается вне кольца. У пентоз первый атом углерода соединяется с кислородом при четвертом углеродном атоме, в результате чего образуется пятичленное кольцо, как показано на рисунке.
Циклические структуры пентоз и гексоз — обычные их формы; в каждый данный момент лишь небольшая часть молекул существует в виде открытой цепи. В состав дисахаридов и полисахаридов также входят циклические формы моносахаридов.
билет 11. Белки́ (протеи́ны, полипепти́ды) — высокомолекулярные органические вещества, состоящие из соединённых в цепочку пептидной связью альфа-аминокислот. В живых организмах аминокислотный состав белков определяется генетическим кодом. Белки растительного происхождения являются замечательным источником белка, поскольку снижают общее потребление насыщенных жиров и холестерина, но лишь при условии их комбинирования, чтобы организм получал полный набор незаменимых аминокислот. Среди популярных в этом отношении продуктов — бобовые, орехи и соя. Помимо этого, растительный протеин также имеется в виде волокон, получаемых из соевой муки. При этом происходит изоляция протеинов, и такой продукт называется структурированным растительным белком (TVP). Он в основном применяется как альтернатива мясу в вегетарианских хот-догах, гамбургерах, «куриных» брикетах и тд. Это низкокалорийный и низкожирный источник растительного белка. Растительные продукты также обеспечивают организм другими полезными веществами, включая фитохимические вещества и клетчатку, которые также имеют большую ценность в рационе.
Существует около 28 аминокислот. В организме человека многие из них синтезируются в печени. Однако некоторые из них не могут быть синтезированы в организме, поэтому человек обязательно должен получать их с пищей. Такие аминокислоты называются незаменимыми и к ним относятся гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, треонин, триптофан и валин. Аминокислоты, которые синтезируются в печени, являются заменимыми и включают аланин, аргинин, аспарагин, аспартовую кислоту, цитруллин, цистеин, гамма-аминомасляную кислоту, глютамовую кислоту, глютамин, глицин, орнитин, пролин, серии, таурин, тирозин.
Процесс синтеза белков постоянно идет в организме. В случае, когда хоть одна незаменимая аминокислота отсутствует, образование белков приостанавливается. Это может привести к самым различным серьезным проблемам — от нарушения пищеварения до депрессии и замедления роста.
Белки являются высокомолекулярными органическими соединениями. Молекулярный вес белков колеблется в больших пределах - от нескольких тысяч до нескольких миллионов. Используя метод ультрацентрифугирования, шведский физик и химик Сведберг получил данные, которые были подтверждены немецким исследователем Бергманом при помощи химического анализа продуктов гидролиза белка, т.е. аминокислот.
Молекулярные веса белков различаются между собой. Наименьшим молекулярным весом обладает рибонуклеаза, а наибольшим - фибриноген крови.Цифры, характеризующие молекулярные веса белков, у различных авторов довольно близки, несмотря на то, что они определяли их различными методами. Кон определял молекулярные веса белков по содержанию серы и железа, Сведберг - методом ультрацентрифугирования, а Бергман - по аминокислотному составу.
Определение молекулярного веса методом криоскопии (по температуре замерзания растворов) и эмбулиоскопии (по температуре кипения) для исследования белков не подходит, так как их растворы не дают резкого снижения температуры, а при нагревании белки разрушаются. Состав белков При образовании белка в результате взаимодействия α-аминогруппы (-NH2) одной аминокислоты с α-карбоксильной группой (-COOH) другой аминокислоты образуются пептидные связи. Концы белка называют C- и N-концом (в зависимости от того, какая из групп концевой аминокислоты свободна: -COOH или -NH2, соответственно). При синтезе белка на рибосоме новые аминокислоты присоединяются к C-концу, поэтому название пептида или белка даётся путём перечисления аминокислотных остатков начиная с N-конца. Химические и физические свойства белков. Белки – амфотерные электролиты. При определенном значении pH среды число положительных и отрицательных зарядов в молекуле белка одинаково. Белки имею разнообразное строение. Есть белки нерастворимые в воде, есть белки легко раство- римые в воде. Есть белки малоактивные в химическом отношении, устойчивые к действию агентов. Есть белки крайне неустойчивые. Есть белки, имеющие вид ни-тей, достигающих в длину сотен нанометров; есть белки, имеющие форму шариков диаметром всего 5–7 нм. Они имеют большую молекулярную массу (104—107).
1.Гидратация.Процесс гидратации означает связывание белками воды, при этом они проявляют гидрофильные свойства: набухают, их масса и объем увеличивается. Набухание бел- ка сопровождается его частичным растворением.
2. Денатурация белков.При денатурации под влиянием внешних факторов (температуры, механического воздействия, действия химических агентов и других факторов) происходит измене- ние вторичной, третичной и четвертичной структур белковой макромолекулы, то есть ее нативной пространственной структуры. Первичная структура, а следователь- но, и химический состав белка не меняются. Изменяются физические свойства: сни- жается растворимость, способность к гидратации, теряется биологическая актив-ность. Меняется форма белковой макромолекулы, происходит агрегирование. В то же время увеличивается активность некоторых групп, облегчается воздействие на белки протеолитических ферментов, а, следовательно, он легче гидролизуется.
3.Пенообразование.Процесс пенообразования–это способность белков образовывать высококонцент- рированные системы «жидкость–газ»,называемые пенами. Устойчивость пены, в ко- торой белок является пенообразователем, зависит не только от его природы и от кон- цнтрации,но и от температуры. Белки в качестве пенообразователей широко исполь- зуются в кондитерской промышленности(пастила, зефир, суфле).Структуру пены имеет хлеб, а это влияет на его вкусовые свойства.
4.Горение.Белки горят с образованием азота, углекислого газа и воды, а также некоторых других веществ. Горение сопровождается характерным запахом жженых перьев.
Билет12.
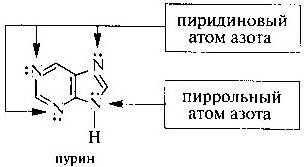
Гетероциклические соединения (гетероциклы) — органические соединения, содержащие циклы, в состав которых наряду с углеродом входят и атомы других элементов. Могут рассматриваться как карбоциклические соединения с гетерозаместителями (гетероатомами) в цикле. Наиболее разнообразны и хорошо изучены ароматические азотсодержащие гетероциклические соединения. Предельные случаи гетероциклических соединений — соединения, не содержащие атомов углерода в цикле, например, пентазол. Гетероциклические ароматические соединения. В ряду этих соединений встречаются оба вида сопряжения. Пи-пи-сопряжение характерно для шестичленных гетероциклов с одним или несколькими гетероатомами. Простейшим их представителем является пиридин, содержащий в цикле один атом азота. Атом азота находится в состоянии sp2-гибридизации (две из трех sp2-гибридных орбиталей образуют сигма-связи). Он поставляет в ароматический секстет один р-электрон. Неподеленная пара электронов на sр2-гибридной орбитали обусловливает свойства пиридина как основания. Атом азота с таким электронным строением принято называть пиридиновым. В результате большей электроотрицательности по сравнению с атомом углерода пиридиновый атом азота понижает электронную плотность на атомах углерода ароматического кольца. Поэтому системы с пиридиновым атомом азота называют пи-недостаточными. Кроме пиридина, примером таких систем служит пиримидин, содержащий два пиридиновых атома азота. р-пи-сопряжение осуществляется в пятичленных гетероциклах с атомами азота, кислорода, серы. Довольно часто в составе биологически значимых соединений встречается гетероцикл с одним атомом азота — пиррол. В пирроле от атома азота в ароматический секстет включается находящаяся на негибридизованной р-орбитали пара электронов, три электрона на sp2-гибридных орбиталях участвуют в образовании трех сигма-связей. Атом азота в таком электронном состоянии получил название пиррольного. Шестиэлектронное облако в пирроле делокализовано на пяти атомах цикла, поэтому пиррол представляет собой пи-избыточную систему. В фуране и тиофене ароматический секстет также включает неподеленную пару электронов негибридизованной р-АО кислорода и серы соответственно, в имидазоле два атома азота вносят разный вклад в образование делокализованного электронного облака: пиррольный атом азота поставляет пару n-электронов, а пиридиновый — один р-электрон. В пиррольном и пиридиновом атомах азота электроны находятся на негибридизованных р-АО. Ароматическим характером обладает также пурин, представляющий собой конденсированную систему из двух гетероциклов — пиримидина и имидазола. Делокализованное электронное облако в пурине включает 10 пи-электронов.

Гемин и хлорофилл. Триптофан вследствие многообразия связанных с ним метаболических реакций и продуктов был одной из первых аминокислот, которые были отнесены к незаменимым. При введении с пищей [14C]-триптофана большая часть изотопа включается в состав белков, однако существенная часть обнаруживается в моче в составе различных катаболитов. Атомы углерода боковой цепи и ароматического кольца могут полностью переходить в амфиболические интермедиаты при трансформации триптофана по кинуренин - антранилат ному пути (Катаболизм аминокислот, образующих ацетил-CoA: метаболическая карта), играющему важную роль в деградации триптофана и в его превращении в никотинамид. У многих животных превращение триптофана в никотиновую кислоту делает необязательным поступление этого витамина с пищей. У крыс, кроликов, собак и свиней пищевой триптофан может полностью заменить этот витамин; у человека, а также у ряда животных избыточное потребление триптофана с пищей повышает экскрецию с мочой производных никотиновой кислоты.
билет 13. Нуклеи́новая кисло́та (от лат. nucleus — ядро) — высокомолекулярное органическое соединение, биополимер (полинуклеотид), образованный остатками нуклеотидов. Нуклеиновые кислоты ДНК и РНК присутствуют в клетках всех живых организмов и выполняют важнейшие функции по хранению, передаче и реализации наследственной информации.
На сегодняшний день в процессе выращивания различных сельскохозяйственных культур активно применяются различные биологически активные вещества. К данной категории веществ можно отнести: фитогормоны, пестициды, фунгициды и удобрения.
К фитогормонам относятся ауксины, гиббереллины, цитокинины. Ауксины активируют рост стеблей, листьев и корней, обеспечивая реакции типа тропизмов, а также стимулируют образование корней у черенков растений. Гиббереллины индуцируют или активируют рост стеблей растений, вызывают прорастание некоторых семян и образование партенокарпических плодов, а также нарушают период покоя у ряда растений. Цитокинины стимулируют клеточное деление (цитокинез), заложение и рост стеблевых почек как у целых растений, так и у недифференцированных каллюсов, а также продлевают жизнь и поддерживают нормальный обмен веществ у изолированных листьев, вызывают их вторичное позеленение. Из природных ингибиторов роста известны кумарин и его производные, абсцизовая кислота и др. Они тормозят рост растений при переходе их в состояние покоя.
К группам синтетических регуляторов относятся также ингибиторы: ретарданты — препараты, уменьшающие длину и увеличивающие толщину стеблей, и морфактины — соединения, вызывающие аномалии в точке роста и появление уродливых органов у растений. К ним примыкают вещества, специфически задерживающие передвижение ИУК и её производных по растению.
К веществам, обладающим резко ингибирующим действием, относятся гербициды, уничтожающие сорную растительность. Синтетические ингибиторы, в отличие от природных, способны более резко подавлять ростовые процессы; они длительный период не поддаются инактивации растительными тканями; характер их действия часто связан не только с ростом, но и с нарушением морфогенетических процессов.
Наиболее распространённый способ обработки растений регуляторами роста — опрыскивание.
Под воздействием ретардантов повышается устойчивость растений к засухе, холоду и загрязнению воздуха. У некоторых культурных растений (яблонь, азалий) они стимулируют зацветание и тормозят вегетативный рост.
Дормины возвращают активно растущие вегетативные почки в состояние покоя, что часто бывает необходимо при резких потеплениях в конце лета и осенью.
Гербициды, которые используются для борьбы с сорной растительностью, давно знакомы овощеводам и садоводам.
Десиканты применяются для предуборочного подсушивания растений.
В процессе выращивания огородных культур активно используются удобрения, инсектициды и фунгициды.
Проведенное нами исследование доказало эффективность регулятора роста гумат натрия «Сахалинский» в выращивании томата.
Используются в количестве, близком к естественному, так как при избытке могут быть получены результаты, обратные ожидаемым и часто негативные.
Применение регуляторов роста преследует многие цели, связанные с задачами защиты растений. Эти вещества малотоксичны для человека, животных, растений и полезной микрофлоры, эффективны, с низкими нормами расхода. Однако ни один из препаратов не является панацеей от всех напастей. Конечно, биорегуляторы повышают устойчивость растений к неблагоприятным внешним воздействиям, но надо помнить, что постоянное выращивание растений в экстремальных для них условиях рано или поздно приведет к их гибели. Так что химические препараты должны использоваться как вспомогательные средства, а не как альтернатива заботливому уходу.
Дезоксирибонуклеи́новая кислота́ (ДНК) — макромолекула, обеспечивающая хранение, передачу из поколения в поколение и реализацию генетической программы развития и функционирования живых организмов. Основная роль ДНК в клетках — долговременное хранение информации о структуре РНК и белков. С химической точки зрения ДНК — это длинная полимерная молекула, состоящая из повторяющихся блоков — нуклеотидов. Каждый нуклеотид состоит из азотистого основания, сахара (дезоксирибозы) и фосфатной группы. Связи между нуклеотидами в цепи образуются за счёт дезоксирибозы и фосфатной группы. В подавляющем большинстве случаев (кроме некоторых вирусов, содержащих одноцепочечную ДНК) макромолекула ДНК состоит из двух цепей, ориентированных азотистыми основаниями друг к другу. Эта двухцепочечная молекула спирализована. В целом структура молекулы ДНК получила название «двойной спирали».В ДНК встречается четыре вида азотистых оснований (аденин, гуанин, тимин и цитозин). Азотистые основания одной из цепей соединены с азотистыми основаниями другой цепи водородными связями согласно принципу комплементарности: аденин соединяется только с тимином, гуанин — только с цитозином
Рибонуклеи́новая кисло́та (РНК) — одна из трёх основных макромолекул (две другие — ДНК и белки), которые содержатся в клетках всех живых организмов.
Так же, как ДНК (дезоксирибонуклеиновая кислота), РНК состоит из длинной цепи, в которой каждое звено называется нуклеотидом. Каждый нуклеотид состоит из азотистого основания, сахара рибозы и фосфатной группы. Последовательность нуклеотидов позволяет РНК кодировать генетическую информацию. Все клеточные организмы используют РНК (мРНК) для программирования синтеза белков.
Клеточные РНК образуются в ходе процесса, называемого транскрипцией, то есть синтеза РНК на матрице ДНК, осуществляемого специальными ферментами — РНК-полимеразами. Затем матричные РНК (мРНК) принимают участие в процессе, называемом трансляцией. Трансляция — это синтез белка на матрице мРНК при участии рибосом. Другие РНК после транскрипции подвергаются химическим модификациям, и после образования вторичной и третичной структур выполняют функции, зависящие от типа РНК.
Нуклеоти́ды — фосфорные эфиры нуклеозидов, нуклеозидфосфаты. Свободные нуклеотиды, в частности АТФ, цАМФ, АДФ, играют важную роль в энергетических и информационных внутриклеточных процессах, а также являются составляющими частями нуклеиновых кислот и многих коферментов. НУКЛЕОЗИДЫ соединения, состоящие из остатков азотистого основания и углевода рибозы (рибонуклеозиды) или дезоксирибозы (дезоксирибонуклеозиды); N-гликозиды пуриновых или пиримидиновых оснований. В молекуле Н. углевод соединён через первый углеродный атом b-гликозидной связью с атомом азота (N-3) пиримидинового основания или атомом азота (N-9) пуринового основания Наибольшее значение в природе имеют Н., входящие в состав нуклеиновых к-т: аденозин, гуанозин, уридин, цитидин и тимидин. В составе транспортных РНК в небольших кол-вах обнаружены редкие Н.— 5-оксиметилцитидин, псевдоуридин, инозин и др. В биосинтезе белка определяют следующие этапы, идущие в разных частях клетки:
Синтез белка.
Первый этап — синтез и-РНК происходит в ядре, в процессе которого информация, содержащаяся в гене ДНК, переписывается на и-РНК. Этот процесс называется транскрипцией (от лат. «транскриптик» — переписывание).
На втором этапе происходит соединение аминокислот с молекулами т-РНК, которые последовательно состоят из трех нуклеотидов — антикодонов, с помощью которых определяется свой триплет-кодон.
Третий этап — это процесс непосредственного синтеза полипептидных связей, называемый трансляцией. Он происходит в рибосомах.
На четвертом этапе происходит образование вторич ной и третичной структуры белка, то есть формирование окончательной структуры белка. Таким образом, в процессе биосинтеза белка образуются новые молекулы белка в соответствии с точной информацией, заложенной в ДНК. Этот процесс обеспечивает обновление белков, процессы обмена веществ, рост и развитие клеток, то есть все процессы жизнедеятельности клетки.
билет14. Однако особенно быстрое развитие Ф. х. как самостоятельной науки началось с 1887 г., когда вант Гоффом и Оствальдом (vant'Hoif, Ostwald) был основан журнал «Zeitschrift fur physikalische Chemie», долгое время являвшийся центральным органом по Ф. х. Почти одновременно В. Оствальд выпустил свой фундаментальный курс «Lehrbuch. der allgemeinen Chemie». (1-й том в 1885 г., 2-й—в 1887), впервые давший полный обзор этой новой науки. В ней же обучались многие русские ученые, к-рые впоследствии пропагандировали Ф. х. в России. В этот период времени направление работ по Ф. х. определялось триумвиратом В. Оствальд, вант Гофф и Ар-реииус (Arrhenius) и сосредоточивалось гл. обр. на разработке вопросов, связанных с теорией растворов вант Гоффа и Аррениуса (см. Осмотическое давление, Диссоциация электролитическая, Растворы). Эти теории позволили установить связь между самыми разнообразными свойствами растворов и тем самым послужили к разъяснению многих процессов как в технике, так и в биологии.
билет15 Энтальпи́я, также тепловая функция и теплосодержание — термодинамический потенциал, характеризующий состояние системы в термодинамическом равновесии при выборе в качестве независимых переменных давления, энтропии и числа частиц.Проще говоря, энтальпия - это та энергия, которая доступна для преобразования в теплоту при определенных температуре и давлении.
Если термомеханическую систему рассматривать как состоящую из макротела (газа) и поршня с грузом весом Р = p S, уравновешивающего давление газа р внутри сосуда, то такая система называется расширенной.
Энтальпия или энергия расширенной системы Е равна сумме внутренней энергии газа U и потенциальной энергии поршня с грузом Eпот = pSx = pV 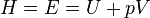
Таким образом, энтальпия в данном состоянии представляет собой сумму внутренней энергии тела и работы, которую необходимо затратить, чтобы тело объёмом V ввести в окружающую среду, имеющую давление р и находящуюся с телом в равновесном состоянии. Энтальпия системы H — аналогично внутренней энергии и другим термодинамическим потенциалам — имеет вполне определенное значение для каждого состояния, т. е. является функцией состояния. Следовательно, в процессе изменения состояния 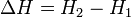
Изменение энтальпии (или Тепловой эффект химической реакции) не зависит от пути процесса, определяясь только начальным и конечным состоянием системы. Если система каким-либо путём возвращается в исходное состояние (круговой процесс), то изменение любого её параметра, являющегося функцией состояния, равно нулю, отсюда 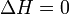 или же
или же 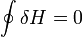
Катаболи́зм ( от греч. καταβολή, «основание, основа») или энергетический обмен — процесс метаболического распада, разложения на более простые вещества (дифференциация) или окисления какого-либо вещества, обычно протекающий с высвобождением энергии в виде тепла и в виде АТФ. Катаболические реакции лежат в основе диссимиляции: утраты сложными веществами своей специфичности для данного организма в результате распада до более простых.
Примерами катаболизма являются превращение этанола через стадии ацетальдегида (этаналя) и уксусной кислоты (этановой кислоты) в углекислый газ и воду, или процесс гликолиза — превращение глюкозы в молочную кислоту либо пировиноградную кислоту и далее уже в дыхательном цикле — опять-таки в углекислый газ и воду. Катаболизм является противоположностью анаболизма — процессу синтеза или ресинтеза новых, более сложных, соединений из более простых, протекающему с расходованием, затратой энергии АТФ. Соотношение катаболических и анаболических процессов в клетке опять-таки регулируется гормонами. Например, адреналин или глюкокортикоиды сдвигают баланс обмена веществ в клетке в сторону преобладания катаболизма, а инсулин, соматотропин, тестостерон — в сторону преобладания анаболизма. Свободная энергия Гиббса (или просто энергия Гиббса, или потенциал Гиббса, или термодинамический потенциал в узком смысле) — это величина, показывающая изменение энергии в ходе химической реакции и дающая таким образом ответ на вопрос о принципиальной возможности протекания химической реакции; это термодинамический потенциал следующего вида: 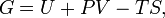
Энергию Гиббса можно понимать как полную химическую энергию системы (кристалла, жидкости и т. д.)
Понятие энергии Гиббса широко используется в термодинамике и химии.
Самопроизвольное протекание изобарно-изотермического процесса определяется двумя факторами: энтальпийным, связанным с уменьшением энтальпии системы (ΔH), и энтропийным T ΔS, обусловленным увеличением беспорядка в системе вследствие роста ее энтропии. Разность этих термодинамических факторов является функцией состояния системы, называемой изобарно-изотермическим потенциалом или свободной энергией Гиббса (G, кДж)
 2018-01-21
2018-01-21 702
702








