Кремниевые кислоты — очень слабые, малорастворимые в воде кислоты общей формулы nSiO2•mH2O. Кремниевые кислоты являются слабыми. Они растворяются в растворах и расплавах щелочей, образуя силикаты:

Растворы кремниевых кислот получают растворением аморфного диоксида кремния в воде, действием сильных кислот на растворимые силикаты натрия или калия:
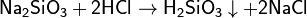
гидролизом хлорсиланов:
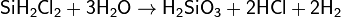
а также методами электродиализа и ионного обмена.
Гидрозоли кремниевых кислот используются как наполнители и связующие материалы в производстве керамических изделий, различных покрытий.
Силикаге́ль представляет собой высушенный гель, образующийся из перенасыщенных растворов кремниевых кислот (n SiO2· m H2O) при pH > 5—6. Твёрдый гидрофильный сорбент.
Получается при подкислении растворов силикатов щелочных металлов с последующей промывкой и высушиванием образовавшегося геля.
Основное применение силикагели находят при осушке воздуха, углекислого газа, водорода, кислорода, азота, хлора и других промышленных газов.
|
|
|
Силикаты и алюмосиликаты представляют собой обширную группу минералов.
Силикаты — важные неметаллические полезные ископаемые: асбест, тальк, слюды.
Их структура образована ионами, то есть силикаты обладают ионными кристаллическими решетками.
1. В основе структур силикатов лежит кремнекислородный тетраэдр [SiO4].
2. Кремнекислородные тетраэдры соединяются друг с другом вершинами через кислород, образуя силоксановую связь Si – O – Si.
3. Для силикатных структур характерным является замещение катиона кремния на катион алюминия. При координационном числе 4 алюминий может замещать кремний в кремнекислородном мотиве, алюминий с координационным числом 6 играет роль связующего катиона между мотивами. В первом случае силикаты получили название алюмосиликатов, во втором – силикатов алюминия.
Ситаллы — стеклокристаллические материалы, полученные объёмной кристаллизацией стекол, и состоящие из одной или нескольких кристаллических фаз, равномерно распределённых в стекловидной фазе.
Ситаллы обладают малой плотностью, высокой механической прочностью, особенно на сжатие, твердостью, жаропрочностью, термической стойкостью, химической устойчивостью и технологичность.
Существуют литиевые, борно-бариевые, магниевые, титановые и другие ситаллы.
Ситаллы применяются для изготовления деталей, требующих прочности и термостойкости (корпуса приборов, шкалы, образцовые меры, подложкимикросхем и др.).
Цеолиты — большая группа близких по составу и свойствам минералов — натролит, шабазит, гейландит, стильбит (десмин),морденит, томсонит, ломонтит.
|
|
|
Кристаллическая структура цеолитов природных и искусственных образована тетраэдрическими группами SiO2/4 и AlO2/4. Открытая каркасно-полостная структура цеолитов [AlSi]O4− имеет отрицательный заряд.
Искусственно синтезированные цеолиты (пермутиты) находят широкое применение в водоочистительных приборах в качестве адсорбентов, ионообменников, молекулярных сит; применяют в качестве доноров и акцепторов электронов.
 2018-01-21
2018-01-21 1283
1283








