Силаны — соединения кремния с водородом общей формулы SinH2n+2.
Способ получения — разложение кислотами силицидов металлов. Например, силицида магния:

Моносилан SiH4 и дисилан Si2Н6 являются бесцветными газами с неприятным запахом, трисилан Si3Н8 — бесцветная, ядовитая, летучая жидкость. Высшие члены гомологического ряда — твёрдые вещества. Силаны растворяются в этаноле, бензине, органосиланах. Силаны воспламеняются на воздухе, Si2Н6 взрывается при контакте с воздухом. Наиболее термически устойчивым является моносилан.
Силаны чрезвычайно легко окисляются, продуктом окисления является либо SiO2, либо промежуточные вещества:

Силаны являются хорошими восстановителями. Силаны устойчивы в нейтральной и кислой средах, но легко гидролизуются даже в присутствии малейших следов ОН—ионов.
С галогенами силаны реагируют со взрывом, при низких температурах образуются галогениды кремния.
Силици́ды — соединения кремния с менее электроотрицательными элементами.
Силициды щелочных металлов бурно, со взрывом, реагируют с водой с выделением силанов, легко окисляются кислородом воздуха. Силициды щелочноземельных металлов также разлагаются водой, растворами кислот и щелочей.
|
|
|
Силициды переходных металлов тугоплавки и стойки к окислению ввиду образования оксидных (металла или кремния) плёнок.
Силициды получают прямым синтезом при спекании металла с кремнием или реакцией кремния с расплавом металла.
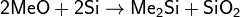
Взаимодействием кремния с гидридами металлов
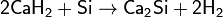
Взаимодействием избытка металла на оксид кремния(IV)
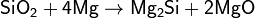
Используется силицид ванадия V3Si как сверхпроводник, силицид рения ReSi как полупроводник. Многие силициды входят в состав жаростойких материалов.
Кремния галогениды, соединения кремния с галогенами. Известны кремния галогениды следующих типов (Х-галоген): SiX4, SiHnX4-n (галогенсиланы), SinX2n+2 и смешанные галогениды, например SiClBr3. При обычных условиях SiF4 - газ, SiCl4 и SiBr4 - жидкости (tпл - 68,8 и 5°С), SiI4 - твёрдое тело (tnл 124°С). Соединения SiX4 легко подвергаются гидролизу:
SiX4 +2H2O=SiO2 +4HX;
на воздухе дымят вследствие образования очень мелких частиц SiO2; тетрафторид кремния реагирует иначе:
SiF4 +2H2O=SiO2 +2H2SiF6
Хлорсиланы (SiHnX4-n), например SiHCl3 (получается действием газообразного HCl на Si), при действии воды образуют полимерные соединения с прочной силоксановой цепью Si-O-Si. Хлорсиланы служат исходными веществами для получения кремнийорганических соединений. Соединения типа SinX2n+2, содержащие цепи атомов Si, при Х - хлор, дают ряд, включая Si6Cl14 (tnл 320°С); остальные галогены образуют только Si2X6.
Тетрахлорид кремния SiCl4 используется при производстве смазочных масел, электроизоляций, теплоносителей, гидрофобизирующих жидкостей и т. д. кремний силикат кварц кристалл.
 2018-01-21
2018-01-21 5029
5029








