Бромноватистая кислота HBrO — представляет собой слабую кислоту; образует соли — гипобромиты. Получается при реакции брома с водой под действием света:
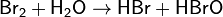
Неустойчивая кислота. Известна только в водном растворе с концентрацией не выше 30 %. При стоянии разлагается. Сильный окислитель.
Иодноватая кислота HIO3 — бесцветное кристаллическое вещество, со стеклянным блеском и горьковато-кислым вкусом, устойчивое при обычной температуре. Легко образуется в кристаллическом состоянии в виде двух различных, не переходящих друг в друга форм ромбической сингонии.
Иодноватая кислота хорошо растворима в воде, в концентрированных растворах проявляется её склонность к полимеризации и устанавливается равновесие.
При медленном нагревании она частично плавится при 110оС, частично образует ангидроиодноватую кислоту HI3O8.
При нагревании HIO3 до 230 °C образуется порошок иодноватого ангидрида, обладающего сильными окислительными свойствами, – I2O5, который растворяется в воде, вновь образуя иодноватую кислоту:
|
|
|

Иодноватая кислота — сильная одноосновная кислота, обладает окислительными свойствами.
Соли иодноватой кислоты называют иодатами.
Получают в водных растворах при окислении иода хлором, пероксидом водорода либо дымящей азотной кислотой.
Иодных кислот известно несколько: ортоиодная H5IO6, метаиодная HIO4. Все кислоты образуют бесцветные кристаллы, хорошо растворимые в воде. Их водные растворы на воздухе желтеют и сильно пахнут озоном. В водном растворе HIO4 быстро превращаются в H5IO6, которая является слабой кислотой и может проявлять окислительные свойства.
Соли всех кислородных кислот галогенов, кроме HIO, более устойчивы, чем соответствующие кислоты, и представляют собой бесцветные кристаллические вещества.
 2018-01-21
2018-01-21 1445
1445








