Количество теплоты, которое выделяется или поглощается при протекании химической реакции, называется тепловым эффектом реакции.
Энтальпия Н -это свойство вещества, являющееся мерой энергии, накапливаемой веществом при его образовании. Часто энтальпию вещества называют его теплосодержанием. Размерность энтальпии - [кДж/моль}
Тепловой эффект химической реакции обозначается символами Q или Δ H, причем их значения равны по величине, но противоположны по знаку:
+ Q = –Δ H.
Реакции, протекающие с выделением теплоты в окружающую среду, называются экзотермическими.
Они характеризуются положительным тепловым эффектом (Q> >0), и соответственно уменьшением энтальпии (теплосодержания) системы (ΔH<0).
Реакции, протекающие с поглощением теплоты из окружающей среды, т.е. с отрицательным тепловым эффектом (Q<0), и приводящие к росту энтальпии (теплосодержания системы) ( Δ H>0), называются эндотермическими .
Термохимические уравнения подчиняются закону Лавуазье-Лапласа:
тепловой эффект прямой реакции равен по абсолютной величине, но противоположен по знаку тепловому эффекту обратной реакции.
.
Энтропия – это мера неупорядоченности состояния системы; Энтропия возрастает (∆Ѕ>0) с увеличением движения частиц при нагревании, испарении, плавлении, расширении газа, при ослаблении или разрыве связей между атомами и т.п.
Изменение энтропии системы в результате протекания химической реакции (∆S) (энтропия реакции) равно сумме энтропий продуктов реакции за вычетом суммы энтропий исходных веществ с учетом стехиометрических коэффициентов. Изменение энтропии в результате протекания химической реакции
aA + bB = сС + dD:
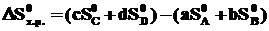 .
.
Энергия Гиббса.
Направление протекания химической реакции определяет энергия Гиббса (∆G). Еще энергию Гиббса называют изобарно- изотермическим потенциалом. Размерность энергии Гиббса кДж/моль.
aA + bB = сС + dD
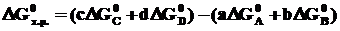 ,
,
где ∆G0 – стандартная энергия Гиббса образования вещества, кДж/моль.
 2018-01-21
2018-01-21 706
706








