не реагирует с водой, разбавленной соляной,серной уксусной,но реагирует с H2SO4 в избыткеO2:

C конц серной кислотой: 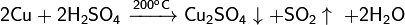
с конц азотной кислотой: 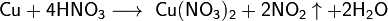
С разбавл азотной кислотой: 
CuCl2+ Cu = CuCl, CuCl2+2NaOH=Cu(OH)2(синеголубой гелеобразный осадок)+2NaCl.. CuCl2+HOH=CuOHCl+HCl
Cu(OH)2 слабое основание
Cu(OH)2 → (t°) CuO + H2O
Cu(OH)2+ускусный альдегид=(t) Cu2O+CH3COOH+H2O
Является амфотерным гидроксидом.
Cu(OH)2 + H2SO4 → CuSO4 + 2H2O
Cu(OH)2 + 2NaOH = Na2[Cu(OH)4]
Применяется для определения количества глюкозы в крови(глюкоза окисляется в глюконовую кислоту) (C 6 H 12 O 6 + Cu(OH)2=(NaOH)C5H11COOH +Cu2O+H2O
Cu легко образует комплексные соединения с орг и неорг веществами:
Cu(OH)2+4NH3=[Cu(NH3)4](OH)2 –реактив Швейдцера(ярко сине-фиолетовый)-может растворять вату,бумагу.целлюлозу
Cu(OH)2+2СH2-OH =(NaOH)CH2-O-Cu-O-CH2 +H2O(ГЛИКОЛАТ МЕДИ)
| | | | |
CH2-OH CH2-OH HO-CH2
С глюкозой образует сине-фиол.раствор т.к возникает глюконат меди:
OH OH
| |
Cu(OH)2+2СH2-СH-СH-СH-СH-С=O =(NaOH) Cu(OH)2+2СH2-СH-СH-СH-СH-С=O+H2O
| | | | | | | | | |
OH OH OH OH H OH O OH OH H
\ /
Cu (глюконат меди)
/ \
OH O OH OH H
| | | | |
2СH2-СH-СH-СH-СH-С=O
|
OH
Cu(OH)2 дает качеств цветную реакцию на белок (Биуретова реакция):белок+ Cu(OH)2 =кобразуется комплексное соединение (сине-фиолет)
Свойства солей 2х валентной меди
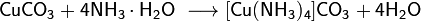
Медь может образовать компл анион 
CuCl2+2NaCN=Cu(CN)2(белый осадок)+2NaCl
Сульфат меди –кристаллы белого цвета хорошо растворимы в воде и образуется красно-синий цвет.т.к присоединяется5H2O при растворении образую аквакомплексы
CuSo4 + 5H2O=[Cu(H2O)4]SO4*H2O
CuSo4* 5H2O медный купорос(синий)- противогрибковое(наружно т.к все соли меди ядовиты),антибактериальное
CuSo4* 5H2O=(t) CuSo4+ 5H2O(белый)
CuCl2 красно_зелен цвет.при растворении в воде образует комплексные соединения CuCl2*2H2O
Cu(NO3)2*3H2Oсиние кристаллы.легко разлагается при t: Cu(NO3)2*3H2O=Cu(NO3)2+3H2O
: Cu(NO3)2=(t)2CuO+4NO2+O2
(CH3COO)2Cu*Cu3(AsO3)2-ацетат арсенид меди-парижская зелень-для обработки растений
 2018-01-21
2018-01-21 1131
1131








