Качественное обнаружение:
1. Реакция с сульфаниловой кислотой и β-нафтолом. К 3 каплям диализата добавляют 3 капли 0,5% раствора сульфаниловой кислоты в 2 н растворе хлористоводородной кислоты, перемешивают: образуется соль диазония.
Спустя 3 минуты к смеси прибавляют несколько капель свежеприготовленного щелочного раствора β-нафтола – появляется оранжево-красное окрашивание или осадок. Интенсивность окраски зависит от количества нитритов в пробе.
2. Реакция с реактивом Грисса. В пробирку с 5 каплями нейтрализованного диализата вносят 3 капли реактива Грисса – появляется темно-красное, красное или розовое окрашивание с образованием осадка. Степень окраски позволяет приблизительно судить о количестве нитрита и в зависимости от этого подготовить к количественному определению стандартные растворы соответствующей концентрации.
57.Особенности химико-токсикологического анализа соединений фтора.
Отн к группе в-в, треб-х особых методов изолир-я. К эт гр в-в относ соли фтористоводородной (плавиковой) к-ты: NaF, NH4F, LiF, CaF2, BaF2, PbF2, CuF2.2H2О, NH4HF2, CrF3, NasAIFe (3NaF.AIF3) и др, а также соли кремнефтористоводородн к-ты: Na2SiF6, K2SiF6, CaSiF6 2H2О, BaSiF6 и др. Данные соли прим в пром-ти, сталеварении, стекловарении, в кач консерванта древесины, в с/х в кач инсектицидов. Отравл соед-ями фтора обусл их ошибочн прим-ем в быту вместо др солей. Токсич доза д/чел 0,012г; смертельн - 10г. Клиника и патологоанатомич картина отравл фторидами нехар-на, набл лишь местные восп-е явления. Поэт диагностика отравл ими затрудн-на. Токсич д-е объясн пораж-ем некот ферментных систем и обмена в-в, ос углеводного и солевого. При остр отравл происх пораж цнс и жкт, а при хронич происх изм-е в зубах и костях (флюороз). Фториды поступ в орг через жкт, где кисл р-я жел сока способст переходу нер-мых соед-й фтора в более р-мые, что улучш их всас-ть. В орг фтор вытесн йод из некот его орг соед-й, а также обр комплексн соед-я с рядом микроэлементов. Наиб конц-я фтора обнаруж-ся в железах внутр секреции, костях и зубах. Выд-е фтора из орг осущ почками, жкт и потовыми жел. В моче фтор появл через 30мин после введ B жел, достигая макс-ма выд-я на 1-5день. За три нед с мочой выд-ся до 55% введённой дозы. Объектами исслед-я явл моча, содерж-е жел, внутр орг и пищевые прод. Изолир-е. Измельч объект в кол-ве 25г подщелач изб едкой извести, смачив р-ром аммония нитрата или конц к-той азотной, высуш и прокалив при темп-ре не выше 500°С до полн сжиг-я. Параллельно дел слепой опыт. Кач обнаруж. Бол-во методов открытия фтора основано на травл-и стекла. Принцип таких методов закл-ся в разруш силикатной основы стекла фтористым водородом с обр-ем летучего SiF4: SiО2 + 4HF = SiF4 + 2H2О. 1. Часть остатка в платиновом (или свинцовом) тигле смач неск-ми капл воды и небольш кол-вом конц к-ты серной. Тигель быстро закрыв часовым ст, низ кот покрыт воском и на пов-ти воска сделана какая-ниб надпись при пом остр иглы. Пробу оставл на сутки и набл травление стекла в тех местах, где была сделана надпись за счёт выд-я фтористого водорода. Ск-ть травления стекла м увелич при нагр-и, но в эт случ вместо воска нужно исп-ть спец лак. 2. Часть получ золы после изолир-я смеш в проб с песком (SiО2) и доб немного конц к-ты серной. У отверстия проб держат стекл палочку с кап воды. При налич фтора выд-ся SiF4, что привод к помутн-ю капельки воды на кончике стекл пал за счёт обр-я кремниевой к-ты. 3SiF4 + 4Н2О = H2SiО4 + 4Н+ + 2[SiF6]2-. 3. В проб с нагр конц к-той помещ кристаллик К бихромата и внос испытуемую пробу (2-3кап р-ра или 5-10мг пор). Смесь нагрев и при налич фтора набл не смачиваемые места на стекле проб, от кот отстаёт тонкая плёнка хромовой смеси. Анализу меш борная и кремниевая к-ты. 3. Капельная р-я. На фильтр бум, пропит-ю цирконализариновым лаком, кот им красн окр, нанос водн р-р исслед-го в-ва. При налич фтора красн окр исчез, появл жёлт окр
Острые отравления окисью углерода. Этиологические факторы развития отравлений окисью углерода. Токсичность. Классификация отравлений окисью углерода по степени тяжести. Определение карбоксигемоглобина методом спектрофотометрии и химическими реакциями.
Отравление окисью углерода- угарный газ. С воздухом образует взрывоопасные смеси. Токсическое действие. Окись углерода присоединяется к гемоглобину крови, образуя карбоксигемоглобин (НЬСО), в результате чего понижается содержание кислорода в крови и тканях (аноксемия и гипоксия). Низкие концентрации кислорода оказывает токсическое действие на клетки, нарушая дыхание тканей. Объектами исследования являются кровь из трупа и воздух, содержащий СО. Классиф отравлений: легкое; среднетяжел; тяжелое(содерж карбоксигемоглобина.)При острых отравлениях концентрация карбоксигемоглобина в крови составляет около 40%, а при смертельных исходах до 60%. Спектрофотометр- Кровь растворяют в аммиаке, наливают в кювету и измеряют оптическую плотность (D) при длинах волн 578 и 564 нм. Хим.определ: 1. Проба Гоппе-Зейлера. К крови добавляют рр NaOH. Нормальная кровь буреет, а кровь, содержащая СОНb, не изменяется (ярко красная). 2.Проба Сальковского-Катаяма. К крови + аммония сульфида + рр кислоты уксусной до слабокислой реакции среды. Нормальная кровь - серо-зелёная, исследуемая - малиново-красная. 3. Проба Бюркера. крови + рр калия гексацианоферрата (III). Нормальная кровь - желтоватого цвета, исследуемая – красн. 4. Проба Ветцеля. крови + рр калия гексацианоферрата и ледяной кислоты уксусной. Нормальная кровь образует серовато-коричневый осадок, а исследуемая - вишнёво-красный осадок.5. Проба Либмана. Кровь+ формалина. Нормальная кровь - коричнево- чёрная, исследуемая красного цвета. 6. Проба Залесского. Кровь+ раствора меди (II) сульфата. Нормальная кровь - зеленоватая, исследуемая – красная
60.Хроматографические методы исследований, применяемые в судебно-химическом анализе. Общая характеристика.
Применяют ТСХ,ВЭЖХ, ГХ.
Хроматографией наз. Резделение в-в, осн-ное на распределении компонентов смеси м\у неподвижной(стационарной) и подвижной(мобильной)фазами. Методы тонкослойной и бум-й Х-фии осн-ны на различии скоростей перемещения компонентов анализ-ой смеси в плоском тонком слое сорбента при движении р-ля(элюента). БХ- это распед.Х-фии,в к-той неподвиж.фазой явл.целлюлоза. Распределение в-в происх.за счет разл.раств-ости в неподвиж.и неподвиж.жидкой фазе. БХ проводят в восходящем,низхоящем и горизогт-ном тока р-ля. Считают величину Rf=A\B(кач.хар-ка): зависит от природы в-ва, хромат.бумагт,природ.р-ля.Идентификация в-в проводят путем сравнения со станд.образцами. Сравнение с известными величинами Rf или после элюиров.пятна. ТСХ= Применяются сорбенты: оксид алюминия, селикогель,целлюлоза, полиамид и т.д. Осн-ные преимущества: большая скорость раздел.по сравнен.с БХ, возможность выбора неподв.фазы, Большая возм.выбора подвиж.фазы по сравнен.с БХ. Применяют пластины закрепл.и незакрепл.слое. В кач.закрепления исп.:крахмал или гипс. Разделение в хромат.камерах, исп.величину Rf. ГХ: в зависим.от агрег.сост.сорбента: 1)газожидкостная Х-фия,2)газотвердожидк.Х-фия. Обязат.условия для ГЖХ: летучесть компонен.анализ.смеси и их стойчивость при темпер.разделении. Источник газоносителя- баллон со сжатым или сжиженным газом. Чаще всего в кач. Газоносителя исп.гелий, реже азот, еще реже водород и др.газы. Осн-ные требования к азоносителю: подвижность газа, его высокая чувс-ть, взрывобезопасность, эконом.доступность. Колонки делятся на 3 вида: 1)насадочные-раздел-ая колонка,заполн. ТВ.пористым носителем,покрытым тонкой пленкой нелетучего в-ва.2)микронасадочные- отлич.меньшим диаметром.3)капиллярные. Виды детекторов в ГЖХ: катарометр, ионизационно-пламенный детектор
61.Спектральные методы анализа. Атомно-абсорбционная спектрометрия, атомно-эмиссионная спектрометрия с индуктивно-связанной плазмой Общая характеристика. Применение в химико-токсикологическом анализе.
Атомно-спектральные методы анализа основаны на измерении спектров эл\маг-го излучения,обысл-ных хим.индивид-стью определяемых компонентов. Возбуждение атомов пробы происходяит при воздействии тепловой, электромагнитной,хим-ой, электрической энергии и др. Атомно-эмисионная спектрометрия с индуктивно-связанной плазмой (АЭС). Анализируемая проба подвергается действию высоких температур, достаточных не только для диссоциации на атомы, но и для возбуждения и ионизации атомов. Возвращаясь из возбужденного в состояние с меньшей энергией, атомы испускают эл\маг-ное излучение на опред-ных длинах волн, к-рое измеряется и исп-ся для идентиф-ции исслед-х элементов. В кач-ве источника возбуждения исп-ся: пламя, печи, электрические разряды, имеющие более высокую температуру, чем пламени и печи, ИСП 10000С. Плазма- ионизированный газ с высокой энергией. Аргоновая плазма яв-ся идеальным источником возбуждения атомов в-ва. Для получения аргоновой плазмы исп-ют электрический разряд, к-ый возн.в газе при наложении магнитного поля. Работа Атомно-эмисионного спектрометра сводится к след-му. Эл\маг. Излучение, испускаемое возбужденными атомами пробы, фокусируется на входную щель диспергирующего устройства. Это устр-во разлагает свет на составные части, превращая его в спектр.Такие устр-ва могут быть 2-х видов: призменные и дифракционные. В призменных устр-вах световой поток разлагается призмой вследствие разных показателей преломления для лучей разной длины волн. В дифрак-ных устр-вах дисперсия происх-т при
62.Иммунохимические методы анализа в химико-токсикологических исследованиях. Общая характеристика, принцип метода. Применение в химико-токсикологическом анализе.
ИХМА, осн-ые на специфическом связывании определяемого соединения соответствующими антителами.ИМХА высокочувс-ны, имеют групповую специфичность, просты в исполении, позвл.одновремено исследовать большое число проб без специальной подготовки и потому удобны для скрининг-диагностики. Классификация основных ИХМА: 1)радиоиммунный анализ- РИА(Способ детек.-радиоакт-ть),2)иммуноферментный анализ- ИФА(ферментативная акт-сть),3)поляризационный флуороиммуноанализ-ПФИА (интенсивность флуоресцентной поляризации),4)иммунохроматографический анализ (образ-ние окрашенного комплекса в тест-зоне),5)металлоиммуноанализ(атомные спектры поглощения),7) рефрактометрический иммуноанализ (преломление света). Наибольшее распр-ние в химико-токс.ан-зе наркот-их и лек.в-в получили ПФИА, ИФА и РИА. Для ПФИА мочи с пом.TD[-анализатора исп.набор реагентов-стандартов:опиаты, барбитураты,бензодиазепины, каннабиноидв,амфетамин-метамфетамин,амфетамин,кокаин,метадон,эфедрин,фенобарбитал,барбамил. Методика проведения анализа вкл.нес-ко этапов- калибровку, собственно анализ, подтверждающий анализ. Для анализа образцов мочи в карусель для анализа помещ.необх.число измерит-х кювет и картриджей, соотв-щее числу образцов.Прибор атомат-ки проводит анализ в теч.15-20 мин и выдает распечатку с указанием сод-и анал-го в-ва в образцах мочи.При получении положительного рез-та, требуется провести дальнейшее исслед-ние образца мочи подтверж-ми методами: хромато-масс-спектрометрий, ГЖХ,ВЭЖХ. При отриц-ном рез-те дельнейшее исслед.не проводят.
63. Спектрофотометрия (прямая, дифференциальная). Общая характеристика. Применение в химико-токсикологическом анализе
Спектрофотометрия - метод исследования и анализа веществ, основанный на измерении спектров поглощения в оптической области электромагнитного излучения. В большинстве спектрофотометров, применяемых в аналитической практике, монохроматизация светового потока осуществляется за счет использования диспергирующих (разлагающих свет в спектр) элементов — призм или дифракционных решеток. Разработаны различные конструкции спектрофотометров, работающих как по однолучевой (одноканальной), так и по двухлучевой (двухканальной) схеме. Принципиальная блок-схема, включающая основные узлы, обеспечивающие работу спектрофотометра.
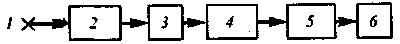
1 – источник излучения; 2 — монохроматор; 3 — кюветное отделение; 4 — приемник излучения (фотоэлементы); 5 – усилитель; 6 – регистратор (отсчетное или записывающее устройство).
Свет от источника излучения 1 попадает в монохроматор 2, в котором он разлагается в спектр. Монохроматизованный световой поток проходит после этого через кюветное отделение 3, в котором устанавливаются кюветы с анализируемым раствором и раствором сравнения («нулевым» раствором). Пройдя через кюветы с растворами, световой поток попадает на фотоэлементы приемника излучения 4, в котором энергия светового потока преобразуется в фототок, усиливаемый в блоке усилителя 5, после чего усиленный электрический сигнал регистрируется в блоке регистратора 6 либо в виде спектральной кривой, либо по показанию отсчитывающего устройства. В качестве источника излучения в спектрофотометрах используют лампы накаливания при работе в видимой области спектра, в которой они обеспечивают непрерывный световой поток (а не линейчатый, даваемый ртутной лампой), и водородные либо дейтериевые лампы — при работе в УФ диапазоне спектра (-200—350 нм). Для разложения светового луча в спектр в монохроматоре чаще всего используют призмы или дифракционные решетки. При работе в видимой и в ближней ИК области используют стеклянные призмы, а также стеклянные конденсоры (линзы) и кюветы. При работе в УФ диапазоне 200-400 нм применяют кварцевую оптику (призмы, конденсоры, кюветы), так как стекло поглощает УФ лучи.
 2018-01-21
2018-01-21 827
827








