Химические свойства алканов определяются природой химической связи и строением.
Для алканов характерны реакции замещения (S), отщепления (E), расщепления, окисления.
Реакции замещения
К реакциям замещения относятся реакции галогенирования, нитрования, сульфогалогенирования, сульфоокисления.
1. Галогенирование. Галогенирование - реакция замещения атома водорода на галоген (чаще всего Cl, Br). Основным условием протекания реакции является УФ - излучение или температура (250 - 400°С) (инициирование).
По реакционной способности галогены располагаются в следующем порядке: Cl > Br > I

Хлорирование метана - цепной радикальный процесс:
Стадия 1 – зарождение цепи (инициирование):

Стадия 2 – рост цепи:

Стадия 3 – обрыв цепи:

При галогенировании изобутана образуется смесь изомеров – 2-хлор-2-метилпропана (64%) и 2-метилхлорпропана (36%)

В процессе хлорирования изобутана на стадии роста цепи образуется два радикала - первичный и третичный:

Более устойчивым радикалом является третичный, так как у него делокализация неспаренного электрона больше, чем у первичного, вследствие +I (индукционный эффект) и гиперконьюгационного эффекта:
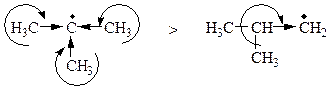
9 sС-Н связей 1 sС-Н связь
Устойчивость радикалов увеличивается в ряду
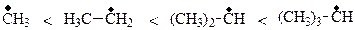
Различная устойчивость образующихся на стадии роста цепи алкильных радикалов определяет активность третичных, вторичных и первичных sС-Н связей: наиболее активна третичная С-Н связь, затем вторичная и первичная.
 2017-11-01
2017-11-01 648
648








