При электрохимической коррозии выделяют два взаимосвязанных процесса: анодный и катодный.
- Анодный процесс – окисление металла, проходит на участках изделий с меньшим потенциалом в данной среде. Анодные участки разрушаются.
- Катодный процесс – восстановление окислителя, находящегося в растворе или расплаве электролита, происходит на участках изделий с бóльшим потенциалом в данной среде. Катодные участки химически не изменяются. Они служат проводниками электронов от анодных участков к окислителю, чем усиливают коррозию анодных участков. Более подробно это будет рассмотрено далее на конкретных примерах.
Окислители при коррозии принято называть деполяризаторами. Коррозию с участием наиболее распространенных окислителей – растворенного кислорода и ионов водорода (кислоты или воды) соответственно называют коррозией с кислородной и водородной деполяризацией. Уравнения катодных процессов приведены в таблице.
| Уравнения катодного процесса при коррозии | |
| с водородной деполяризацией (в отсутствие растворенного О2) | с кислородной деполяризацией в присутствии растворенного О2) |
| кислая среда | |
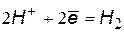 (1) (1) | 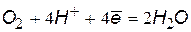 (3) (3) |
| нейтральная и щелочная среда | |
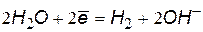 (2) (2) | 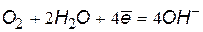 (4) (4) |
Окислительно-восстановительные потенциалы кислорода и водорода в различных средах (точнее, соответствующих окислительно-восстановительных пар) указаны в таблице.
| Кислая среда (рН = 0) | Нейтральная среда (рН = 7) | Щелочная среда (рН = 14) | |||
| Oк/Вс | Е0, В | Oк/Вс | Е0, В | Oк/Вс | Е0, В |
| 2H+/H2 | 0,00 | 2H2O/H2 | -0,41 | 2H2O/H2 | -0,83 |
| O2/2H2O | +1,22 | O2/4OH– | +0,81 | O2/4OH– | +0,40 |
Окислительные свойства кислорода выше окислительных свойств иона водорода (или воды). В присутствии кислорода в растворе коррозия необязательно будет проходить за счет кислородной деполяризации, так как концентрация растворенного кислорода, как правило, невелика. Установлено, что при рН³7, т.е. в нейтральных и щелочных растворах, процесс обычно протекает с кислородной деполяризацией - уравнение (4), в кислых средах – преимущественно с водородной деполяризацией - уравнение (1).
Коррозия, как и любой окислительно-восстановительный процесс, может осуществляться только при условии, что потенциал окислителя больше потенциала восстановителя (металла анодных участков).
 2014-01-25
2014-01-25 3867
3867
