Своеобразие свойств вещества в коллоидном состоянии объясняется тем, что значительная доля всех молекул или атомов, составляющих вещество, находится на поверхности раздела фаз; эти молекулы являются «особенными» (отличными от тех, которые находятся в объеме, при том же химическом составе) как по положению в несимметричном силовом поле, так и по энергетическому состоянию. В итоге вклад поверхностных сил в свойства системы существенно превосходит вклад объемных свойств составляющих ее веществ.
Поверхность раздела фаз в коллоидной химии – это граничная область между фазами, слой определенной толщины, в котором происходит изменение различных свойств от значений, характерных для одной фазы, до значений, характерных для другой.
На границе раздела фаз формируется поверхностный слой (межфазная поверхность) толщиной в один или несколько молекулярных размеров (диаметров). Термодинамические параметры межфазной поверхности отличаются от аналогичных параметров объемной фазы того же вещества.
С понятием «поверхность» связано представление о поверхностных явлениях. Поверхностные явления – это процессы, возникающие на любой границе раздела двух или нескольких фаз и приводящие к изменению свойств веществ при переходе от протяженного тела к межфазным поверхностным слоям.
Эти явления обусловлены тем, что контактирующие фазы различаются по структуре и, соответственно, по физико-химическим свойствам. Следовательно, силовое поле, действующее на структурные элементы вещества (молекулы, ионы, атомы, атомные группировки, ассоциаты), которые находятся в поверхностных слоях и контактируют с другими фазами, будет отличаться от силового поля, которое действует на структурные элементы вещества в объеме тела. И чем больше различия в свойствах фаз, тем сильнее будут выражены различия в свойствах межфазной поверхности и объема каждой из фаз.
Нескомпенсированность межмолекулярных взаимодействий, в свою очередь, обусловлено различием состава и строения контактирующих фаз. Это порождает возникновение на поверхности раздела поверхностных сил и избытка энергии – поверхностной энергии.
Наиболее просто связь между поверхностными свойствами и термодинамическими характеристиками контактирующих фаз проявляется для однокомпонентных двухфазных систем (например, жидкость на границе с ее насыщенным паром).
На поверхности раздела фаз молекулы испытывают сильное притяжение со стороны жидкой фазы и почти никакого притяжения со стороны паровой фазы. Равнодействующая сил направлена в сторону жидкости и стремится втянуть молекулы внутрь жидкой фазы. Эта равнодействующая сила называется внутренним молекулярным давлением.
Его причиной является межмолекулярное взаимодействие, и чем оно больше, тем больше внутреннее давление.
Две вышеупомянутые фазы (жидкость и пар) могут существовать в равновесии только при наличии устойчивой границы раздела между ними, не проявляющей тенденции к самопроизвольному увеличению, т. е. термодинамически устойчивой (при данных температуре и объеме системы). С макроскопической точки зрения это означает, что с поверхностью связана некоторая энергия, так что общая энергия системы не является суммой энергии двух объемных фаз, а включает еще и избыточную энергию, пропорциональную площади поверхности раздела фаз:
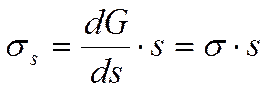 .
.
Входящая в это уравнение величина σ – это удельная (приходящаяся на единицу площади) поверхностная энергия. Наличие на поверхности раздела фаз избытка энергии означает, что для образования новой поверхности нужно совершить работу, поэтому величина σ одновременно представляет собой работу обратимого изотермического образования единицы поверхности; эту величину также называют поверхностным натяжением.
Оно характеризует избыток поверхностной энергии, приходящийся на 1 м2 межфазной поверхности.
Поверхностное натяжение (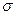 ) равно термодинамически обратимой изотермической работе, которую надо совершить, чтобы увеличить площадь межфазной поверхности на единицу.
) равно термодинамически обратимой изотермической работе, которую надо совершить, чтобы увеличить площадь межфазной поверхности на единицу.
Применительно к дисперсной системе можно записать объединенное уравнение первого и второго начал термодинамики относительно энергии Гиббса:
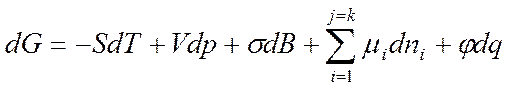 (1)
(1)
где S – энтропия; dT, dp – изменение температуры и давления; dВ – изменение площади поверхности раздела фаз; σ – поверхностное натяжение; μi, ni – химический потенциал и число моль компонента i; φ, q – электрический потенциал и заряд поверхности.
В условиях изобарно-изотермического процесса (dT = 0, dp = 0) в отсутствии физико-химических и электростатических взаимодействий граничных фаз (dni = 0, dq = 0) из уравнения (1) получим выражение для свободной поверхностной энергии через отношение удельных энергии Гиббса и площади поверхности раздела фаз:
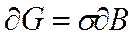 ,
,  (2)
(2)
Индексы T, p, ni и q означают, что температура, давление, число моль компонента i и электрический заряд поверхности остаются неизменными.
Таким образом, поверхностное натяжение есть частная производная от энергии Гиббса по площади раздела фаз при постоянной температуре, давлении, в отсутствие химического, электрического и других видов взаимодействия.
Напомним, что кроме энергии Гиббса можно использовать энергию Гельмгольца для описания изменения поверхностной энергии на границе раздела фаз:
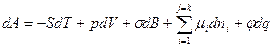 (3)
(3)
и что существует связь между характеристическими функциями:
dG = dH – TdS
dA = dU – TdS
Отсюда 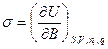 (4) или
(4) или 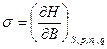 (5) или
(5) или 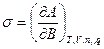 (6)
(6)
Обычно поверхностное натяжение выражают через энергию Гиббса, так как легче обеспечить постоянные давление и температуру, чем объем.
Поверхностное натяжение с повышением температуры уменьшается, и в критической точке, при которой поверхность раздела “жидкость – пар” исчезает, поверхностное натяжение равно нулю. Чем меньше σ на границе раздела двух жидкостей σ 1,2, тем выше взаимная растворимость. При критической температуре поверхностное натяжение σ1,2 на границе двух взаимно ограниченных растворимых жидкостей равно разности поверхностных натяжений этих жидкостей на границе с воздухом (правило Антонова).
σ 1,2 = σ 1 - σ 2
Поверхностные явления зависят не только от температуры, но и от давления, природы вещества фаз и величины поверхности.
Если для чистых индивидуальных веществ величина σ имеет определенное значение, то для растворов σ зависит не только от природы жидкости-растворителя, второй граничащей среды, температуры, но и от природы и количественного содержания растворенного вещества.
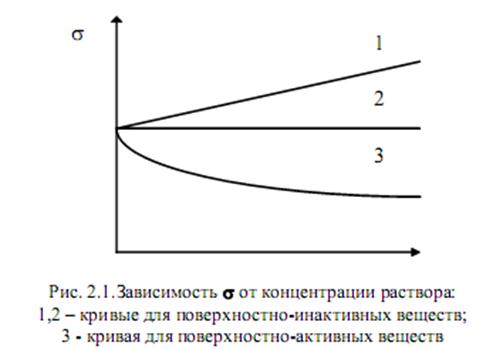
Обозначим через σ0 поверхностное натяжение растворителя, через σ - поверхностное натяжение раствора. При растворении вероятны следующие случаи:
1) σ > σ0 - растворенное вещество (ПИВ) повышает поверхностное натяжение растворителя;
2) σ = σ 0 - растворенное вещество не изменяет поверхностного натяжения растворителя;
3) σ < σ 0 - растворенное вещество (ПАВ) понижает поверхностное натяжение растворителя.
Согласно современной теории П.А.Ребиндера дисперсные системы делятся на лиофобные и лиофильные по величине свободной межфазной энергии σ1,2. Условие существования лиофобной системы может быть выражено σ2,1 > σ m, где σ m - некоторая граничная величина, которая характеризует среднюю кинетическую энергию теплового движения частиц:
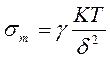
где γ - безразмерный множитель;
к - постоянная Больцмана;
δ - дисперсность частиц, участвующих в броуновском движении.
Условие существования лиофильной коллоидной системы может быть выражено σ 1,2< σ m. Такие лиофильные системы образуют мыла, красители, самопроизвольно образующиеся эмульсии.
Поверхностное натяжение растворов отличается от такового у чистых жидкостей и зависит от концентрации растворенного вещества в соответствии с кривой, называемой изотермой поверхностного натяжения, характеризующей раствор при постоянной температуре.
Существует несколько методов определения поверхностного натяжения.
1. метод наибольшего давления образования пузырьков.
Основан на законе Лапласа.
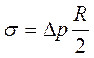
Где R – радиус пузырька или капилляра.
Проводят в приборе Ребиндера. Вычисление ведут по формуле, опираясь на справочные данные для воды.
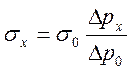
2. метод счета капель – сталагмометрия.
Основан на счете и взвешивании капель.
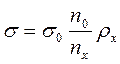
где n0 и nх число капель воды и исследуемой жидкости соответственно, ρх – плотность исследуемой жидкости.
3. метод отрыва кольца (используют торсионные весы)
4. метод взвешивания платиновой рамки
5. метод капиллярного поднятия жидкости.
Основан на зависимости молекулярного давления от кривизны поверхности раздела фаз. На вогнутых поверхностях оно меньше, на выпуклых - больше, чем на плоских. Этим объясняется поднятие уровня жидкости в капилляре.
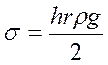
Где h – высота капиллярного поднятия;
r – радиус капилляра;
g – ускорение свободного падения (9,8 м/с2);
ρ – плотность жидкости.
 2014-01-31
2014-01-31 2095
2095
