Реактивы: смесь фенола с водой, 10 %-ный раствор гидроксида натрия, 10 %-ный раствор серной кислоты, 10 %-ный раствор карбоната натрия, насыщенный раствор гидрокарбоната натрия.
К 1 мл смеси фенола с водой постепенно при перемешивании прибавляют 10 %-ный раствор гидроксида натрия до полного растворения фенола. К полученному раствору фенолята натрия по каплям приливают 10 %-ный раствор серной кислоты. Наблюдают помутнение раствора в результате выделение малорастворимого в воде фенола:


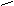
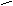

 ОН ОNа
ОН ОNа
+ NаOН + H2O
фенол фенолят натрия
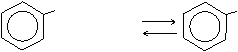 ОNа ОН
ОNа ОН
+ H2SO4 + NаHSO4
фенолят натрия фенол
В две пробирки наливают по 0,5 мл смеси фенола с водой, затем в одну из них прибавляют 1-2 мл раствора карбоната натрия, а в другую – 1-2 мл раствора гидрокарбоната натрия. Отмечают, что фенол растворился в пробирке, содержащей карбонат натрия.
 ОН ОNа
ОН ОNа
+ Nа2СO3 ¾® + NаНСO3
фенол фенолят натрия
Контрольные вопросы:
1. Какие свойства проявляет фенол в реакциях со щёлочью и карбонатом натрия?
2. Почему фенол растворяется под действием карбоната натрия и не растворяется под действием гидрокарбоната натрия?
Опыт 80. Взаимодействие фенолов с бромной водой
Реактивы: растворы фенола, пирокатехина, резорцина, гидрохинона и пирогаллола, полученные в оп. 78, бромная вода.
Бромирование фенола
К 1 мл водного раствора фенола, полученного в оп. 78, добавляют по каплям бромную воду. Образующееся в начале помутнение при встряхивании исчезает. Продолжают приливать бромную воду в пробирку при встряхивании и наблюдают появление обильного белого осадка, переходящего в светло-жёлтый.
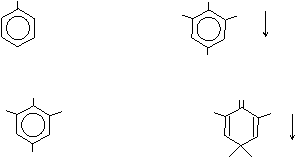 ОН ОН
ОН ОН
(Н2О) Br Br
+ 3 Br2 ¾¾®
- 3 HBr
фенол Br
2,4,6- трибромфенол (белый осадок)
ОН О
Br Br (Н2О) Br Br
+ Br2 ¾¾®
- HBr
Br Br Br
тетрабромциклогексадиенон (жёлтый осадок)
 2018-03-09
2018-03-09 1888
1888








