Реактивы: бензол, толуол, ксилол, концентрированная серная кислота (r = 1,84 г/см3).
Сульфирование бензола, толуола и ксилола проводят параллельно. В одну пробирку наливают 1 мл бензола, в другую – 1 мл толуола, в третью – 1 мл ксилола (пробирки должны быть сухими). Затем в каждую пробирку добавляют по 4 мл концентрированной серной кислоты (r = 1,84 г/см3). Пробирки закрывают пробками с воздушными холодильниками и нагревают на кипящей водяной бане, часто встряхивая смесь, в течение 15 минут. При встряхивании углеводороды образуют с кислотой эмульсии, которые постепенно растворяются. Чем быстрее сульфируется углеводород, тем быстрее он переходит в раствор (объясните, почему). Отмечают различие в скоростях сульфирования бензола, толуола и ксилола. Нагревание прекращают, когда в одной из пробирок реакционная смесь перестаёт расслаиваться. Все пробирки охлаждают и выливают их содержимое в отдельные стаканчики с холодной водой (по 20-25 мл); отмечают, в каком стаканчике непрореагировавшего исходного вещества выделилось больше. Делают вывод о том, какой из трёх углеводородов сульфируется легче всего, а какой труднее.






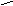

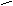
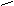 СН3 CH3 CH3
СН3 CH3 CH3

 2 + 2H2SO4 +
2 + 2H2SO4 +
 - 2 H2O SO3H HO3S
- 2 H2O SO3H HO3S
толуол о-толуол- п-толуол-
сульфокислота сульфокислота
Напишите уравнения реакции сульфирования орто-, мета- и пара-ксилолов, а также бензола.
Контрольные вопросы:
1. По каким признакам можно судить о скорости протекания реакции сульфирования бензола и его гомологов?
2. Объясните, как алкильные радикалы влияют на скорость сульфирования в ароматическом кольце?
3. Рассмотрите механизм реакции сульфирования мета-ксилола.
4. Предложите способ выделения из реакционной смеси продуктов сульфирования бензола и его гомологов.
Фенолы.
Осторожно: фенолы могут вызвать ожоги кожи!
 2018-03-09
2018-03-09 753
753








