В гальванических элементах типа Даниэля—Якоби (медно-цинковый) сами металлические электроды принимают участие в окислительно-восстановительной реакции, лежащей в основе работы элемента. Однако большинство окислительно-восстановительных процессов в растворах протекают между простыми и сложными ионами. При измерении э. д. с. гальванического элемента на основе таких реакций применяют инертные электроды — платиновые или графитовые, которые не участвуют в протекающих химических взаимодействиях, а являются лишь передатчиками электронов между ионами-восстановителями и ионами-окислителями.
Выполнение работы. Измерить э. д. с. гальванического элемента на основе окислительно-восстановительной реакции:
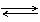 Sn2+ +Fe3+ Sn0+Fe2+
Sn2+ +Fe3+ Sn0+Fe2+

 Для этого в один стаканчик (см. рис. 37) налить раствор, состоящий из смеси солей SnCl2 и SnCl4 с концентрацией каждой соли в нём 1 моль/л и погрузить в раствор платиновую проволоку. На поверхности платинового электрода устанавливается равновесие,
Для этого в один стаканчик (см. рис. 37) налить раствор, состоящий из смеси солей SnCl2 и SnCl4 с концентрацией каждой соли в нём 1 моль/л и погрузить в раствор платиновую проволоку. На поверхности платинового электрода устанавливается равновесие,
 Sn4+ + 2е Sn2+
Sn4+ + 2е Sn2+
которое и определяет потенциал электрода E(Sn4+/Sn2+). В другом стаканчике погрузить платиновую проволоку в раствор смеси солей железа (III) и железа (II) с концентрацией обоих ионов железа 1 1моль/л. В этом случае на поверхности платинового электрода "возникает равновесие,
 Fe3+ + e Fe2+
Fe3+ + e Fe2+
определяющее потенциал электрода Е(Fe3/Fe2+). Соединить стаканчики электролитным мостиком, подключить электроды к потенциометру и записать значение э. д. с. гальванического элемента по показанию шкалы прибора в милливольтах.
Запись данных опыта. Пользуясь значениями стандартных, электродных потенциалов, вычислить э. д. с. исследованного гальванического элемента. Сравнить значение э. д. с. полученное в опыте и вычисленное по табличным данным.
 2018-02-13
2018-02-13 542
542








