I следствие:
Понижение температуры кристаллизации раствора по сравнению с растворителем прямо пропорционально моляльной концентрации раствора:
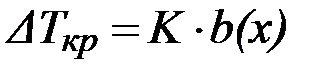
|
где К – криоскопическая постоянная растворителя (К×кг/моль);
b(х) – моляльная концентрация раствора (моль/кг).
II следствие:
Повышение температуры кипения раствора по сравнению с растворителем прямо пропорционально моляльной концентрации раствора:
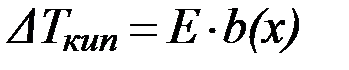 , ,
|
где Е – эбулиоскопическая постоянная растворителя (К×кг/моль).
Значения констант К и Е определяются исключительно природой растворителя.
Криоскопическая и эбулиоскопическая постоянные растворителя (К и Е) - имеют физический смысл понижения температуры кристаллизации и повышения температуры кипения раствора с концентрацией 1 моль/кг.
Температура кристаллизации раствора (Tкр.)- температура, при которой давление пара растворителя над раствором становится равным давлению пара над твердой фазой.
Температура кипения раствора (Tкип)- температура, при которой давление пара растворителя над раствором становится равным атмосферному давлению.
Понятие диффузии и осмоса, сходство и различие этих процессов.
Диффузия -процесс самопроизвольного выравнивания концентраций веществ в термодинамической системе.
Осмос -процесс преимущественно одностороннего проникновения молекул растворителя через полупроницаемую мембрану.
Скорость пассивной диффузии при равновесии равна скорости осмоса. Диффузионное передвижение вещества всегда идет от большего к меньшему химическому потенциалу, а осмос может происходить в любом направлении. Диффузия является двусторонним процессом.Осмос преимущественно односторонний процесс.
 2020-01-15
2020-01-15 202
202








