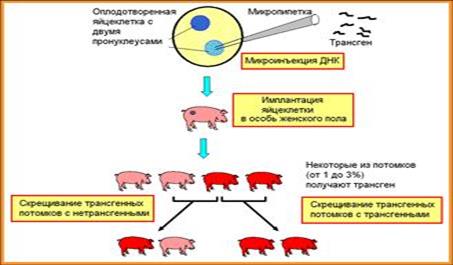
Рекомбинантную ДНК вводят с помощью микроинъекции в один из пронуклеусов оплодотворенной яйцеклетки. Интеграция трансгена (перенесенного генетического материала) происходит случайно и может привести к нарушению экспрессии генов и быть летальной.Трансген интегрирует только в одну хромосому, поэтому трансгенное животное является гемизиготным. Трансгенные животные как фармацевтические фабрики (биореакторы). Продукция фармацевтически- важного белка (например активатора плазминогена для растворения кровяных тромбов) с молоком трансгенной овцы. Трансгенные быстрорастущие породы лосося были получены введением гена гормона роста под контролем сильного промотора. Все особи одного возраста; вес трансгенных рыб в 11 раз выше веса нетрансгенного контроля.
ПРИМЕНЕНИЕ
При введении свиньям трансгена бычего гормона роста под контролем промотора металлотионеина неблагоприятные эффекты наблюдались. Количество гормона у разных особей в группе трансгенных свиней различалось, однако в целом вся эта группа быстрее прибавляла в весе. К сожалению, этот положительный результат частично обесценивался различными патологиями: у животных отмечались язва желудка, почечная недостаточность, хромота, воспаление перикарда, уменьшение подвижности суставов, предрасположенность к пневмонии. Причины этих симптомов неизвестны. Возможно, они связаны с долговременным присутствием в организме избытка гормона роста. В этих экспериментах трансген синтезировался более или менее непрерывно.
Положительные результаты были получены и в ходе экспериментов с трансгенными свиньями. Например, были созданы здоровые трансгенные свиньи, в геноме которых присутствовала следующая генетическая конструкция: регуляторная область гена Р-глобина человека, два гена а,-глобина человека и один ген рА-гло- бина человека. В результате ее экспрессии в клетках крови свиней синтезировался человеческий гемоглобин, при этом в результате замены человеческого промотора гена р-глобина свиным человеческий гемоглобин синтезировался в значительно большем количестве. Человеческий гемоглобин, продуцируемый трансгенныи сзичьями, обладал такими же химическими свойствами, что и природный человеческий. Его можно было очистить от гемоглобина свиней обычной хроматографией. Эти результаты указывают на принципиальную возможность замены цельной крови, используемой при трансфузии, человеческим гемоглобином, полученным методом трансгеноза. Однако изолированный гемоглобин переносит кислород не так эффективно, как гемоглобин в составе эритроцитов. Более того, он быстро разрушается в организме животного, которому был введен, а продукты его распада токсичны для почек. Таким образом, получение заменителя человеческой крови с помощью трансгеноза — это дело далекого будущего.
В последнее время большое внимание уделяется вопросу об использовании органов животных для трансплантации человеку. Основная проблема межвидовой трансплантации — это гиперострое отторжение. Гиперострое отторжение влечет за собой связывание антител организма- хозяина с углеводной антигенной детерминантой на поверхности клеток пересаженного органа. Связавшиеся антитела вызывают острую воспалительную реакцию (активацию каскада комплемента), происходит массовая гибель несущих антитела клеток и быстрая потеря пересаженного органа. В естественных условиях воспалительная реакция блокируется особыми белками на поверхности клеток, выстилающих стенки кровеносных сосудов. Эти белки — ингибиторы комплемента видоспецифичны. Было высказано предположение, что если бы животное-донор несло один или несколько генов человеческого белка, ингибирующего комплемент, то пересаженный орган был бы защищен от первичной воспалительной реакции. С этой целью были получены трансгенные свиньи, несущие различные человеческие гены ингибитора комплемента. Клетки одного из этих животных оказались совершенно нечувствительными к компонентам системы каскада комплемента. Предварительные эксперименты по пересадке органов трансгенных свиней приматам показали, что ткани пересаженного органа повреждаются слаьее, а сам орган не отторгается немного дольше. Возможно, трансгенные свиньи, несущие человеческий ген ингибитора комплемента и лишенные основного поверхностного белка клеток свиней, который вызывает острейшее отторжение, будут служить источником органов для трансплантации человеку.
35 Укажите основную цель генной терапии соматических клеток человека; дайте характеристику методам генной терапии ex vivo и in vivo?
Соматическая генная терапия вносит изменения в гены любых клеток организма, за исключением репродуктивных клеток. В качестве мишеней предлагаются самые различные органы: костный мозг, печень, мышцы, кожа, легкие, кровеносные сосуды, сердце, головной мозг. Соматическая терапия, однако, сознательно избегает таких генетических изменений, которые могут передаваться потомству пациента. Следовательно, цель этого вида генной терапии такая же, как и в традиционной медицине – спасение человеческой жизни или облегчение страданий больного.
Соматическая генная терапия подразделяется на две категории в зависимости от того, каким методом осуществляют интродукцию генов. Во многих ситуациях клетки вначале удаляют из организма пациента, а затем подвергают обработке в лаборатории; эту процедуру часто называют генной терапией ex vivo. Как только генетическая модификация будет завершена, клетки возвращают в организм пациента в надежде на то, что они приживутся в ткани-мишени в количестве, достаточном для достижения желаемого эффекта. Ввиду того, что протоколы ex vivo должны составляться для каждого человека индивидуально, они трудоемки и дорогостоящи. Так же сущетсвует in vivo.
 2020-01-14
2020-01-14 264
264








