Современные технологические процессы массового производства черных и ряда цветных металлов связаны с наличием жидких фаз:
– металлической,
– оксидной (шлак), в основном, в процессах черной металлургии;
– сульфидной (штейн), в процессах цветной металлургии.
При взаимодействии расплавов между собой и с газовой фазой идут химические реакции:
– окисления примесей;
– восстановления элементов;
– науглероживания и обезуглероживания;
– дегазации металла;
– легирования металла;
– десульфорации (обессеривания);
– дефосфорации (обесфосфоривания) и др.
При разработке технологии проведения плавки — получения металлического сплава заданного состава необходимо знать:
– закономерности перераспределения различных элементов между металлургическими фазами,
– уметь рассчитывать термодинамическую активность компонентов в металлургических расплавах,
– оценивать влияние различных факторов на полноту перехода элементов из одних фаз в другие,
– оценивать скорости процессов.
В основе этих знаний лежат:
– представления о строении (структуре) расплавов и природе сил, действующих между структурными единицами расплава,
– данные о физико-химических свойствах расплавов (вязкости, электропроводности и др.).
Под структурой расплава понимают взаимное расположение в пространстве составляющих его частиц.
Структура расплава взаимосвязана:
– с электронной природой частиц, величиной сил взаимодействия между частицами;
– с физико-химическими свойствами расплава.
По вышеуказанным признакам металлические расплавы существенно отличаются от расплавленных шлаков (и штейнов). Эти жидкости рассматривают раздельно.
Металлические расплавы
Структура расплавов
Для металлических расплавов характерны значительные силы взаимодействия между атомами. Как следствие – отщепление валентных электронов и их коллективизация. Межчастичные связи – это взаимодействия катионов с коллективом свободных электронов.
Температура расплавов в обычных металлургических процессах незначительно превышает их температуру плавления (исключения – электронная, плазменная плавки). В этом случае жидкости по своим свойствам и строению близки к твердым телам, но не к газам.
Экспериментальные факты.
1. Относительное увеличение объема металлов при плавлении металлов не более
6 %. Объем при испарении увеличивается в десятки раз.
Значит, средние расстояния между атомами при плавлении изменяются мало.
2. Теплота плавления существенно меньше теплоты испарения.
| , | Mn | Cu | Cr | Fe |
 | 14,6 | 13 | 16,4 | 15,4 |
 | 231 | 304,6 | 315,9 | 352,5 |
Значит, силы сцепления между атомами при плавлении ослабляются относительно мало.
Изменение энтропии: 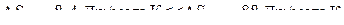 .
.
Значит, порядок в жидкости нарушается при плавлении относительно мало.
3. Теплоемкости металлов при плавлении изменяются незначительно.
| Mn | Ni | Cr | Fe | Al | |
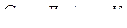 | 46,4 | 35,8 | 42,7 | 41,8 | 32,6 |
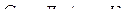 | 46,0 | 35,8 | 40,6 | 34,1 | 29,3 |
Значит, с учетом (1–2) в жидкости сохраняется характер теплового движения, свойственный твердому металлу.
4. При 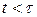 жидкость проявляет твердость, хрупкость и малую сжимаемость (кратковременные трещины).
жидкость проявляет твердость, хрупкость и малую сжимаемость (кратковременные трещины).
5. Рентгенограммы жидкостей сходны с рентгенограммами микрокристаллических тел (с размерами кристалликов ~ 1 нм (10–9м).
Для жидкостей характерен ближний порядок и отсутствие дальнего порядка.
Прямое изучение структуры жидких металлов весьма затруднено и практически невозможно. Особенно это относится к железу и его сплавам, имеющим высокую температуру плавления. Поэтому предложенные модели жидкого состояния основываются на косвенных данных и теоретических предположениях. В значительной мере они гипотетические. Рассмотрим некоторые из них.
Согласно модельной теории свободного объема жидкость состоит из объема составляющих ее частиц и «свободного объема», образовавшегося вследствие скачкообразного уменьшения плотности при плавлении. При этом образуются как бы отдельные ячейки, в которых, вследствие свободного объема, происходит колебание частиц. Принимается, что каждая частица колеблется в своей ячейке независимо от других. Определяется средний потенциал взаимодействия частицы с окружающими ее частицами («стенками ячейки») и рассчитывается сумма состояний всей системы.
Модель свободного объема оказалась полезной для описания явлений переноса. Так А.И. Бачинский принял, что динамическая вязкость жидкости обратно пропорциональна величине свободного объема:
η = α /(Vж — Vтв),
где VЖ и Vтв — объемы 1 моля жидкости и твердого тела; α — постоянная для данной жидкости.
Это правило хорошо согласуется с опытными данными.
Особое значение для развития представлений о жидком состоянии имеет теория Я.И. Френкеля (1926 г.), так называемая дырочная теория, получившая развитие и в работах других исследователей. Согласно этой теории при нагреве, тем более при плавлении, увеличение объема происходит не только за счет увеличения расстояния между частицами, но и, главным образом, за счет возникновения добавочных вакантных узлов — «дырок». Количество этих дырок при нагреве металла увеличивается постепенно, а при плавлении – скачкообразно вследствие потери устойчивости в расположении частиц. Значительное увеличение количества дырок при плавлении вызывает резкое увеличение коэффициентов диффузии, осуществляемой через вакантные места, и повышение растворимости.
Радиус образуемых дырок или полостей имеет размер порядка десятых нанометра, т.е. такого же порядка, как и параметр решетки. Так как возникновение дырок или полостей равновероятно в любой группе частиц, они непрерывно появляются в одних местах и исчезают в других.
Увеличение амплитуды колебаний частиц и расстояний между ними, а также образование большого количества дырок сильно искажают правильное расположение атомов в пространственной решетке при плавлении. При этом нарушается дальний порядок в расположении атомов, но сохраняется ближний порядок, т.е. характерное для кристаллов правильное расположение атомов в равновесных положениях в «узлах решетки» на некотором расстоянии от произвольно выбранного центрального атома. С учетом ближнего порядка строение жидкости иногда называют квазикристаллическим.
Ближний порядок распространяется на небольшие расстояния, оцениваемые примерно в 1...2 нм. С возрастанием расстояния от произвольно выбранного центрального атома возрастает степень неопределенности в относительном расположении более отдаленных атомов.
Тепловое движение частиц в жидкости вблизи температуры плавления также подобно движению в кристаллах. Оно состоит из колебаний возле центров равновесия и относительно редких скачков из одногo центра равновесия в другой. В случае несферических молекул к этому добавляются вращение частиц.
Средняя продолжительность оседлой жизни в положении подвижного равновесия в узле квазикристаллической решетки, т.с. длительность задержки между перескоками (τ) согласно уравнению (1) пропорциональна периоду колебаний ( ,с) вблизи этого положения равновесия и сильно зависит от температуры, причем уменьшается с ростом последней:
,с) вблизи этого положения равновесия и сильно зависит от температуры, причем уменьшается с ростом последней:
 ,
,
где 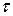 – время «оседлой жизни» частиц;
– время «оседлой жизни» частиц;  – период колебаний частиц;
– период колебаний частиц; 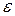 – энергия активации «скачка» частицы;
– энергия активации «скачка» частицы; 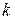 – постоянная Больцмана;
– постоянная Больцмана; 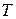 – температура.
– температура.
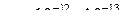 .
. 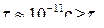
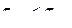
Следовательно, в жидкости колебание атомов около некоторого среднего положения не изменяется в течение от 10 до 1000 колебаний.
Значительное число совершающихся в жидкости скачков частиц с места на место и, соответственно, малая, по сравнению с перемещением в кристаллах, продолжительность оседлой жизни вызывает проявление основного внешне видимого свойства жидкостей — их текучести. Значительное повышение температуры жидкости над точкой плавления вызывает резкое уменьшение времени оседлой жизни частиц и приближение характера их движения к наблюдаемому в газе.
Следовательно, общим для конденсированного состояния, в каком находятся жидкость и кристаллы, является то, что энергия межчастичного взаимодействия в нем превалирует над энергией теплового движения. В газе — наоборот.
С учетом теплового движения частиц наличие или отсутствие порядка их расположения в кристаллах или жидкости следует рассматривать в зависимости от времени, в течение которого протекает процесс или производится наблюдение.
Для последующего сравнения рассмотрим сначала кристаллическую решетку. С целью изучения ближнего порядка в такой решетке выберем в ней небольшой объем металла. Вследствие лишь редких нарушений в расположении частиц при возникновении дефектов структуры, которыми можно пренебречь, все тепловое движение частиц в этом объеме сводится к колебаниям атомов возле регулярно расположенных узлов решетки. Поэтому, в зависимости от времени наблюдения или протекания процесса, необходимо учитывать возможность фиксации в такой решетке одной из двух структур:
– мгновенного порядка в расположении атомов в кристалле при среднем времени оседлой жизни атомов меньше периода колебания (τ<<τo)
– и среднего порядка при τ>>τo.
Мгновенный порядок, характерный для физических процессов, протекающих за время, меньшее периода колебания атомов (например, процесса рассеяния электронов), нерегулярный. Но в кристаллах, где амплитуда колебания атомов в решетке значительно меньше параметра решетки, степень нерегулярности в расположении атомов небольшая.
Средний порядок регулярный с характерной трансляционной повторяемостью. Он определяет большинство свойств кристаллов.
При рассмотрении жидкости, в которой вблизи температуры плавления τ значительно больше τo и значительную часть теплового движения частиц составляют перескоки из одного центра равновесия в другой, в зависимости от времени наблюдения t следует различать три типа структур по степени разупорядоченности частиц.
1. Мгновенную структуру без заметного упорядочения кристаллического типа для быстро протекающих процессов при t << τo. Такой характер структуры высокой степени неупорядоченности обусловлен тем, что в данных условиях фиксируется не среднее положение атомов в центрах их колебаний, а мгновенные положения. Вместе с тем размах нерегулярных тепловых колебаний атомов в жидкости сравним с межатомными расстояниями.
2. Среднюю структуру ближнего окружения произвольно выбранного атома, существующую при τ >> t >> τo. При таком времени в небольшой группе соседних атомов
(n ≈ 1 – 20) средние центры их колебания останутся практически неподвижными (как отмечалось, в кристаллах такое усреднение приводит к полному порядку). Возникает кратковременная квазикристаллическая структура небольших групп атомов, наиболее близкая к структуре твердых тел. Время существования такой упорядоченной структуры невелико — порядка t/n. С течением времени она изменяется.
3. При t > τ вследствие непрерывного изменения структуры ее квазикристалличность теряется. Остается лишь средняя структура радиального ближнего порядка. Именно эта структура, существенная для медленных и равновесных процессов, наблюдается на кривых, экспериментально полученных при определении рассеяния атомами рентгеновских лучей или нейтронов. Хотя за время их получения (десятки минут и часы) положение атомов меняется, среднестатистическое распределение их остается постоянным.
Из представлений о квазикристаллическом строении жидкости не следует, что в ней имеются кристаллы. Имеет место лишь упорядочение, которое удовлетворительно описывает модель строения, предложенная К.У. Стюартом. Он предположил, что упорядочение структуры сохраняется не только в ближайшем окружении некоторых атомов, названных в данный момент центральными, но сохраняется в пределах отдельных групп частиц, из которых состоит жидкость. Эти группы он назвал сиботаксисами (от греческого hibotos), что по смыслу соответствует используемому в настоящее время слову «кластер» англ. cluster -гроздь, группа. Кластеры не имеют четких границ. Они непрерывно появляются и исчезают. При этом атомы, принадлежащие к одному кластеру, переходят к другому, вновь возникающему. В местах соединений кластеров наблюдается разупорядочение их поверхностных слоев. Поэтому в каждый данный момент времени порядок в расположении частиц убывает от центра кластера к его поверхности. Время существования кластеров и их размеры зависят от состава жидкости и температуры.
Развивая теорию кластеров (сиботаксисов), Б.А. Баум с сотрудниками разработали квазихимическую модель строения жидких металлов. Эта модель представляет интерес для изучения тонкостей, в которых одновременно имеется несколько типов межчастичных взаимодействий, вызывающих появление микронеоднородности в их строении. К таким жидкостям относятся сталь и ферросплавы.
В отличие от описанной модели кластеров (сиботаксисов) в квазихимической модели учтены особенности силовых полей конкретных атомов жидкости, т.е. различная энергия взаимодействия атомов разной химической природы.в бинарных и более сложных системах. Это вызывает появление кластеров разных составов, строения и продолжительности существования. При этом учтены равноправность двух типов движения частиц — колебаний возле центров равновесия и перескоков между этими центрами, а также существенная роль межатомного притяжения в формировании конденсированного (жидкого, кристаллического) состояния.
Особое внимание неравноценности межатомных связей как причины неоднородности явилось для авторов модели основанием для названия ее квазихимической.
При описании квазихимической модели жидкости ее авторы, в качестве примера, рассматривают расплав железа с небольшим количеством атомов углерода. В таком расплаве существуют атомные связи Fe – Fe и Fe – С, причем последние сильнее первых. Это вызывает искажение электронной структуры атомов железной матрицы, охватывающей несколько координационных сфер вокруг атома примеси.
В результате примесь по сравнению с атомом матрицы имеет избыточный заряд. Внутри координационной сферы происходит перераспределение электронов. В том числе из недостроенных З- d -оболочек, допускающих образование направленных связей.
Модель жидкости, предложенная Дж. Берналом, основана на предположении, что различие между кристаллическим и жидким состояниями заключается в разных системах упаковки частиц, представляющих собой симметричные сферы. В кристаллах структура упорядоченная, регулярная и атомы находятся в строго фиксированных положениях. В жидкости, вследствие большего удельного объема (меньшей плотности), атомы не так жестко связаны между собой и находятся не в таких строго фиксированных положениях, как в кристаллах, т.е. структура нерегулярная.
Вследствие нефиксированности структуры жидкость можно переохладить ниже температуры кристаллизации. Этим она существенно отличается от кристаллов, которые перегреть выше температуры плавления невозможно.
В жидкости, как и в кристаллах, атомы между собой связаны. Но в кристаллах в результате теплового движения атомы колеблются возле некоторых центров равновесия, не меняя соседей (точнее говоря, редко их меняя). В жидкости же в результате такого движения часто происходит обмен соседями.
Таким образом, согласно Берналу, кристаллы имеют регулярную и связанную структуру, жидкости — нерегулярную и связанную структуру, газы — нерегулярную и несвязанную структуру.
Отмечая значительный вклад приведенных модельных представлений в развитие теорий жидкого состояния, следует признать, что они, все же, позволяют лишь весьма грубо описать свойства жидкости. Полное количественное описание свойств жидкости, представляющей собой систему огромного количества взаимодействующих между собой частиц, дает лишь использование методов статической физики.
 2020-01-14
2020-01-14 830
830








