Вначале необходимо приготовить оксалат бария, для чего к раствору 1,5 г оксалата натрия в 40 мл воды прилить раствор 2,5 г дигидрата хлорида бария в 6 мл воды. Выпавшие кристаллы отфильтровать на воронке Бюхнера и промыть несколько раз холодной водой [7].
Для получения триоксалатоферрата (III) калия в стакан емкостью 50-100 мл поместить 1,25 г сульфата железа (III), полученный оксалат бария, 1,5 г оксалата калия и 30 мл воды. Нагревать смесь в течение нескольких часов на водяной бане, поддерживая постоянный объем. После отделения осадка сульфата бария упарить фильтрат до объема 5 мл и охладить. Кристаллы триоксалатоферрата (III) калия отфильтровать, промыть небольшим количеством воды, а затем спиртом и высушить в вакуум-эксикаторе над серной кислотой. Препарат следует защищать от солнечного света, сушку лучше производить в темном месте.
Синтез хелатного комплекса
Приготовить раствор 4 г FeCl3 в 3,5 мл воды и раствор 9,3 г ЭДТА в 30 мл воды. Нагревать смесь в течение нескольких часов на плитке, затем дать остыть. Выпавшие кристаллы отфильтровать и высушить.
Выращивание кристалла берлинской лазури
При выращивании кристаллов необходимо учитывать, что если кристаллизация идет очень медленно, получается один большой кристалл если быстро - множество мелких кристаллов. Вещества, состоящие из одного кристалла, - монокристаллы.
Выращивают кристаллы разными способами: например, охлаждая насыщенный раствор. С понижением температуры растворимость большинства веществ уменьшается, и они, как говорят, выпадают в осадок. Сначала в растворе и на стенках сосуда появляются крошечные кристаллы-зародыши, а затем идет кристаллизация по всему объему раствора. Когда охлаждение медленное, а в растворе нет твердых примесей (скажем, пыли), зародышей образуется немного, и постепенно они превращаются в красивые кристаллы правильной формы [17].
Приготовить горячие насыщенные растворы FeCl3 и желтой кровяной соли. Растворы смешать в химическом стакане, выпавший осадок отфильтровать на воронке Бюхнера и поместить в чистую фильтровальную бумагу для получения затравки. Через неделю выбрать самый большой кристалл для затравки, обвязать его лавсановой нитью и поместить в маточный раствор. Через 14 дней были получены более крупные кристаллы.
Выращивание кристалла турнбулевой сини
Приготовить горячие насыщенные растворы FeSO4 и красной кровяной соли. Растворы смешать в химическом стакане, выпавший осадок отфильтровать на воронке Бюхнера и поместить в чистую фильтровальную бумагу для получения затравки. Через неделю выбрать самый большой кристалл для затравки, обвязать его лавсановой нитью и помещают в маточный раствор. Через 14 дней получают более крупный кристалл, в форме куба.
Идентификация
1) выращенные кристаллы имеют кубическую форму, что соответствует литературным данным. При рассматривании через микроскоп подтверждается кубическая структура кристалла.
2) окраска кубических кристаллов "турнбулевой сини"-"берлинской лазури" очень близка, что указывает на идентичность их структуры.
3) поскольку более устойчивым является цианидный комплекс Fe (II), то при образовании "турнбулевой сини" происходит валентный переход:
[Fe(CN)6]3- + Fe2+ = Fe3+ + [Fe(CN)6]4-
4) таким образом, осуществляется переход к более устойчивому цианидному комплексу Fe (II), т. е. к "берлинской лазури".
5) окраска полученного комплексного соединения железа (III) с ЭДТА соответствует литературным данным (желтая).
6) окраска полученного триоксалатоферрата (III) калия соответствует литературным данным (оранжево-коричневая).
Выводы
1) целью данной работы было установить кубическую структуру и идентичность "турнбулевой сини"-"берлинской лазури".
2) выращены кристаллы турнбулевой сини и берлинской лазури.
3) визуальный осмотр полученных кубических кристаллов свидетельствует о близости формы и окраски этих кристаллов, в том числе и при осмотре через микроскоп.
4) сделан вывод на основании литературных данных, что за счет валентного перехода FeII3[Fe(CN)6]2 превращается в Fe4[Fe(CN)6]3, т. е. процесс идет в направлении создания более устойчивого комплекса Fe (II).
5) получено 2,32 грамма триоксалатоферрата Fe(III), что составляет 85% от теоретического выхода
6) получен комплекс железа (III) с ЭДТА
Список литературы
1. Теория кристаллического поля.
http://www.college.ru/chemistry/course/content/theory.html - WWW, курс «Открытая Химия 2.5», 2007
2. Налбандян В. Б. Курс лекций по общей и неорганической химии. – WWW.: Химический факультет РГУ, 2002.
3. Гольданский В.И. Эффект Мёссбауэра. М.: Изд-во АН СССР, 1963;
4. Мёссбауэр Р.Л. Резонансное ядерное поглощение квантов в твердых телах без отдачи. Успехи физических наук, 1960, т. 72, вып. 4, с. 658–671.
5. И.В. Овчинников, Ю.Г. Галяметдинов. Магнитные жидкие кристаллы на основе координационных соединений. // Рос. хим. ж. (Ж. Рос. хим. об-ва им. Д.И. Менделеева). – 2001. – т. XLV, №3. – С. 74-79.
6. Леенсон И. Лазурь берлинская.
http://www.krugosvet.ru/articles/111/1011153/1011153a1.htm - WWW, энциклопедия «Кругосвет», 2007.
7. Практикум по неорганической химии: Учеб. пособие /под ред. В.П. Зломанова. – М.: Изд-во МГУ, 1994 – 320с.
8. Мелентьева Г.А. Фармацевтическая химия: В 2 т. – М.: “Высшая школа”, 1976. – Т.1 – 780 с.; Т. 2. – 827 с.
9. Беликов В.Г. Фармацевтическая химия: Учеб. для фармац. ин-тов и фак. мед. ин-тов. – М.: “Высшая школа”, 1985. – 768 с.
10. Максютина Н.П и др. Методы анализа лекарств, - Киев: Здоровье,1987
11. Пономарев В.Д. Аналитическая химия. – М.: Химия,1982
12. Крамаренко В.Ф. Токсикологическая химия. – Киев: Выща школа, 1989 г. - 447 с.
13. Справочник школьника по химии 8-11 класс. / под ред. Н.Е. Кузьменко, В.В. Еремина - М.: ООО «Издательский дом «ОНИКС 31 век»:ООО «Издательство «Мир и Образование», 2003. - 624 с.
14. Третьяков Ю.Д. Неорганическая химия. Химия элементов: учебник для вузов. В 2 книгах. - М.: Химия, 2001 - 472с.
15. Химическая энциклопедия. В 5 томах. Том 1. / под ред. Кнунянца И.Л., Зефирова Н.С., Кулова Н.Н. – М.: Большая российская энциклопедия, 1988 – 624 с.
16. В.П. Васильев. Комплексоны и комплексонаты. // Соросовский образовательный журнал. – 1996. – № 4. – с. 39-44.
17. Энциклопедия для детей. Том 17. Химия. / глав. ред. В. А. Володин. – М.: Аванта+, 2000. – 640 с.
18. Турова Н.Я., Неорганическая химия в таблицах. – М.: Высш. хим. колл. РАН, 1999. – 140 с.
Приложение
Параметры мёссбауэровских спектров:
1) Вероятность эффекта Мёссбауэра в общем случае записывается в виде [3]:

где < x2 >- средний квадрат смещения ядер в поглотителе из положения равновесия при твердотельных колебаниях в направлении пучка γ-квантов, l -длина волны γ-кванта. Величина <х2> зависит от фононного спектра твердого тела и его абсолютной температур Т. С ростом температуры <x2> растет, а f' падает. Вероятность эффекта Мёссбауэра падает также с уменьшением порядкового номера элемента, так как при этом сильно возрастает энергия первого возбужденного ядерного состояния Е0 и на ядрах легких элементов эффект не наблюдается. Пока он отмечен для 103 нуклидов 44 элементов.
Исследования зависимостей f' от температуры используют при установлении координационных чисел, для определения фазовых переходов и изучения характерных динамических параметров твердых тел до и после фазового перехода. Особенно эффективен этот метод в области низких и сверхнизких температур и для некристаллических веществ, когда, как правило, затруднены рентгеноструктурные исследования.
Площади спектральных линий, наблюдаемые экспериментально, пропорциональны концентрации исследуемого атома в образце при фиксированной температуре. На измерении этих площадей основано применение мессбауэровской спектрометрии для решения некоторых задач аналитической химии и фазового анализа вещества [4].
2)Энергетический сдвиг спектра излучения относительно спектра поглощения вычисляется как сумма температурного сдвига dT и изомерного сдвига d.
Температурный (доплеровский) сдвиг линии возникает вследствие изменения энергии γ-квантов при их излучении и поглощении в результате релятивистского изменения массы излучающих и поглощающих ядер соответственно ("красное смещение"). Например, для 57Fe ожидаемое смещение при переходе от комнатной температуры к Т → 0 близко к естественной ширине линии. Поскольку различие в температурах источника и поглотителя более 300 К встречается редко, вклад dT мал и обычно маскируется более сильным сдвигом, который от температуры не зависит.
Для тождественных ядер в отсутствии электрических и магнитных полей спектр представляет собой одиночную линию (рис. 7, а).
Изомерный (химический) сдвиг связан с электрическим монопольным кулоновским взаимодействием между ядром с зарядовым радиусом r и электронами атома [3]:

где е -элементарный заряд, Z -атомный номер, ∆ <r2> -изменение среднего квадрата радиуса ядра при его возбуждении (ядерный параметр),  -квадраты волновой функции s-электронов на ядре в поглотителе (а) и источнике (s) γ-излучения соответственно (электронные параметры). Последние представляют большой интерес для химии. Вследствие изменения заселенности s-состояний или экранирования s-электронов валентными р-, d-, f-электронами изменяются значения
-квадраты волновой функции s-электронов на ядре в поглотителе (а) и источнике (s) γ-излучения соответственно (электронные параметры). Последние представляют большой интерес для химии. Вследствие изменения заселенности s-состояний или экранирования s-электронов валентными р-, d-, f-электронами изменяются значения  , измеряемые экспериментально по изомерным сдвигам. Например, в комплексах железа, в зависимости от характера участия d-электронов в химической связи (координации, степени электронной делокализации), максимум резонансного поглощения сдвигается на величину δ относительно резонансной линии поглощения (испускания) при u = 0 (рис. 7, б) [4].
, измеряемые экспериментально по изомерным сдвигам. Например, в комплексах железа, в зависимости от характера участия d-электронов в химической связи (координации, степени электронной делокализации), максимум резонансного поглощения сдвигается на величину δ относительно резонансной линии поглощения (испускания) при u = 0 (рис. 7, б) [4].
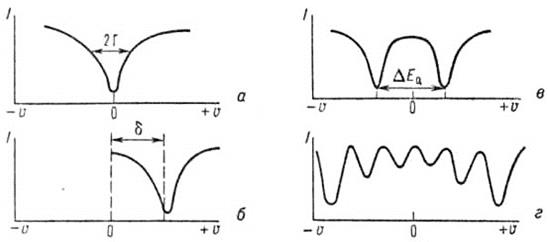
Рис. 7. Схематическое изображение спектров мёссбауэровского резонансного поглощения γ-квантов: I-интенсивность потока γ-квантов, прошедших через поглотитель, u -скорость движения источника γ-квантов относительно поглотителя; а - резонансная линия при u = 0; б, в, г - соответственно изомерный сдвиг (d), квадрупольный дублет (DEQ), магнитная сверхтонкая структура для ядер 57Fe.
Значения δ отсчитывают от стандарта, который принят для спектроскопии данного ядра. При этом выбирают соединения, стабильное химически и дающее простой мёссбауэровский спектр. Например, в случае 119Sn δ отсчитывается от значения, соответствующего соединению 119SnO2, а для 57Fe в качестве стандарта используют нитропруссид натрия.
По величине химического сдвига можно судить о различии в характере химических связей. С помощью мессбауэровской спектроскопии изучено большое число соединений, составлены номограммы, с помощью которые по δ определяют валентность элемента в неизученных соединениях. В зависимости от конфигурации валентных электронных оболочек атомов и ионов могут быть проведены квантовомеханические расчеты 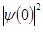 для свободных атомов. Однако для атомов в твердых телах эти расчеты носят пока полуколичественный характер.
для свободных атомов. Однако для атомов в твердых телах эти расчеты носят пока полуколичественный характер.
3) Электрическое квадрупольное взаимодействие возникает вследствие взаимодействия квадрупольного момента ядра Q с градиентом электрического поля q, создаваемого электронной оболочкой атома или кристаллической решеткой твердого тела, в результате чего в спектрах поглощения наблюдается не одна, а несколько линий. Если спин ядра I > 1/2, a q ≠ 0, это взаимодействие приводит к "расщеплению" ядерного энергетического уровня на подуровни, расстояние между которыми определяется, например, для ядра 57Fe выражением [4]:
 , где
, где 
qxx, qyy, qzz - градиенты электрического поля на ядре вдоль соответствующих осей. Величина q характеризует отклонение распределения электронного заряда от сферического.
 2020-01-14
2020-01-14 637
637







