Термическая перегруппировка 2-карена (31) и его производных была первым примером превращений, которые впоследствии стали называть 1,5-гомодиенильным сдвигом.87
Хорошо известно, что при температурах выше 330°С винилциклопропан превращается в циклопентен; реакция протекает путем гомолитического разрыва связи, изомеризации образовавшегося дирадикала и последующей рекомбинации.88 Энергия активации этой перегруппировки довольно высока и составляет 208 кДж•моль-1 (см.89).
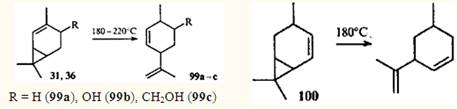
Однако 2-карен и его производные, молекулы которых содержат винилциклопропановый фрагмент, претерпевают перегруппировку уже при 180°С, образуя при этом соответствующие производные транс -изолимонена 99а-с. 90-91 Подобным же образом реагирует 4-карен (100).92

Это превращение обусловлено особенностями строения производных 2- и 4-карена: подобно тому, как в цис -1,3-диеновых системах возможен 1,5-диенильный сдвиг водорода, в соединениях ряда карана, имеющих винилциклопропановый фрагмент, возможен 1,5-гомодиенильный сдвиг. Реакция протекает через шестиэлектронное переходное состояние и подчиняется правилам отбора для термических водородных сдвигов.56 Гомолитического разрыва углерод-углеродной связи не происходит, так как энергия активации 1,5-гомодиенильного сдвига значительно ниже, чем энергия винилциклопропановой перегруппировки; в случае 2-карена она составляет 118 кДж•моль-1 (см.91). Необходимое условие осуществления 1,5-сдвига — эндо -ориентация участвующих в образовании ПС связи С—Н и винильной группы.93 Это — единственное стереохимическое требование для термической перегруппировки цис -1-метил-2-винилциклопропана, расположение заместителей в молекуле которого не вносит дополнительного напряжения. Это требование выполняется и для молекулы 2-карена (31), но из-за того, что двойная связь входит в шестичленный цикл, она отклоняется от направления, оптимального для сопряжения с ЦПК и образования ПС. Расстояние между С(3) и атомом водорода при С(8) в конформации "плоского кресла" составляет ~3.1 Å.38 Это означает, что молекула 2-карена (31) при нагревании должна сначала изменить конформацию (при этом расстояние С(3)—Н(8) уменьшается до 2.З Å), и только затем может произойти 1,5-гомодиенильный сдвиг.
Природа заместителя в положении 4 может влиять на энергию активации конформационного перехода, но даже объемные заместители не препятствуют 1,5-сдвигу; правда термическая перегруппировка таких соединений требует более высокой температуры.94

α-Туйен (101), молекула которого также содержит винилциклопропановый фрагмент, при нагревании выше 300°С остается неизменным. Однако эксперименты с дейтериевой меткой показали, что в действительности происходит вырожденная винилциклопропановая перегруппировка. В данном случае ПС, необходимое для осуществления 1,5-гомодиенильного сдвига, является труднодостижимым: расстояние между D(4) и С(5) или С(3) составляет ~ 2.8 Å.95

Следует отметить, что благодаря геометрии молекул именно карановые структуры оказались подходящими моделями для изучения 1,5-гомодиенильного сдвига. В реакциях термической изомеризации терпеноидов с бицикло[4.1.0]-гепт-2-еновым скелетом 1,5-гомодиенильный сдвиг происходит регио- и стереоспецифично, что позволяет, например, синтезировать новые кислородсодержащие терпеноиды из производных 2-карена.96
Не всегда наличие эндо -ориентированного винилциклопропанового фрагмента и подходящей связи С—Н в соединениях каранового ряда означает возможность термического 1,5-водородного сдвига. Так, при нагревании карадиена 77 в бензоле в интервале температур 120-190°С основным (при сравнительно низких температурах — единственным) продуктом его превращения был триен 61. 97 При повышении температуры до 170 - 190°С в небольших количествах (до 3 %) образовывались также п - и м -цимолы.
Казалось бы, наиболее реальным процессом в описываемых условиях должен быть 1,5-гомодиенильный сдвиг: винильная группа и одна из связей С(8)—Н имеют эндо - ориентацию, расстояние С(4)—Н(8) составляет ~2.2Å, т.е. легко достижимо идеальное ПС 1,5-сдвига, рассчитанное теоретически.93 Однако продуктом такого превращения должен быть м -мента-1(7),4,8-триен, который в действительности не образуется. Винилциклопропановая перегруппировка при этих температурах также невозможна, так как для радикальной реакции они недостаточно высоки. Можно предположить, что за скелетную перегруппировку ответственна валентная таутомерия. Тогда термическая изомеризация 77 → 61 фактически сводится к превращению трансоидного диена 77 в цисоидный диен 58. Формально — это 1,3-сигматропный сдвиг.

Принято считать, что некатализируемый 1,3-сдвиг водорода в термических реакциях не происходит, так как переходное состояние разрешенного антараповерхностного сдвига является труднодостижимым из-за больших угловых напряжений в пропиленовом фрагменте.98 Супраповерхностный сдвиг, который вполне мог бы реализоваться с пространственной точки зрения, запрещен правилами сохранения орбитальной симметрии. Однако расчет ab initio 1,3-сдвига в пропене показал, что запрещенный супраповерхностный перенос водорода требует меньшей энергии активации, чем разрешенный антараповерхностпый.99 Для объяснения этого неожиданного результата была привлечена гипотеза о контроле орбиталью, лежащей ниже граничной.100 Эта гипотеза лежит в основе предположения об осуществлении 1,3-сдвига в молекуле диена 77.
К исследованию механизма термической изомеризации карадиена 77 были привлечены кинетические исследования.97 Превращения углеводорода 77 в триен 61 — последовательность двух согласованных реакций, причем первая (предполагаемый 1,3-сдвиг) по совершенно очевидным соображениям является лимитирующей. Кинетические исследования показали, что эта стадия описывается уравнением первого порядка. Определенная из экспериментальных данных энергия активации составляет 112 кДж•моль-1, что близко к расчетной величине энергии активации антараповерхностного 1,3-сдвига (115 кДж•моль-1).99 На то, что 1,3-сдвиг возможен в этой реакции, указывает высокое отрицательное значение энтропии активации, равное 96 кДж•моль-1•град-1 (—23 э.е.). Сравнение этой величины с соответствующим параметром 1,5-сдвига (-8 ÷ -16 э.е.) показывает, что переходное состояние термической перегруппировки карадиена 77 является высокоупорядоченным и участвующие атомы связаны очень жестко. Энергия активации 1,5-сдвига в 2-карене (31) (118 кДж•моль-1)91 несколько выше, чем энергия активации термической изомеризации диена 78, и это может быть объяснением, почему в данном случае не осуществляется 1,5-сдвиг.
Особенно интересна термическая перегруппировка Берсона - Вилькотта.47 Формально она представляет собой перемещение метальной группы по всем возможным положениям триеновой системы в молекуле углеводорода 61. Тем не менее её следует рассматривать в ряду карановых перегруппировок, Так как в действительности осуществляется не 1,3- или 1,5-алкильпый сдвиг, а 1,5-сдвиг диметилметиленовой группы в карадиеновом таутомере 58, что было показано с помощью дейтериевых меток.
Эта частная реакция послужила толчком для развития экспериментальных и теоретических исследований, которые значительно расширили и в чем-то изменили классические представления о сигматропных реакциях. Триен 61 оказался прекрасной моделью для этих исследований, так как перегруппировка осуществляется только при наличии гем -диметильной группы: в отсутствие геминальных заместителей циклогептатриен претерпевает 1,5-сдвиг водорода уже при температурах выше 100°С.101 Присутствие третьей метильной группы, которая "гуляет" по триеновой системе семичленного цикла, позволило обнаружить эту перегруппировку ("walk rearragement").

Следует отметить, что механизм сдвига не позволяет считать перегруппировку гептатриена 61 в полном смысле согласованной, ибо она протекает через дирадикальный интермедиат при температурах ~ 400°С. В процессе перегруппировки происходит перемещение циклопропановой связи, которая в исходной молекуле не является σ-связью, что тоже не позволяет считать перегруппировку сигматропной. Тем не менее довольно долго полагали, что перегруппировка триена 61 полностью отвечает правилам отбора для согласованных сигматроппых миграций алкильных групп, т.е. протекает как супраповерхностная с сохранном конфигурации мигрирующей группы. Изящные работы Клернера с соавт.102-104 полностью опровергли эти представления: заменив одну из метильных групп алкоксикарбонильной, нитрильной или алкоксиалкильной, он доказал, что перегруппировка протекает с обращением конфигурации, т.е. по "запрещенному" пути.
Недавно в вышедших почти одновременно теоретических работах 105,106 это явление было объяснено на основании расчетов ab initio. В случае незамещенного норкарадиена 102 в дирадикальном ПС А запрещенного термического 1.5-алкильного сдвига метиленовая группа с неспаренным электроном находится несколько дальше от шестичленного кольца, чем в ПС В разрешенного сдвига, что понижает энергию ПС запрещенного сдвига на ~ 4 кДж•моль-1 (см.105).

Переходные состояния C и D для 1,5-сдвига в цис - (103) и транс -7-циано-7-метилноркарадиенах (104), протекающего с обращением конфигурации (и поэтому запрещенного), на 12 и 13 кДж•моль-1 соответственно более предпочтительны, чем ПС Е аналогичного сдвига с сохранением конфигурации (и поэтому разрешенного). Расстояние между атомами водорода метильной группы и цикла в запрещенных ПС С и D на 0.12 и 0.37Å меньше, чем в разрешенном ПС Е. 106

Можно сделать вывод, что при протекании сигматропной перегруппировки через дирадикальный интермедиат стерический фактор может доминировать над электронным, что и приводит к нарушению фундаментальных правил сохранения орбитальной симметрии. Исследования, приведшие к этому поразительному результату, были начаты с изучения терпеноидов — триеиа 61 и его валентного таутомера диена 58.
 2020-01-14
2020-01-14 256
256








