Спектры излучения и поглощения атомов и молекул.
Дискретность (иначе – прерывистость) некоторых физических характеристик атомов и молекул.
В начале ХХ в. считалось, что атом имеет «планетарную» структуру – заряженное ядро и движущиеся вокруг него по орбитам электроны. В классической физике движение по орбите – это движение с ускорением (центростремительным). Известно, что заряженная частица, т.е. электрон, движущаяся с ускорением, излучает
электромагнитные волны и, следовательно, теряет энергию. Итог – падение электрона на ядро. По оценкам этот процесс реализуется за время 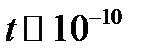 с. Это и будет примерное время существования атома как физической системы из ядра и электронов. Однако из эксперимента известно, что атом – устойчивая система!
с. Это и будет примерное время существования атома как физической системы из ядра и электронов. Однако из эксперимента известно, что атом – устойчивая система!
2.В процессе падения на ядро по законам классической физики электрон должен непрерывно излучать энергию. Следовательно, спектр излучения атома должен быть непрерывным. Однако из эксперимента известно, что у атомов спектры линейчатые. Пример – атом водорода. У него положение линий в спектре испускания (и поглощения) электромагнитного излучения описывается «обобщенной формулой Бальмера»:
 .
.
Здесь m принимает значения 1, 2, 3, …, при заданном m n= m +1, m +2, m +3 …; λ – длина волны излучения, а индексы внизу указывают, к какой серии относится линия в спектре: m =1 и n =2, 3, 4, … - серия Лаймена, m =2 и n =3, 4, 5, … - серия Бальмера и т.д.; наконец, R =1.097 ۰ 107 м -1 – постоянная Ридберга

Экспериментально было показано, что некоторые физические характеристики атомов являются дискретными. Так, в опытах Франка-Герца была доказана дискретность величины энергии, которую могут принимать атомы ртути при столкновениях с электронами. В экспериментах Штерна-Герлаха была продемонстрирована дискретность проекции момента количества движения атома на заданное направление, т.е. пространственное квантование у атомов.


 2020-04-12
2020-04-12 363
363








