Этот метод позволяет рассчитать стандартную теплоту образования, абсолютное значение энтропии в стандартном состоянии и коэффициенты температурной зависимости теплоемкости.
1) Выбирают вещество, лежащее в основе рассматриваемого соединения.
2) Строят полный скелет соединения, проводя последовательные замещения водородного атома на группу —СН3.
3) Вводят группы —СН3, которые впоследствии будут замещены на соответствующие функциональные группы (ОН, NO2, NH2 и т.д.)
4) Заменяют ординарные связи сложными (С=С, С≡С)
Если есть необходимость, то вводят дополнительные поправки.
После чего все поправки суммируются:


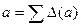
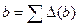
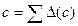
Для определения соответствующих поправок необходимо знать так называемые типовые числа того атома углерода, у которого проводится замена (атом типа А) и соседнего с ним менее гидрированного углеродного атома (атом типа В). Типовые числа атомов углерода определяют по числу имеющихся у атома углерода атомов водорода
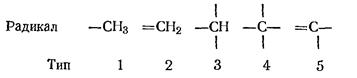
Тип 5 относится к углеродному атому бензольного или нафталинового кольца.
Более подробно описано в книге «Расчёты химических равновесий» (авторы Казанская А.С., Скобло В.Н.)
Пример: рассчитать теплоту образования, энтропию образования и коэффициенты температурной зависимости теплоемкости газообразного ацетона
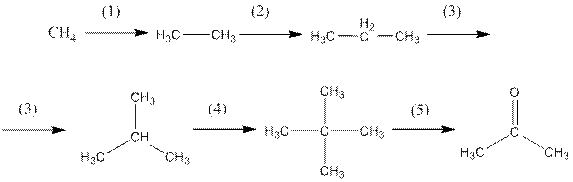
1) первичное замещение в метане (метан→этан)
2) вторичное замещение А=1, B=1 (этан→пропан)
3) вторичное замещение А=2, B=1 (пропан→изобутан)
4) вторичное замещение А=3, B=1(изобутан→неопентан)
5) замещение двух метильных групп на карбонильный кислород =О (в кетоне)
Сведем поправки [Казанская А.С., Скобло В.Н. Расчёты химических равновесий. М.: Высшая школа,1974.-288с.]. в таблицу и просуммируем их
| Замещение | Δ(ΔН) | Δ(S) | Δ(a) | Δ(b)·103 | Δ(c) ·106 |
| Основная группа (метан) | -17,89 | 44,5 | 3,79 | 16,62 | -3,24 |
| (1) | -2,5 | 10,35 | -2 | 23,2 | -9,12 |
| (2) | -4,75 | 10,1 | 0,49 | 22,04 | -8,96 |
| (3) | -6,31 | 5,57 | -0,3 | 21,74 | -8,77 |
| (4) | -8,22 | 2,81 | -0,28 | 24,21 | -10,49 |
| (5) | -13,2 | -2,4 | 5,02 | -66,08 | 30,21 |
| Σ | -52,87 | 70,93 | 6,72 | 41,73 | -10,37 |
Переведем полученные величины в джоули и сравним со справочными данными [Краткий справочник физико-химических величин / под ред. А. А. Равделя, А. М. Пономарёвой. – 10-е изд., испр. и дополн. – СПб.: Иван Фёдоров, 2003. – 240 с.].
| Замещение | Δ(ΔН) | Δ(S) | Δ(a) | Δ(b)·103 | Δ(c) ·106 |
| Σ (Дж) | -221,53 | 283,72 | 28,16 | 174,85 | -43,45 |
| Из справочника | -217,57 | 294,93 | 22,47 | 201,8 | -63,5 |
Дополнительно проверим сходимость теплоемкости при произвольной температуре:
1) По справочным данным:

2) По расчетным значениям:
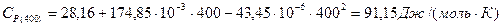
 2020-04-12
2020-04-12 1038
1038








