Теоретична частина.
Хімічний зв'язок - це така взаємодія між атомами або молекулами, що призводить до створення з них стабільних чи метастабільних хімічних сполук. Такими сполуками можуть бути як молекули, так і конденсовані системи. Природа зв'язку (те, завдяки чому і як він виникає) є об'єктом багаторазових обговорень і в науковій, і в навчальній літературі.
Існує декілька концепцій у теорії хімічного зв'язку.
Маллікен запропонував наступну концепцію природи хімічного зв'язку: хімічний зв'язок можна розглядати як суму електростатичних та орбітальних взаємодій. Повну енергію хімічної частки можна розрахувати як:
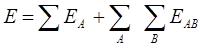

Також Маллікен запропонував концепцію орбітального аналізу хімічних зв'язків - принцип відповідності атомних орбіталей. Згідно із цим принципом, s- і р-орбіталі бувають двох типів. Якщо АО однотипні, то їх комбінація зв'язуюча, а якщо не однотипні - антизв'язуюча. Тип АО визначається знаком перед варіаційним коефіцієнтом с у хвильовому рівнянні.
Мета: освоєння методики розрахунку енергії хімічного зв’язку в наближенні орбітально-електростатичної концепції Маллікена.
Завдання до роботи.
.Енергію О-О зв’язку та її складові компоненти конформерів пероксикислот занести в таблицю.
. Обгрунтувати вклад електростатичних та орбітальних взаємодій в енергію зв’язку -О-О-.
. Провести аналіз впливу природи замісника і конформації пероксикислот на енергію -О-О- зв’язку.
Таблиця 8. Енергетика О1-О2 зв’язку пероксикислот.
| ЕАВ, еВ | (OH)C6H4C(O)OOH | (CH3)(OH)C6H3C(O)OOH | ||
| Конформер | Конформер | |||
| А | Б | А | Б | |
| ЕJAB | -9.989 | -10.067 | -10.398 | -10.063 |
| ЕKAB | -4.434 | -4.415 | -4.487 | -4.413 |
| Еe,eAB | 301.601 | 303.374 | 302.746 | 303.414 |
| Еe,N | -594.110 | -596.578 | -597.117 | -596.604 |
| ЕN,NAB | 297.716 | 298.526 | 299.878 | 298.511 |
| ЕCAB | 5.207 | 5.323 | 5.507 | 5.322 |
| ЕАВ | -9.216 | -9.159 | -9.378 | -9.155 |
Висновки. Виконавши цю роботу, мною були розраховані енергії хімічного зв’язку пероксикислот в наближенні орбітально-електростатичної концепції Маллікена. Як ми можемо бачити з данних, котрі наведені в таблиці 8, конформація пероксикислот суттєво не впливає на значення енергії та її складових.
Енергія дисоціації пероксикислот
Теоретична частина.
Міцність хімічного зв'язку визначається енергією, яку необхідно витратити, щоб розірвати цей зв'язок. Така енергія зветься енергією дисоціації.
Розрив зв'язку може бути здійснений шляхом гомолізу або гетеролізу.
Гомоліз - розрив зв'язку, який полягає в розпаруванні електронів, що його утворюють, кожен з електронів далі залишається на одному з відокремлених фрагментів.
Гетероліз - розрив зв'язку, що супроводжується утворенням йонних частинок і відбувається таким чином, що пара електронів, яка утворювала зв'язок, залишається на одному з фрагментів.
Мета. Освоєння методики розрахунку енергії дисоціації хімічного зв’язку.
Завдання до роботи.
1. Розрахувати енергію більш стабільного конформера пероксикислот.
2. Розрахувати енергію RС(О)ОО . і RС(О)ОО - в рівноважному стані.
3. Розрахувати енергію Н . -радікала і Н+ - катіона.
Таблиця 9. Стандартні ентальпії утворення пероксикислот та продуктів їх дисоціації
| Об’єкт | ∆Hf0, ккал/моль | Об’єкт | ∆Hf0, ккал/моль |
| (ОН)C6H4C(O)OOH | -87.202 | (CH3)(OH)C6H3C(O)OOH | -95.702 |
| Н. | 52.102 | Н. | 52.102 |
| (ОН)C6H4C(O)OO· | -41.321 | (CH3)(OH)C6H3C(O)OO· | -49.965 |
| Н+ | 353.580 | Н+ | 353.580 |
| (ОН)C6H4C(O)OO- | -89.495 | (CH3)(OH)C6H3C(O)OO- | -109.512 |

Для (ОН)C6H4C(O)OOH:
D1 = (353.580 + (-89.495)) - (-87.202) = 351.287 ккал/моль
Для (CH3)(OH)C6H3C(O)OOH:
D2 = (353.580 + (-109.512)) - (-95.702) = 339.77 ккал/моль
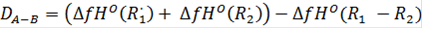
Для (ОН)C6H4C(O)OOH:
D3 = (52.102 + (- 41.321)) - (-87.202) = 97.983 ккал/моль
Для (CH3)(OH)C6H3C(O)OOH:
D4 = (52.102 + (-49.965)) - (-95.702) = 97.839 ккал/моль
Висновки. Виконавши цю роботу мною були розраховані енергії дисоціацій пероксикислот. Дивлячись на отримані значення енергій можна стверджувати, що розрив зв'язку, здійснений шляхом гомолізу, є енергетично вигіднішим, ніж шляхом гетеролізу. Тому, скоріше за все, пероксикислоти будуть дисоціювати з утворенням радикалів.
 2020-04-20
2020-04-20 142
142








