Ряд напряжения металлов. Гальванические элементы
3.1.1 Рассчитайте электродный потенциал Bi в 0,01 м растворе его соли.
Значение электродного потенциала рассчитаем на основании уравнения Нернста:
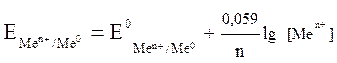 .
.
Значение стандартного электродного потенциала Е0 висмута возьмем из ряда СЭП (+0,21 В), n – количество электронов, участвующих в процессе, равно заряду иона висмута «3+», концентрация ионов металла указана в условии задачи – 0,01 моль/л. Подставляем данные в формулу и производим расчет:
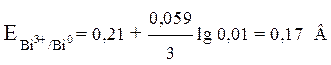 .
.
3.1.2 Какой гальванический элемент называется концентрационным? Составьте схему, напишите электронные уравнения электродных процессов и вычислите ЭДС гальванического элемента, состоящего из серебряных электродов, опущенных: первый в 0,01 Н, а второй в 0,1 Н растворы AgNO3.
Гальванический элемент, составленный из одинаковых электродов, погруженных в растворы одного и того же электролита, различающихся только концентрацией, называется концентрационным. При этом электрод, помещенный в более разбавленный раствор (с меньшей концентрацией ионов в растворе), играет роль анода, а электрод в более концентрированном растворе (с большей концентрацией ионов металла в растворе) – роль катода.
Схема работы данного гальванического элемента:
 |
Ag AgNO3 (0,01 н) AgNO3 (0,1 н) Ag.
Электродные процессы:
А) Ag0 – 1ē = Ag+ – процесс окисления;
К) Ag+ + 1ē = Ag0 – процесс восстановления.
Величина электродного потенциала отдельно взятого электрода рассчитывается по уравнению Нернста. Значение электродного потенциала серебра возьмем из ряда СЭП (+0,8 В), количество электронов, участвующих в процессе, равно заряду иона серебра «+1».
По уравнению Нернста найдем электродные потенциалы металла анода и катода:
| EК = 0,8 + | 0,059 | l g 0,1 = 0,741 В; |
| 1 |
| EА = 0,8 + | 0,059 | l g 0,01 = 0,682 В. |
| 1 |
В данном случае будем считать, что СН = [Men+], поскольку фактор эквивалентности нитрата серебра равен 1.
ЭДС гальванического элемента рассчитаем по формуле
ЭДС = ЕК – ЕА = 0,741 – 0,682 = 0,059 В.
 2020-05-21
2020-05-21 407
407








