КйЩечный сок-3 л
-
 |


|

Составная часть
коллоодов
Трансцелгюпярная (1-3%) Цереброспинальная жидкость Внутриглазная жидкость Другие жидкости
Рис. 4.2. Суточный баланс воды в организме (А) и виды воды
в организме (Б)
Вода перемещается между различными отделами жидких сред организма под воздействием сил гидростатического и осмотического давления. В связи с тем, что плазматические мембраны клеток хорошо проницаемы для воды, изменение осмолярности внутриклеточной или внеклеточной жидкости приводит к ее перемещению путем осмоса из области менее низкой концентрации растворенного вещества в область его более высокой концентрации.
Внутриклеточная и внеклеточная жидкости электронейтральны и осмотически равновесны, хотя возможны временные изменения их осмолярности. В норме осмолярность как внутриклеточной, так и внеклеточной жидкости составляет 290 мосмоль/кг Н,О.
Методы определения объема жидких фаз организма. Существенное значение в современных клинических исследованиях имеет метод разведения радиоизотопных препаратов по всему водному сектору организма (окись трития) или по внеклеточному пространству (изотоп 82Вг).
Общее количество воды в организме измеряют по расщеплению тяжелой воды (D,O), трития или антипирина, которые легко диффундируют через клеточные мембраны.
Для определения объемов отдельных жидких фаз тела используют метод разведения, основанный на том, что в кровь вводят вещество, свободно распределяющееся только в одной или нескольких жидких фазах.
Для определения объема плазмы крови используют краски — Эванс синий или некоторые «тест-вещества» — изотопы, связанные с белками плазмы (например, меченый альбумин), которые остаются в пределах сосудистого русла в течение всего времени наблюдения.
Для определения объема внеклеточной жидкости используют вешества, проникающие в клетку: инулин, сахарозу, маннитол, тиосульфат и изотопы натрия и хлора.
Объем внутриклеточной жидкости недоступен для прямого измерения и определяется по разности объемов общей воды тела и объема внеклеточной жидкости.
Количество интерстициальной жидкости представляет разность между объемами внеклеточной жидкости и плазмы крови.
Внутриклеточная жидкость — жидкая фаза цитоплазмы и ядра, вода которой составляет примерно 30—40 % массы тела. Посредством внутриклеточной жидкости осуществляются процессы клеточного метаболизма и поддерживается постоянство клеточного состава различных органов. В состав внутриклеточной жидкости входят вода, неорганические вещества, растворимые газы, проме
жуточные продукты обмена углеводов, липидов, белков, нуклеиновых кислот, свободные макромолекулы (белки, РНК), ряд ферментов. Активная реакция (pH) внутриклеточной жидкости — 7,0. Состав внутриклеточной жидкости зависит от типа клеток и тканей, стадии их развития, физиологического состояния и меняется при патологии.
В отличие от внеклеточной жидкости концентрация натрия во внутриклеточной жидкости очень низкая, тогда как ионы К" удерживаются за счет действия Na'.K’-АТФазы. Основные внутриклеточные анионы — фосфаты и органические анионы. На рис. 4.3 приведена сравнительная характеристика внеклеточной и внутриклеточной жидкости.
Внеклеточная жидкость составляет 20 % массы тела. Она имеет несколько фаз.
Плазма — жидкое межклеточное вещество крови, в котором находятся белки и форменные элементы — эритроциты, тромбоциты и лейкоциты. Содержание белка в плазме — около 70 г/л, а на долю «чистой» воды приходится 93 % объема. Электролитный состав плазмы является важным показателем метаболических процессов в организме.
 | |||
 | |||
| ||||
| ||||
Интерстициальная (тканевая, межклеточная) жидкость, составляющая 15 % массы тела, является непосредственной питательной средой органов (микросреда). Состав и свойства микросреды специфичны для отдельных органов и соответствуют их структурно-функциональным особенностям. Тканевая жидкость по составу близка к плазме крови, но содержит значительно меньше белка (10—30 г/л), метаболитов, ферментов; иное, чем плазма, количество ионов и витаминов.
Лимфа — составная часть тканевой жидкости. Она переносит крупномолекулярные белки, частично жиры и углеводы из тканевой жидкости, куда они попадают из клеток, в кровь.
Лимфатические капилляры выполняют также концентрационную функцию, поскольку реабсорбируют воду в области венозного конца капилляра.
Основные ионы внеклеточной жидкости — натрий, а также анионы хлора и гидрокарбоната. Состав интерстициальной жидкости и плазмы крови очень схож благодаря эндотелию капилляров, разделяющему эти отделы, и проницаемости его для мелких ионов. Основное отличие интерстициальной жидкости от плазмы крови заключается в том, что плазма содержит значительно большее количество белка.
По определению К. Бернара, тканевая жидкость — это «внутреннее море», в котором активно живут клетки. Полагают, что интерстициальная жидкость представляет собой не свободно перемещающуюся воду, а гель, удерживающий ее в фиксированном состоянии. Основу геля составляют гликозаминогликаны, в частности гиалуроновая кислота. Благодаря свойству относительной статичности тканевая жидкость обеспечивает концентрацию транспортируемых веществ в пунктах их назначения, не позволяя им растекаться по организму.
Водно-электролитный баланс. В случае, когда количество поступающей в организм воды и солей равно их выделению из организма, говорят о водно-электролитном балансе.
При положительном водно-электролитном балансе количество воды и солей, поступающих в организм, превышает их количество, выделяемое из организма.
При отрицательном водно-электролитном балансе количество воды и солей, выделяемых из организма, превышает их количество, поступающее в организм.
Водно-электролитный баланс у человека рассчитывают по суточному потреблению и выделению воды и электролитов.
Роль соединительной ткани в водно-ионном балансе. Соединительную ткань образуют вырабатываемые фибробластами коллагеновые волокна и находящиеся между ними в определенных информационных состояниях молекулы протеиногликанов и гликопротеинов. Протеиногликаны и гликопротеины за счет конформационных свойств их молекул обладают способностью удерживать молекулы воды, определяя тем самым процессы гидратации соединительной ткани. Эти же молекулы активно отдают воду, определяя и процессы дегидратации соединительной ткани. Большая часть жидкости, поступающей в кровь из кишечника, образует слабый гель с гликозаминогликанами соединительной ткани, главным образом с гиалуроновой кислотой. Этот гель ненасытен, его давление на 6 мм рт. ст. ниже атмосферного. Вследствие этого он активно связывается с водой. Вода распределяется пропорционально между тканевой жидкостью и плазмой крови.
Процессы гидратации и дегидратации соединительной ткани регулируются гормонами (например, кортизоном) и биологически активными веществами, среди которых ведущую роль играют витамины, простагландины и олигопептиды. Яды змей и пчел содержат большое количество олигопептидов: апамин, МСД-пептид, тертиапин и др. При поступлении этих ядов в организм наблюдается набухание (гидратация) соединительной ткани, что внешне проявляется в виде отека.
В процессах гидратации и дегидратации соединительной ткани участвуют различные ферменты, среди которых наиболее активна гиалуронидаза.
Механизм действия гиалуронидазы. Гиалуронидаза катализирует гидролиз 0-связей входящей в состав соединительной ткани гиалуроновой кислоты и понижает вязкость ее раствора. Вследствие этого вода из околоклеточного пространства устремляется в соединительную ткань. Здесь она может накапливаться, что приводит к гидратации соединительной ткани, или с помощью специальных ферментов выводиться в полости органов.
Движение жидких сред в организме ограничено биологическими барьерами.
4.1.2. Барьерные функции
Внешние барьеры отделяют клетки, органы и ткани от окружающей среды. Внутренние барьеры разделяют клетки, органы, ткани и собственно кровь.
К внешним барьерам относятся: кожа, органы дыхания, органы пищеварения, печень, почки. Внешние барьеры регулируют обмен веществ между организмом и окружающей средой, предохраняют его от повреждающих физических и химических воздействий, препятствуют проникновению в организм токсинов, бактерий, ядов. Они также способствуют выведению из организма конечных продуктов метаболизма.
Внутренние барьеры, называемые гистогематическими (от греч. histos — ткань и haima — кровь), регулируют взаимоотношения между кровью и внутренней средой органа. Основоположницей учения о гистогематических барьерах является Л. С. Штерн.
Внутренние барьеры регулируют как поступление из крови в органы и ткани необходимых пластических и энергетических материалов, так и своевременное удаление из тканей конечных продуктов клеточного метаболизма. Внутренние барьеры сохраняют необходимое для нормальной жизнедеятельности относительное постоянство состава, физико-химических и биологических свойств жидких сред организма — крови, лимфы, тканевой жидкости и др. Благодаря гистогематическим барьерам каждый орган имеет свою адекватную среду, а кровь не приходит в непосредственное соприкосновение с клетками.
Функции гистогематических барьеров:
• Избирательная проницаемость. Гистогематические барьеры задерживают, а в ряде случаев вообще не пропускают из крови в ткани те или иные вещества, сохраняя таким образом постоянство внутренней среды — гомеостазис.
Гистогематические барьеры избирательно пропускают токсические клеточные метаболиты, гормоны, биологически активные вещества в обратном направлении — из тканей в кровь — в том случае, если их содержание в клетках достигает порогового значения.
• Защитная функция гистогематических барьеров особенно отчетливо выражена по отношению к токсинам, антителам, лекарственным веществам.
• Регулирующая функция. Переход биологически активных веществ через гистогематические барьеры зависит от величины молекул переносимого вещества, размеров пор в мембранах, наличия ионселективных каналов, электрического заряда веществ, их растворимости в липидах мембраны, а также от метаболических потребностей организма, нервньгх и гуморальных влияний, гемодинамики, микроциркуляции и др.
Для растворимых в липидах веществ гистогематические барьеры более проницаемы, поскольку липофильные молекулы легче проходят через липидные слои клеточных мембран.
Факторы, влияющие на функциональное состояние гисто- гематических барьеров. Барьерные функции зависят от возраста, пола, нервных и гуморальных взаимоотношений в организме, тонуса вегетативной нервной системы, многочисленных внешних и внутренних воздействий. На функциональное состояние гистоге- матических барьеров влияют стрессы, смена сна и бодрствования, голодание, степень утомления, травмы и др.
Некоторые содержащиеся в крови и тканях или введенные извне биологически активные вещества — ацетилхолин, гистамин, кинины, некоторые ферменты (например, гиалуронидаза) — в физиологических концентрациях изменяют проницаемость гистогема- тических барьеров и облегчают переход веществ из крови в ткань.
Противоположное действие оказывают катехоламины, соли кальция, витамин Р.
В большинстве случаев гистогематические барьеры препятствуют поступлению из крови в ткани лекарственных веществ и антител. Вместе с тем, некоторые факторы существенно уменьшают их сопротивляемость.
К ним относятся:
• облучение (местное или общее) световыми волнами различной длины (инфракрасными и ультрафиолетовыми);
• воздействие ультракороткими, высокочастотными волнами, рентгеновскими лучами, ультразвуком, электромагнитными полями;
• введение в организм некоторых гормонов (например, кортизола), психотропных веществ и витаминов.
Транскапиллярный транспорт. Транспорт веществ через стенки гемокапилляров осуществляется несколькими путями. Наиболее интенсивны процессы диффузии. Через общую обменную поверхность капилляров взрослого человека диффундирует около 60 л жидкости в 1 мин (около 85 тыс. л/сут). С помощью микропино- цитозных пузырьков через капиллярную стенку в обоих направлениях переносятся метаболиты и крупные молекулы белков. Через фенестры и межклеточные щели, расположенные между нексусами, проникают низкомолекулярные соединения и вода. Широкие щели синусоидных капилляров способны пропускать жидкость, различные вещества, в том числе высокомолекулярные соединения и мелкие частички. Базальный слой является преградой для транспортировки высокомолекулярных соединений и форменных элементов крови.
Виды гистогематических барьеров:
• гематоэнцефалический — между кровью и тканью мозга;
• гематотестикулярный — между кровью и просветом извитых семенных канальцев;
• гематоплацентарный — между кровью матери и кровью плода;
• гематофолликулярный — между кровью и фолликулами яичников.
К гистогематическим барьерам относят также гематоофтальми- ческий, гематоликворный, гематолимфатический, гематоплевраль- ный, гематосиновиальный и гематолабиринтный барьеры.
4.1.3. Гомеостазис
Внутренняя среда организма характеризуется относительным постоянством. «Постоянство внутренней среды,— полагал К. Бернар,— есть условие свободной жизни организма».
Роль функциональных систем в поддержании постоянства внутренней среды организма. Постоянство внутренней среды определяется содружественной деятельностью многочисленных функциональных систем, поддерживающих своими механизмами саморегуляции содержание во внутренней среде веществ, определяющих различные стороны метаболизма, а также безвредный для организма уровень конечных продуктов метаболизма. Отдельные функциональные системы определяют оптимальный уровень физиологических показателей, таких как кровяное давление, осмотическое давление, температура тела и т.д., которые сами по себе не участвуют непосредственно в метаболических процессах, но определяют их нормальное течение.
Многочисленные функциональные системы гомеостатического уровня связаны между собой результатами их деятельности. Муль- типараметрическое взаимодействие результатов деятельности этих функциональных систем определяет динамический гомеостазис в целом — гомеокинезис (см. также гл. 2).
4.2. ГОРМОНЫ И БИОЛОГИЧЕСКИ АКТИВНЫЕ ВЕЩЕСТВА [I]
Гормоны и биологически активные вещества участвуют в нейрогу- моральной регуляции физиологических функций.
Гормоны (от греч. hormaino — приводить в движение, побуждать) — группа биологически активных веществ, синтезируемых и секретируемых железами внутренней секреции, тканью органов, выполняющих неэндокринные функции (например, поджелудочная железа), и эндокринными клетками, рассеянными диффузно вне пределов одного органа.
Термин «гормон» предложен английскими физиологами В. Бейлиссом и Э. Старлингом в 1902 г.
4.2.1. Общие функции гормонов
Регулируя активность ферментов, гормоны изменяют проницаемость клеточных мембран, влияют на клеточный метаболизм, контролируют генетический аппарат, обеспечивают рост, дифференцировку тканей и развитие организма. Гормоны участвуют в поддержании гомеостазиса, адаптации организма к постоянно меняющимся условиям внешней среды, определяют ритмы физиологических функций, психическую деятельность, интеллект, размножение и вскармливание потомства.
Гормоны обратимо активируют такие клеточные процессы, как изменение мембранного потенциала, внутриклеточный обмен кальция, сокращение, секрецию и энергетический обмен. В ряде случаев
гормоны пролонгируют реакции образования ферментов, синтез специфических белков, митоз и другие процессы.
Гормоны выполняют в организме информационную функцию, осуществляя внутриклеточные, межклеточные и межорганные взаимодействия и специализированные регуляторные функции.
Особенности действия гормонов. Гормоны обладают высокой биологической активностью, т.е. эффективны в чрезвычайно низких концентрациях, порядка 10 6— 1(Г12 моль/л.
Выработка гормонов одной и той же химической природы характеризуется множественной локализацией их синтеза в организме. Например, различают панкреатическую и мозговую формы инсулина. Одни и те же регуляторные пептиды вырабатываются в ЦНС и желудочно-кишечном тракте.
Поступление гормонов из мест их образования к реагирующим клеткам происходит по множественным путям через циркулирующие жидкости: межклеточную жидкость, цереброспинальную жидкость, лимфу и кровь.
Один и тот же гормон может:
• передавать информацию локально по межклеточным контактам в пределах ткани, где он образуется;
• оказывать местное влияние на близлежащие ткани через межклеточную жидкость;
• обладать дистантным действием через циркулирующие жидкости на отдаленные от места выработки органы- и ткани- мишени, имеющие к ним аффильные рецепторы. Например, гипоталамический гормон аргинин-вазопрессин обладает короткодистантным действием в пределах ЦНС и, когда поступает в общий кровоток, оказывает дальнодистантное действие на рецепторы собирательных трубочек почек.
Один и тот же гормон в разных тканях может воспроизводить противоположные эффекты.
Каждый гормон может действовать разнонаправленно и в пределах одной и той же клетки в зависимости от его концентрации и функционального состояния клетки.
Гормоны определяют ритмы физиологических функций, синхронизируют суточные ритмы метаболических процессов.
Сами гормоны поступают во внутреннюю среду с определенным ритмом. Они определяют ритмы физиологических функций в
цикле «сон-бодрствование», процессах роста и развития, условиях жизни и труда человека в различной социальной и природно-климатической среде. Гормоны осуществляют своеобразную настройку гормональнозависимых физиологических процессов к факторам внешней среды.
Источники гормонов. Гормоны вырабатываются специализированными секреторными клетками различного строения, размеров, происхождения и локализации — гландулоцитами, популяциями клеток и самостоятельными органами.
Специализированные тканевые образования, основная функция которых заключается в выработке гормонов, называются железами внутренней секреции (эндокринные железы).
Клетки, сочетающие морфологические признаки нейронов и гландулоцитов, проводниковую и эндокринную функции, называются нейросекреторными. К особому типу клеток с функцией внутренней секреции относятся хромаффинные клетки. Выделяют также неспециализированные клетки, секретирующие так называемые тканевые гормоны.
Химическая классификация гормонов. По химической структуре гормоны подразделяются на три группы: производные аминокислот (амины и йодтиронины), белково-пептидные гормоны (небольшие пептиды, гликопротеины, белки) и стероиды.
Отдельное место занимает обширное семейство эйкозаноидов, наиболее известные из которых — простагландины, тромбоксаны и лейкотриены.
4.2.2. Железы внутренней секреции
Железы внутренней секреции — самостоятельные органы с особой морфологической структурой и специализированными функциями по выработке гормонов с широким спектром действия в организме.
К железам внутренней секреции относят гипофиз и эпифиз, расположенные в пределах головного мозга, и периферические железы, которые делят на зависимые и независимые от передней доли гипофиза (аденогипофиза).
К гипофиззависимым относят щитовидную железу, надпочечники (корковое вещество) и половые железы (яички, яичники). Взаи
моотношения между ними и аденогипофизом строятся по принципу прямых (положительных) и обратных (отрицательных) связей. Это значит, что тропные (от греч. tropos— направляю) гормоны аденогипофиза активируют выделение гормонов соответствующими железами, которые, в свою очередь, в определенных концентрациях воздействуют на аденогипофиз и активируют или тормозят его активность.
К гипофизнезависимым относятся все прочие железы — околощитовидные, эпифиз, панкреатические островки, мозговое вещество надпочечников, параганглии. Их деятельность подчинена собственным внутренним механизмам и ритмам.
Характерными морфофункциональными особенностями желез внутренней секреции являются:
• высокая степень специализации рабочих клеток — эндокри- ноцитов — по выработке гормонов;
• отсутствие выводных протоков для синтезируемых веществ;
• обилие кровеносных капилляров;
• интенсивный метаболизм;
• многочисленный и разнообразный рецепторный аппарат;
• избирательная химическая чувствительность к эндогенным веществам.
4.2.3. Динамика образования и действия гормонов
Синтез и секреция гормонов. Синтез и механизмы освобождения гормонов из эндокринных клеток определяются их химической природой.
Белково-пептидные гормоны и катехоламины по мере синтеза депонируются в гранулах. Опорожнение гранул происходит механизмами экзоцитоза. Тиреоидные гормоны хранятся в клетках в виде капельных включений, а стероидные гормоны выделяются по мере синтеза.
Секреция всех гормонов характеризуется общими признаками.
Гормональный секреторный цикл складывается из:
• поступления исходных веществ в клетку;
• внутриклеточного движения исходных продуктов синтеза, извлекаемых из внутриклеточных хранилищ;
• синтеза первичного секреторного продукта;
• транспорта, созревания и накопления секрета в клетке;
• выделения секрета из клетки.
По сравнению с нейромедиаторами гормоны секретируются с относительно небольшой скоростью — от 2 х 10'' до 0,4 х 10 2 г/сут.
Скорость секреции гормонов определяется рядом факторов. Она различна в эмбриональном периоде и постнатальном развитии — детстве, периодах полового созревания, репродуктивном возрасте, в менопаузе, старости. Скорость секреции определяется также функциональным состоянием организма, в частности физической и умственной активностью, наличием психоэмоционального стресса, менструальным циклом, беременностью, лактацией. Она также обусловлена природой синтезируемого гормона.
Эндокринные клетки в покое и под влиянием специфических стимулов секретируют гормоны не непрерывно и равномерно, а дискретно, отдельными порциями, что связано со спецификой их биосинтеза, депонирования и транспорта (рис. 4.4).
Секреторный гормональный цикл подвержен ритмическим изменениям, в которых выделяют максимум и минимум активности.

Рис. 4.4. Суточная ритмика секреции соматотропного гормона
Ритмы гормональной секреции
Экзогенные ритмы. Формируются под влиянием внешних синхронизаторов. К внешним синхронизаторам относятся: смена света и темноты, прием пищи, метеорологические факторы (температура, инсоляция, атмосферное давление), а для человека — различные социальные факторы.
Эндогенные ритмы. Ритмы, не зависящие от действия внешних синхронизаторов, сформировались в связи с циклическими явлениями в природе: суточными, лунными, сезонными, годичными и др. Так, например, эпифиз вырабатывает гормон мелатонин ночью, а днем — серотонин. Эпифиз, в свою очередь, определяет ритмы половых циклов, сна и бодрствования, суточные колебания температуры тела и ритм метаболических процессов в клетках организма.
Взаимодействие экзогенных и эндогенных ритмов, их динамическая синхронизация обеспечивают нормальную жизнедеятельность.
Суточные ритмы. Основными (базисными) ритмами секреции гормонов являются циркадианные ритмы (околосуточные, суточные). С одной стороны, они зависят от внешних синхронизаторов, а с другой — от врожденной циркадианной ритмики организма.
В структуре суточных ритмов существует временная последовательность активаций желез внутренней секреции и гормональнозависимых физиологических процессов. Например, концентрация кортизола — гормона коркового вещества надпочечников — в плазме крови у человека достигает максимального уровня утром, перед пробуждением. За 2—3 ч до этого увеличивается концентрация кортикотропина — тропного гормона гипофиза, стимулирующего синтез и секрецию кортизола в клетках коркового вещества надпочечников.
В реализации циркадианных ритмов гипофизарных, половых и других гормонов участвует гипоталамус, особенно его супрахиазма- тические ядра. Гуморальная регуляция ритмической деятельности гормонов осуществляется некоторыми нейропептидами. В частности, вещество П контролирует биоритм синтеза адреналина. Суточные колебания продукции самого вещества П связаны с ритмами сна, бодрствования и двигательной активности.
Формы переноса гормонов кровью. В крови гормоны циркулируют в нескольких молекулярных формах: свободной, связанной с
белками плазмы крови и адсорбированной форменными элементами — эритроцитами, лимфоцитами, моноцитами и тромбоцитами.
В свободной форме переносятся гидрофильные, легко растворимые в плазме, белковые гормоны. Они достигают клеток-мишеней без участия каких-либо переносчиков.
В связанной с белками (альбуминами) форме циркулируют катехоламины, которые достаточно долгое время находятся в депонированном состоянии (лишь 5—10% их находится в свободном состоянии), и гидрофобные гормоны.
Белки, образуя с гормоном крупномолекулярный комплекс, предотвращают их фильтрацию через капилляры клубочков нефрона (почечный фильтр) и экскрецию почками. Затрудняя транспорт гормонов через мембрану гепатоцитов, белки в значительной степени ограничивают метаболизм (инактивацию, биологическую трансформацию) гормонов в печени.
Однако по достижении транспортной формой гормона клетки-мишени белок «освобождает» гормон, и он легко проникает в клетку.
Стероидные и тиреоидные гормоны гидрофобны. Их транспорт осуществляется белками-переносчиками — глобулинами и альбуминами.
4.2.4. Взаимодействие гормонов
с клетками-мишенями
Информационная роль гормонов. Гормоны и олигопептиды обеспечивают передачу информации о различных, особенно метаболических, потребностях и их удовлетворении в ЦНС. Кроме того, гормоны обеспечивают информационное взаимодействие клеток на уровне центральной и вегетативной нервной системы, отдельных желез внутренней секреции, клеток в плазме крови, в органах-мишенях, а также молекул в процессах метаболизма в печени, почках и других органах.
По способу передачи информации выделяют аутокринное, изо- кринное, паракринное, телекринное и нейрокринное действие гормонов (рис. 4.5).
Аутокринное действие оказывают гормоны, высвобождающиеся из секретирующей клетки и действующие на нее же.

Рис. 4.5. Формы передачи информации гормонами клеткам-мишеням: А, Б — сложные формы взаимодействия секреторных нейронов гипоталамуса и клеток адено- и нейрогипофиза
Изокринно действуют секретируемые вещества, переносимые от клетки к клетке по контактам их поверхностей.
Паракринным действием обладают вещества (тканевые гормоны), поступающие из секретирующей клетки в межклеточное пространство и влияющие путем местной диффузии на соседние клетки.
Телекринное (дистантное) действие (на значительном удалении от места образования) оказывают гормоны, которые приносятся к клеткам-мишеням с током крови. Дистантным сигнальным действием обладают все традиционные «классические» гормоны желез внутренней секреции.
Нейрокринное действие обеспечивается нейросекретами белковой и пептидной природы, которые высвобождаются из окончаний нейросекреторных клеток. В пределах ЦНС нейропептиды
оказывают либо короткодистантное действие на многие нейроны, либо локальное — в области синаптических окончаний нейросекреторных волокон, нередко сосуществуя с основным медиатором. Нейрогормоны регулируют синтез и секрецию медиаторов, изменяют чувствительность рецепторов постсинаптических мембран либо оказывают на клетку-мишень прямое деполяризующее или гиперполяризующее действие. В ряде случаев нейропептиды взаимодействуют с периферическими органами через кровь, в которую они выводятся из нервных окончаний в сосудах.
Взаимодействие гормонов с рецепторами. Органы, ткани и клетки, избирательно реагирующие на гормон и отвечающие специфическим биологическим эффектом, называют органами-, тканями- и клетками-мишенями соответственно.
Рецепция гормонов подразделяется на два типа:
1) поверхностный (мембранный), при котором с мембранными рецепторами взаимодействуют белковые и пептидные гормоны, катехоламины, а также практически все гистогормоны и нейромедиаторы;
2) внутриклеточный, при котором в разных вариантах с цитоплазматическими и ядерными рецепторами связываются стероидные и тиреоидные гормоны.
Рецепторы пептидных гормонов и катехоламинов — мембранные рецепторы — асимметрично встроены в плазматическую мембрану; их узнающий фрагмент ориентирован к наружной поверхности, в сторону межклеточного пространства. В мембране они способны совершать продольные и поперечные движения. Высокой подвижностью обладают инсулиновые рецепторы, совершая латеральные и «поплавковые», а также вращательные движения — в направлении внеклеточного или внутриклеточного пространства.
Рецепторы стероидных гормонов локализованы в цитоплазме и ядре — имеют цитозольное происхождение, накапливаясь в ядре вторично в результате перехода в него гормон-рецепторных комплексов из цитозоля.
Рецепторы тиреоидных гормонов представлены несколькими независимыми пулами ядерных, цитоплазматических, митохондриальных рецепторных белков и, возможно, белков плазматических мембран.
Общие свойства и функции гормональных рецепторов:
• гормональные рецепторы специфичны; для каждого гормона существуют свои собственные рецепторы в клетках разного типа;
• многие клетки несут набор разных рецепторов (например, кардиомиоциты имеют рецепторы к адреналину, тироксину, глюкокортикоидам, инсулину и многим другим гормонам).
Рецепторы иногда подразделяют на подтипы. Большинство гормонов взаимодействуют с несколькими подтипами рецепторов. В различных тканях и даже в одной и той же клетке может находиться несколько подтипов рецепторов гормона. Вариабельность действия гормона объясняется полиморфизмом их рецепторов.
Пластичность рецепторов. Количество и плотность рецепторов на всей поверхности или в определенных участках клетки постоянно изменяются, отражая ее жизнедеятельность. В основе локального увеличения количества рецепторов лежат образование агрегатов рецепторов (петчинг) и концентрирование их на одном из полюсов клетки.
Одним из механизмов снижения количества рецепторов являются интернализация клеткой комплекса «гормон-рецептор» и последующее разрушение его лизосомами. В результате при избытке гормона снижается чувствительность клетки и происходит ослабление ее ответа на гормон.
Клетки-мишени тонко реагируют на интенсивность гормонального воздействия как путем изменения числа рецепторов, так и изменением их сродства (чувствительности) к гормону.
Мембранная рецепция. Большинство белково-пептидных гормонов взаимодействует с определенными рецепторами на наружной стороне клеточной мембраны, свыше 100 из которых сопряжены с G-белками плазматической мембраны. Большинство из них имеет 7-доменную структуру, представленную на рис. 4.6.
Как видно из рис. 4.6, полипептидная цепь рецептора, включающая от 400 до 600 аминокислотных остатков, 7 раз «прошивает» плазматическую мембрану. Домен с МН2-концом находится снаружи клетки, с СООН-концом — внутри. Участок взаимодействия с G-белками находится в третьей цитоплазматической петле.
G-белки являются обязательными участниками преобразования гормонального сигнала. Десятки рецепторов сопряжены с раз-
|
|
 |
ними G-белками, но и один и тот же G-белок может сопрягаться со многими рецепторами. G-белки либо участвуют в образовании вторичных посредников, либо сами непосредственно выполняют регуляторные функции в клетке. G-белки управляют несколькими мембранными ферментами и рядом ионных каналов, взаимодействуют с цитоскелетом.
Через 7-доменные рецепторы действуют многие гормоны и биологически активные вещества: либерины и статины гипоталамуса, адреналин, ангиотензин II, дофамин, серотонин, гистамин, некоторые ростовые факторы, частично — эйкозаноиды.
Гормоны, связанные с 7-доменными рецепторами, никогда не проникают в ядро, а влияют на метаболизм клетки посредством сложного биохимического механизма, который приводит к биологическому эффекту с участием вторичных посредников (рис. 4.7).
Внеклеточная
 |
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
| ||||||||||||||
 | |||
 | |||
| ||||
| ||||
 |
| |||||
| |||||
| |||||
 | |||||||
 |  | ||||||
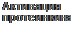 | |||||||
Рис. 4.7. Мембранная рецепция пептидных гормонов
Образующиеся на поверхности клетки гормон-рецепторные комплексы выполняют многие функции: активируют ионные каналы, регулируют активность G-белков, изменяют обмен нуклеотидов и фосфоинозитидов, концентрацию ионизированного кальция в цитоплазме. В результате облегчается или угнетается образование вторичных посредников гормональных реакций в клетках.
Вторичными посредниками являются циклические нуклеотиды (цАМФ, цГМФ), ионы Са2\ метаболиты мембранных фосфолипидов, содержащих инозитол, простагландины и их производные и др.
Вторичные посредники активизируют диацил- и глицеринза- висимые протеинкиназы, которые находятся в клетке в неактивном состоянии. Протеинкиназы осуществляют фосфорилирование множества внутриклеточных белков, которые могут влиять на различные функции клетки, в частности ее дифференцировку и рост.
Кроме указанных веществ функцию вторичных посредников выполняют мембранные рецепторы — ферменты и некоторые ростовые факторы.
Цитоплазматическая рецепция стероидных гормонов. Стероидные гормоны и производные тирозина взаимодействуют с цитоплазматическими рецепторами, после чего проникают в ядро клетки.
Известны цитоплазматические рецепторы к эстрадиолу, андрогенам, глюкокортикоидам и минералокортикоидам, структурная организация которых для разных стероидных гормонов идентична.
Стероиды поступают в ядро реагирующих клеток в комплексе с цитозольными рецепторами. Такие гормон-рецепторные комплексы, прежде чем достичь ядра, претерпевают конформационные изменения в цитозоле, и после удаления из них низкомолекулярных веществ специальный транспортный белок переносит их в ядро. Переход стероидов в ядро вызывает структурную перестройку хроматина и активацию генов в соответствующих местах. Стероид-ре- цепторные комплексы способны связываться практически со всеми компонентами хроматина, с ДНК, РНК, некоторыми кислыми и основными белками. Ряд эффектов стероидов осуществляется вне ядра, на посттранскрипционном уровне в результате взаимодействия с рецепторами рибосом, плазматическими мембранами компонентов цитоскелета. Клеточный механизм действия стероидных гормонов представлен на рис. 4.8.
 |
|
| |||||
| ||||||
Наряду с этим имеются данные о том, что стероиды вначале связываются специфическими белками мембран клетки, которые транспортируют их или к цитоплазматическому рецептору, или, минуя его, непосредственно к рецепторам ядра.
В трансмембранном проведении и последующем внутриклеточном взаимодействии стероидных гормонов определенную роль играют G-белки.
В организме нет ни одной клетки, не испытывающей влияния стероидных гормонов. Каждая клетка находится под действием разных стероидов. В клетках отдельных органов и тканей стероидные гормоны накапливаются и взаимодействуют в различных соотношениях, инициируя ответы различной интенсивности.
Рецепция тиреоидных гормонов. Механизмы действия тиреоидных гормонов до конца не раскрыты. Трийодтиронин связывается с рецепторами в ядре клетки и воздействует на геном, охватывая процессы транскрипции и трансляции, вследствие чего в клетках организма усиливается синтез белка.
Действие тиреоидных гормонов осуществляется также после комплексирования их с рецепторами клеточной мембраны, где они непосредственно влияют на активность некоторых локализованных в ней ферментов, стимулируют транспорт глюкозы и аминокислот через мембрану.
 Гормон-рецепторные комплексы, образованные на поверхности клетки, попадают в цитоплазму, где взаимодействуют с белками и образуют внутриклеточный фонд (пул) тиреоидных гормонов.
Гормон-рецепторные комплексы, образованные на поверхности клетки, попадают в цитоплазму, где взаимодействуют с белками и образуют внутриклеточный фонд (пул) тиреоидных гормонов.
8 Нормальная физиология
Внутриклеточное действие тиреоидных гормонов во многом определяется взаимодействием трийодтиронина с рецепторами митохондрий и повышением активности ферментов — регуляторов углеводного обмена.
Внутриклеточное взаимодействие гормонов. Взаимодействие гормонов в клетках осуществляется в разных формах: эффекты одних гормонов могут блокировать, усиливать либо ослаблять действие других.
Пермиссивные эффекты реализуются на уровне подпороговых концентраций одного гормона, разрешающего действие другого. Пермиссивный эффект осуществляется на уровне синтеза белка, а также рецепторов и вторичных посредников.
Сенсибилизирующие (облегчающие) эффекты проявляются в резком повышении чувствительности клеток-мишеней к другим гормонам. Во всех случаях сенсибилизирующие эффекты обусловлены повышением концентрации рецепторов соответствующих гормонов и облегчением внутриклеточных процессов перекрестного проведения гормональных сигналов.
Синергизм проявляется в однонаправленном действии гормонов: в результате действия одного гормона усиливается влияние другого. Например, соматотропин, инсулин и тироксин синергичны в стимуляции ростовых процессов; лютропин, эстрогены, глюкокортикоиды и инсулин — в отношении секреции молочной железы.
Антагонизм — разнонаправленное действие гормонов по отношению к регулируемому процессу. Например, паратирин (паратгормон) и кальцитонин — антагонисты в регуляции кальциевого обмена; глюкагон и инсулин — углеводного и липидного.
Одна и та же группа гормонов может быть антагонистична в отношении одних процессов и синергична в отношении других.
Изложенное выше свидетельствует о том, что существуют два механизма постмембранного действия гормонов, принципиально различающихся по признаку того, где образуется гормон-рецептор- ный комплекс — внутри клетки или на ее поверхности.
Наиболее характерным признаком гормонов, действующих через вторичные посредники, является их способность вызывать активацию ранее синтезированных, предсуществующих белков — ферментов, поэтому их эффекты развиваются относительно быстро.
Самое медленное воздействие на клеточный метаболизм оказывают стероидные и тиреоидные гормоны, так как они реализуют свое действие в клетке через экспрессию генов, с образованием множества мРНК, инициирующих, в свою очередь, синтез белков.
Вместе с тем, и пептидные гормоны также обладают способностью избирательно влиять на транскрипцию генов в ядре клетки. Эффекты пептидных гормонов могут быть реализованы с поверхности мембран клеток как за счет вторичных посредников, так и путем прямого поступления гормонов внутрь клетки и механизма интернализации гормон-рецепторного комплекса.
4.2.5. Регуляция секреции гормонов
Регуляция функций желез внутренней секреции осуществляется несколькими взаимосвязанными механизмами: внутриклеточным, нервным, гормональным и негормональным.
Внутриклеточная регуляция реализуется с помощью рецепторов гормонов, G-белков, циклических нуклеотидов, ферментов, Са2+ и других вторичных посредников синтеза и секреции гормонов, наконец — с участием генома. Гены задают тип синтезируемого в клетке гормона, тогда как другие гормоны являются регуляторами генов.
Нервная регуляция представлена сложной совокупностью периферических и центральных механизмов, среди которых главная роль принадлежит гипоталамо-гипофизарному механизму.
Нейроны гипоталамуса, получающие информацию от внешней и внутренней среды, передают ее с помощью медиаторов на нейросекреторные пептидергические нейроны. Последние синтезируют и выделяют разнообразные нейрогормоны, поступающие из гипоталамуса в гипофиз и/или, минуя его, в общий кровоток и далее к железам внутренней секреции.
Продолжительность действия гормонов. Время действия гормонов характеризуется периодом их полураспада, необходимым для расщепления и инактивирования половины имеющегося гормона (табл. 4.1).
Латентный период — время от момента рецепции гормонального сигнала до появления специфической клеточной реакции. Для каждого гормона оно индивидуально (от нескольких секунд
до нескольких суток) и может быть представлено в нарастающей последовательности: пептиды — секунды, минуты; белки и гликопротеины — минуты, часы; стероиды — часы; йодсодержащие гормоны — сутки.
Таблица 4.1
Продолжительность действия гормонов
| Белково-пептидные гормоны | Производные аминокислот | Стероиды |
| Вазопрессин, < 1 мин | Адреналин, 10 с | /Альдостерон, 30 мин |
| Инсулин, 7 мин | Норадреналин, 15 с | Кортизол, 90—100 мин |
| Пролактин, 12 мин | Трийодтиронин, 1 сут | 1,25-дигидроксивита- мин D, 15 ч |
| АКТГ, 12-25 мин | Тироксин, 7 сут | 25-гидроксивитамин D, 15 сут |
| Л Г, 15—45 мин | ||
| ФСГ, 180 мин |
Примечание'. ЛГ — лютеинизирующий гормон; ФСГ — фолликулостимулирующий гормон.
Коротколатентным действием обладает адреналин, который изменяет активность предсуществующих, т.е. ранее синтезированных, ферментов. Длительный латентный период наблюдается у половых стероидных гормонов. Их действие направлено на геном клетки и связано с образованием специфических клеточных белков, используемых в пластических анаболических процессах.
В целом, время жизни гормона определяется его химической природой, типом гормон-рецепторного взаимодействия, механизмами трансмембранного проведения и внутриклеточного усиления сигнала. Во многих отношениях эти процессы еще остаются недостаточно изученными.
Распад гормонов. В различных органах — печени, почках, легких, мозге — существуют ферменты, инактивирующие и расщепляющие «отработанные» белковые и пептидные гормоны. Часть гормонов разрушается в плазме крови. Некоторые гормоны после взаимодействия с рецепторами подвергаются внутриклеточной деградации. Распад гормон-рецепторных комплексов или гормона после его отщепления от рецептора происходит в лизосомах.
4.2.6. Гормоны эндокринных желез
Функции желез внутренней секреции исследуются при их экстирпации или при введении в организм соответствующих гормонов.
4.2.6.1. Гормональные функции гипофиза
Эффекты удаления гипофиза. Удаление гипофиза в раннем возрасте нарушает рост и половое созревание животных. Половая активность у взрослых животных после удаления гипофиза тоже прекращается. При этом наблюдается гипофункция щитовидной железы, атрофия надпочечников, кахексия (истощение) и полиурия.
Гормоны гипофиза. Основные гормоны гипофиза и их действие приведены в табл. 4.2.
Гипофиз тесно связан в своей деятельности с гипоталамусом и другими лимбическими образованиями мозга, а также с эпифизом.
Выделяемые передним гипоталамусом (супраоптические и па- равентрикулярные ядра) вазопрессин и окситоцин через аксональный транспорт поступают в заднюю долю гипофиза. Передняя доля гипофиза под влиянием гипоталамических либеринов вырабатывает адренокортикотропный, тиреотропный, соматотропный и гонадотропные гормоны.
Гормоны каждой из желез внутренней секреции через кровь оказывают обратные влияния на соответствующие рецепторы гипоталамической области и через либерины и статины оказывают положительные и отрицательные влияния на выделение тропных гормонов гипофиза (рис. 4.9).
Нейросекреторные функции гипоталамуса. В гипоталамусе выделяют три основные группы нейросекреторных клеток: нона- пептидергические, Либерии- и статинергические и моноаминерги- ческие, которые образуют в переднем, среднем и заднем гипоталамусе три группы нервных центров.
Нонапептидергические крупноклеточные центры гипоталамуса включают крупноклеточные супраоптические и паравентрикуляр- ные ядра, вырабатывающие нонапептиды — вазопрессин и окситоцин. В мелких клетках этого центра продуцируется большая группа регуляторных пептидов — кортиколиберин, соматолиберин, тироли- берин, опиатные пептиды, нейротензин, ангиотензин II, ВИП и др.
| Гормоны гипофиза |
| Отдел гипофиза | Название гормона | Физиологические эффекты |
| Аденогипофиз | Соматотропин (СТГ), белок | Анаболическое действие. Стимулирует синтез белка клетками, рост костей (стимуляция энхондрального окостенения), мышц и других органов. Увеличивает относительное содержание в организме белка и воды, снижает содержание жиров. Избыточная продукция СТГ ведет к гигантизму в молодом возрасте и к акромегалии в зрелом и пожилом возрасте. Недостаток СТГ в детстве проявляется в карликовости |
| Лактотропин (пролактин), белок | Усиливает пролиферацию роста молочных желез и секрецию молока, тормозит синтез ФСГ и Л Г, стимулирует рост предстательной железы и яичек. Участвует в организации материнского поведения: вызывает материнское поведение — заботу о потомстве даже у животных, не имеющих своего потомства. Стимулирует секрецию прогестерона и образование желтого тела в яичниках. Поддерживает активность желтого тела. Обладает антистрессорным действием | |
| Тиреотропный гормон (’ПТ), гликопротеид | Стимулирует процессы йодирования тирозина в щитовидной железе и распад тиреоглобулина на йодированные аминокислоты. При гипосекреции ТТГ снижается продукция тиреоидных гормонов | |
| Фоллитропин (ФСГ), гликопротеид | У женщин: стимулирует рост фолликулов, секрецию эстрогенов и овуляцию. У мужчин: влияет на образование андрогеневязывающего белка клетками Сертоли — опосредованная стимуляция сперматогенеза, стимулирует развитие семявыносящих канальцев | |
| Лютропин (ЛГ), глико протеид | У женщин: стимулирует овуляцию, образование желтого тела, развитие и созревание половых клеток, секрецию половых гормонов. В мужском организме вызывает разрастание в семенниках интерстициальной ткани (клеток Лейдига), участвующей в сперматогенезе, а также стимулирует продукцию тестостерона |
|
|
| Таблица 4.2 |
| Глава 4. Внутренняя среда организма. Системные механизмы гомеостазиса |
|
| Гормон, стимулирующий интерстициальные эндокриноциты | У мужчин: стимулирует рост интерстициальных эндокриноцитов яичек |
| Кортикотропин (АКТГ), полипептид | Регулирует образование и секрецию глюкокортикоидов коры надпочечников. Мобилизует жир из жировой ткани. Влияет на интенсивность обмена веществ: при двустороннем удалении надпочечников введение АКТГ повышает потребление кислорода тканями, усиливает жировой обмен, понижает чувствительность организма к инсулину. Участвует в механизмах стресса | |
| 0-эндорфин, олигопептид | Тормозит синтез и секрецию кортикостероидов, кортикотропина и меланотропина; снижает болевую чувствительность; подавляет чувство голода и пи- щедобывательное поведение | |
| Нейрогипофиз | Окситоцин, нонапептид | Стимулирует сокращения беременной матки, миоэпителиальных клеток ацинусов молочных желез, выделение молока. Активность окситоцина достигает максимума к концу беременности. Усиливает тонус гладких мышц желудочнокишечного тракта |
| Антидиурети- ческий (АДГ), вазопрессин, нонапептид | Увеличивает реабсорбцию воды в почечных канальцах. Стимулирует выделение гиалуронидазы клетками дистальных отделов почечных канальцев. В больших концентрациях повышает тонус гладкой мускулатуры сосудов. Повышает кровяное давление. Стимулирует секрецию кортикотропина, тиротропина, соматотропина. Участвует в процессах памяти | |
| Промежуточная доля гипофиза (у человека практически отсутствует) | Меланотропин или меланоцитостимулирующий гормон (МСГ), полипептид | Стимулирует синтез меланина, распределение гранул пигмента в коже, радужке, сетчатке глаза, повышает возбудимость скелетных мышц и нервов, учащает сердцебиение, изменяет психоэмоциональное состояние, вызывает страх и беспокойство. На секрецию МСГ существенно влияет освещенность окружающей среды |
| Гормоны и биологически активные вещества |
Вен 'рамолиопы к-о

Рис. 4.9. Схема гормональных гипоталамо-гипофизарных взаимодействий с периферическими железами внутренней секреции: 1 — ткани; 2— щитовидная железа; 3— паращитовидные железы; 4— поджелудочная железа; 5— надпочечники; 6— молочные железы; 7— половые железы
Аксоны крупноклеточных нейронов образуют гипоталамо-ги- пофизарный путь, оканчивающийся в заднем нейрогипофизе, и туберо-инфундибулярный путь, оканчивающийся в переднем нейрогипофизе и туберальной части аденогипофиза.
Меньшая часть аксонов этого центра образует экстрагипотала- мические пути, соединяющие его с передним, средним, продолговатым и спинным мозгом, в которых нонапептиды осуществляют нейротропное и нейромедиаторное действие.
Либерии- и статинергические мелкоклеточные центры вырабатывают главные гипофизотропные гормоны и составляют так называемую гипофизотропную зону гипоталамуса. Аксоны нейросекреторных клеток, вырабатывающих либерины и статины, обычно заканчиваются в срединном возвышении. Эти клетки связаны также с желудочками мозга.
Моноаминергические мелкоклеточные центры гипоталамуса вырабатывают норадреналин, серотонин, дофамин. Аксоны моноами- нергических нейронов образуют внутригипоталамические связи, иннервируют разные отделы головного мозга и связаны с нейрогипофизом, с желудочками мозга. Моноамины поступают также в портальный кровоток аденогипофиза.
4.2.6.2. Гипофизотропные гормоны гипоталамуса
Гипофизотропные гормоны гипоталамуса усиливают (высвобождают) рилизинг-гормоны — либерины и угнетают (ингибируют) секрецию и высвобождение (выделение) соответствующих тропных гормонов передней доли гипофиза — статины.
Кортиколиберин (кортикотропин рилизинг-гормон). Основное количество кортиколиберина локализуется в гипоталамусе, однако он выявляется и в других отделах ЦНС, включая кору головного мозга и различные подкорковые ядра, где он выполняет роль нейротрансмиттера, координируя ответы организма на различные стрессовые ситуации.
Гипофизотропные нейроны, секретирующие кортиколиберин, локализуются в дугообразном, дорсомедиальном, вентромедиальном ядрах, но наибольшее их количество расположено в паравен- трикулярных ядрах гипоталамуса. Скорость биосинтеза и высвобождения кортиколиберина модулируется моноаминами. Нервные аксоны этих нейронов достигают срединного возвышения, где они контактируют с капиллярами портальной системы. С током крови кортиколиберин достигает клеток аденогипофиза. Период полураспада кортиколиберина в плазме крови составляет около 60 мин. Кортиколиберин избирательно увеличивает высвобождение АКТГ и других гормонов, производных общего предшественника — про- опиомеланокортина (ПОМК). Его влияние на усиление высвобождения АКТГ ингибируется глюкокортикоидами. Стимуляция высвобождения АКТГ наблюдается только в присутствии ионов Са2+.
Кортиколиберин стимулирует синтез и высвобождение АКТГ посредством цАМФ и инозитолфосфата.
Иммунореактивный кортиколиберин и прокортикотропин- мессенджерная РНК (мРНК) выявляются и в различных органах (например, в мозговом слое надпочечников, печени, поджелудочной железе, спинном мозге, плаценте). Такой внегипоталамический «тканевой» кортиколиберин вызывает более продолжительное, чем гипофизотропный кортиколиберин, высвобождение АКТГ. У женщин в период беременности уровень иммунореактивного корти- колиберина увеличивается, достигая пика в период родов. После родов его содержание в крови быстро падает, достигая нормальных значений. Показано, что источником такого кортиколиберина является плацента.
Соматолиберин (соматотропин рилизинг-гормон). Сомато- либерин синтезируется в дугообразном (аркуатном) и вентромедиальном ядрах гипоталамуса. Аксоны нейронов указанных ядер оканчиваются в области срединного возвышения. Высвобождение соматолиберина стимулируется серотонином, норадреналином и эндорфинами.
Тиролиберин (тиреотропин рилизинг-гормон). Тиролиберин широко представлен в ЦНС и желудочно-кишечном тракте. Нейроны, секретирующие тиролиберин, локализованы в медиальной и парвоцеллюлярной областях паравентрикулярного ядра, в супра- хиазматическом, преоптическом, дорсомедиальном ядрах гипоталамуса. Аксоны, содержащие тиролиберин, выявляются в дорсомедиальном ядре, медиальной области паравентрикулярного ядра гипоталамуса, но наибольшая их концентрация отмечается в области срединного возвышения.
Тиролиберин, помимо своей гипофизарной функции, в других областях ЦНС выполняет роль нейропередатчика или нейромодулятора и оказывает, в основном, стимулирующее влияние. Это проявляется повышением спонтанной двигательной активности животных, артериального давления, увеличением времени судорожной активности и летальности от стрихнина, увеличением двигательной активности у животных после введения морфина. Тиролиберин потенцирует возбуждающее действие ацетилхолина на нейроны коры головного мозга, вызывает анорексию, повышает высвобождение норадреналина и дофамина из синаптосом и ускоряет период обмена норадреналина. Кроме того, тиролиберин участвует в терморегуляции и при введении его в желудочки мозга вызывает гипертермию. Показано также, что тиролиберин широко представлен в поджелудочной железе.
Гонадолиберин (гормон, высвобождающий лютеинизирующий и фолликулостимулирующий гормоны, — люлиберин). Гипоталамическая регуляция фолликулостимулирующего (ФСГ) и лютеинизирующего (Л Г) гормонов осуществляется одним гормоном гипоталамуса — гонадолиберином, который в высокой концентрации определяется в области срединного возвышения и organum vasculosum. У человека наибольшее количество нейронов, содержащих гонадолиберин, локализуется в области медиобазального гипоталамуса между третьим желудочком и срединным возвышением. Нейроны, содержащие гонадолиберин, локализуются и в других областях ЦНС, ответственных за эмоциональное и половое поведение. В регуляции секреции гонадолиберина участвуют половые гормоны, олигопептиды и моноамины. Опиоидные пептиды и ГАМК угнетают, а серотонин, адреналин, норадреналин, нейропептид Y, ангиотензин II и ацетилхолин стимулируют высвобождение гонадолиберина.
Гонадолиберин высвобождается пульсирующим способом. С каждым пульсом из гипоталамуса высвобождается в среднем 65—90 пг гонадолиберина. Из гипоталамуса гонадолиберин через портальные сосуды транспортируется в гипофиз, где связывается с плазматическими мембранами клеток его передней доли.
Пролактолиберин (пролактин рилизинг-гормон). Из экстрактов гипоталамуса различных животных (крысы, птицы и др.) изолированы фракции, обладающие способностью высвобождать пролактин (ПРЛ). Полагают, что эту функцию выполняют тиролиберин и ВИП. Секреция пролактолиберина осуществляется гормонами передней гипоталамической области и области срединного таламуса.
Ме
 2020-05-25
2020-05-25 459
459








