1. Что называют контактной коррозией? В каких условиях она возникает?
2. Что такое протекторная защита.
3. Как изменяются электродные потенциалы металлов в растворе электролита.
4. Как оценивают эффективность катодной защиты?
5. Поясните принцип катодной защиты.
6. Нарисуйте и поясните поляризационную диаграмма короткозамкнутой двухэлектродной системы (гальванической макропары)
7. Виды контроля коррозионного процесса
8. Диаграммы Эванса.
9. В чем основные отличия процесса химической коррозии от процесса электрохимической коррозии?
10. Каковы причины возникновения коррозионных элементов?
Лабораторная работа №8 Защита металлов от коррозии с помощью ингибиторов
Цель работы. Изучить защиту металлов от коррозии с помощью ингибиторов
Теоретическая часть
С целью повышения коррозионной стойкости металлов в агрессивную среду вводят определенные химические соединения – ингибиторы. Ингибиторная защита может применяться как самостоятельный метод борьбы с коррозией, так и в сочетании с другими методами. Существует некоторая условная классификация ингибиторов.
По механизму действия на процесс электрохимической коррозии:
- анодные ингибиторы,
- катодные ингибиторы,
- смешанные ингибиторы.
По химическому составу ингибиторы подразделяются на:
- неорганические,
- органические.
По эффективности действия в зависимости от рН среды ингибиторы
бывают:
- кислотные,
- щелочные,
- ингибиторы для нейтральных сред.
По условиям применения ингибиторы можно разделить на:
- для растворов,
- летучие ингибиторы.
Говоря об ингибиторах коррозии, следует рассматривать конкретную коррозионную среду, так как универсальных ингибиторов не существует.
Механизм защитного действия ингибиторов сводится к экранированию поверхности металла, в результате которого нет доступа агрессивной среды к металлу. Со средой ингибитор не взаимодействует. Защитное действие ингибитора объясняется пленочной и адсорбционной теориями, согласно которым сначала ингибитор адсорбируется на поверхности металла, а затем образует с металлом химическое соединение, которое в виде пленки покрывает всю защищаемую поверхность. Хорошими защитными свойствами эта пленка будет обладать в том случае, если химическое соединение в данной среде не будет растворяться.
Анодные ингибиторы увеличивают анодную поляризацию металла, смещая потенциал анодных участков в положительную сторону. Анодные ингибиторы уменьшают скорость перехода ионов металла в раствор за счет изоляции анодных участков защитными пленками.
В качестве анодных ингибиторов используют соли азотной, азотистой, хромовой и бихромовой кислот и другие соединения. Необходимо отметить, что соли хромовой и бихромовой кислот при неправильной их концентрации могут быть опасными и вместо защиты от коррозии вызвать ее ускорение.
Катодные ингибиторы уменьшают скорость коррозии за счет затруднения доступа деполяризатора к поверхности металла и сокращения площади катодных участков вследствие образования экранирующей защитной пленки.
Катодными ингибиторами являются бикарбонат кальция Са(НСО3)2, декстрин, уротропин и другие.
SiO×Наиболее эффективными являются ингибиторы смешанного действия, так как они уменьшают скорость анодной и катодной реакций. К ингибиторам смешанного действия относятся силикаты с общей формулой - n2Ме×2О и полифосфаты – (МеPО3)n. Защитное действие силикатов и полифосфатов состоит в образовании непроницаемой защитной пленки на поверхности металла.
Использование ингибиторной защиты требует знания механизма коррозионного процесса и соблюдения условий, обеспечивающих эффективную защиту металла в данной среде. Количественная оценка действия ингибитора на скорость коррозионного процесса характеризуется коэффициентом ингибирования или защитным действием Z.
Коэффициентом ингибирования называется отношение скорости коррозии металла в среде не содержащей ингибитора к скорости коррозии того же металла после введения в эту среду ингибитора и вычисляется по уравнению:
g =  ; (1)
; (1)
где g - коэффициент ингибирования;
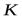 - скорость коррозии металла в отсутствии ингибитора, г/м2ч;×
- скорость коррозии металла в отсутствии ингибитора, г/м2ч;×
 - скорость коррозии металла при наличии ингибитора, г/м2ч.×
- скорость коррозии металла при наличии ингибитора, г/м2ч.×
Защитное действие ингибитора определяется по уравнению 2 и выражается в процентах:
Z =  (2)
(2)
К наиболее важным факторам, влияющим на эффективность действия ингибиторов, относятся: температура среды, концентрация ингибитора, кислотность среды и взаимное влияние ингибиторов.
Температура среды. Для большинства ингибиторов с увеличением температуры агрессивной среды наблюдается возрастание эффективности действия g, а затем при достижении определенной температуры (60-800С) снижение. При увеличении концентрации кислоты и концентрации ингибитора максимум ингибиторного эффекта возрастает.
Концентрация ингибитора. Ингибитора необходимо вводить в количестве достаточном для того, чтобы покрыть поверхность металла мономолекулярным слоем. Для большинства органических ингибиторов характерно с ростом их концентрации до некоторого определенного количества повышение эффективности защитного действия, а затем эффективность не меняется. У неорганических анодных ингибиторов при малых концентрациях наблюдается рост скорости коррозии и только при достижении определенной концентрации наступает резкое уменьшение скорости коррозии вследствие пассивации поверхности металла. Для каждой конкретной системы оптимальную концентрацию ингибитора определяют опытным путем. Однако при эксплуатации промышленный ингибитор может адсорбироваться на образующихся продуктах коррозии, может разрушаться (например, микроорганизмами), осаждаться из раствора или испаряться. Поэтому на практике в первый момент “пуска” ингибиторной защиты вводят избыточное количество ингибиторов в систему, а в дальнейшем осуществляют контроль и восполняют при необходимости добавку ингибитора.
Кислотность среды. Большинство ингибиторов эффективно действуют только при определенных значениях рН раствора. Это связано со стойкостью защитных пленок или ингибитора. Пленкообразующие ингибиторы проявляют защитное действие только в таких средах, где наблюдается образование труднорастворимых соединений. Карбонаты и фосфаты эффективно действуют в нейтральных средах, а нитриты, сульфиды, органические соединения и другие – в кислых средах.
Взаимное влияние ингибиторов. Смеси ингибиторов, имеющих одинаковое или близкое химическое строение, обладают, как правило, аддитивностью (рисунок 1). Но на практике аддитивность встречается очень редко.
Смеси ингибиторов, имеющих разное химическое строение, могут проявлять антагонизм или синергизм.
Антагонизм это ослабление эффективности действия ингибиторов в смеси. Такие сочетания в системе недопустимы. Примером антагонистического эффекта служит воздействие смеси анилина и хлорида сурьмы на сталь, погруженную в раствор соляной кислоты.
Синергизм это увеличение эффективности действия ингибиторов в смеси. Синергизм ведет к достижению большего защитного эффекта, чем при раздельном применении этих ингибиторов. При синергизме можно дорогой ингибитор заменить смесью двух дешевых.
Синергизм обнаруживается в смесях органических и неорганических веществ, а также в смесях органических соединений с неорганическими соединениями.
Экономическая эффективность применения ингибиторов складывается из таких показателей  как:
как:

1-аддитивность, 2 – антагонизм, 3 – синергизм
Рисунок 16 – Варианты действия смеси двух ингибиторов
1 – Увеличение промежутков времени работы деталей между ремонтами, что приводит к снижению расходов на ремонт и увеличивает выпуск продукции за счет сокращения простоев.
2 – Удешевляет стоимость конструкции вследствие применения углеродистых и низколегированных сталей вместо дорогих коррозионностойких материалов.
3 - Экономия топлива за счет улучшения теплообмена, ухудшающегося вследствие отложения продуктов коррозии на стенках теплообменников.
4 – Уменьшение потерь от утечек воды и других жидкостей из-за коррозионных повреждений системы.
В конкретных условиях могут быть учтены и другие факторы, определяющие экономическую эффективность применения ингибиторов. Так, например, можно учесть уменьшение расхода энергии на преодоление гидравлических сопротивлений от накипи и других коррозионных отложений в системах без применения и с применением ингибиторов. На каждый рубль, затраченный на производство ингибиторов, можно получить в итоге пять рублей прибыли.
Выполнение работы
Испытание проводится на двух образцах одного и того же материала. Перед началом работы необходимо зачистить поверхность образцов наждачной бумагой, измерить длину, ширину и толщину с помощью штангенциркуля, а затем протереть их смоченной в бензине фильтровальной бумагой. После этого взвесить образцы на аналитических весах с точностью до четвертого знака и поместить на металлических крючках в фарфоровые стаканы. Один стакан заполняется агрессивной средой без ингибитора, а второй – с агрессивной средой с ингибитором. Время испытания составляет 50 минут. После окончания эксперимента образцы вынимают из раствора, промывают под струей холодной воды и на фильтровальной бумаге помещают в сушильный шкаф для сушки в течение 1-2х минут. Сухие образцы охлаждают на воздухе до комнатной температуры и взвешивают на аналитических весах. Определив потери массы и площадь поверхности образцов, определяют скорость коррозии по формуле:
К =  , г/м2ч×
, г/м2ч×
(3)
m – потери массы за время испытания, г;Dгде
S – площадь поверхности образца, м2;
- время испытания, ч.t
Проведя эти вычисления, определить коэффициент ингибирования по формуле 1 и защитное действие по формуле 2.
 2020-06-12
2020-06-12 159
159








