1. Система, состоящая из одной фазы:
A) изолированная
Б) гомогенная
B) гетерогенная
Г) открытая
2. Мера способности системы совершать работу:
А) давление
Б) объем
В) энергия
Г) теплота
3. Если при переходе системы из одного состояния в другое, сохраняется давление, процесс называется:
A) адиабатическим
Б) изобарным
B) изотермическим
Г) изохорным
| 4. При изобарном процессе теплота расходуется на: A) уменьшение объема; Б) изменение внутренней энергии; B) совершение работы расширения. 5. Количество теплоты, которое выделяется при сгорании 1 моль вещества: A) теплота растворения Б) теплота сгорания B) теплота образования Г) теплота разложения |
6. При охлаждении, кристаллизации, полимеризации энтропия:
А) увеличивается
Б) уменьшается
В) не изменяется
7. Система, неспособная к обмену с окружающей средой ни веществом, ни энергией, называется
| А) | закрытой |
| Б) | многофазной |
| В) | изолированной |
| Г) | однофазной |
8. Закончите определение: «Изобарным называется процесс, протекающий при постоянном...
| А) | объёме |
| Б) | значении концентрации |
| В) | давлении |
| Г) | значении температуры |
9. Как называется процесс, идущий при постоянном количестве теплоты?
| А) | адиабатическим |
| Б) | самопроизвольным |
| В) | изобарным |
| Г) | изотермическим |
10. Тело или группа тел, находящихся во взаимодействии, мысленно обособленные от окружающей среды и имеющие поверхности раздела – это:
| А) | вариантность |
| Б) | фаза |
| В) | составная часть |
| Г) | термодинамическая система |
11. Система, способная к обмену с окружающей средой веществом и энергией, называется
| А) | изолированной |
| Б) | идеальной |
| В) | закрытой |
| Г) | открытой |
12. Выберите выражение, соответствующее тепловому эффекту экзотермических реакций.
| А) | 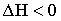 |
| Б) | 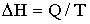 |
| В) | 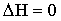 |
| Г) | 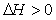 |
13. Выберите правильное соотношение между тепловыми эффектами реакции при постоянном давлении и при постоянном объёме:
| А) | D H = D UR - D nT |
| Б) | D H = D U + D nRT |
| В) | D H = D URT - D n |
14. Вставьте пропущенное выражение в формулировке закона Гесса:
“Тепловой эффект химической реакции................. от пути, по которому протекает реакция; он определяется только видом и состоянием исходных веществ и продуктов”
| А) | зависит |
| Б) | не зависит |
| В) | отличается |
| Г) | не отличается |
15. Что должно находиться в числителе выражения для константы равновесия реакции, идущей при постоянном объёме?
| А) | сумма парциальных давлений продуктов |
| Б) | произведение концентраций продуктов |
| В) | произведение концентраций исходных веществ |
| Г) | произведение парциальных давлений исходных веществ |
16. Как изменится выход продуктов экзотермической обратимой реакции при нагревании?
| А) | уменьшится |
| Б) | увеличится |
| В) | не изменится |
17. Как изменяется скорость химической реакции с повышением температуры?
| А) | не зависит |
| Б) | уменьшается |
| В) | увеличивается |
18. Вставьте пропущенное слово: «Количество теплоты, затрачиваемой на нагревание одного моля вещества на один градус, называется..... теплоёмкостью»
| А) | удельной |
| Б) | истинной |
| В) | изохорной |
| Г) | мольной |
19. Укажите обозначение и размерность внутренней энергии в системе СИ:
| А) | U, Дж/моль |
| Б) | Q, Дж |
| В) | G, кДж/моль |
| Г) | Н, Дж/моль |
20. Вставьте пропущенное слово: «Термодинамическое равновесие – это состояние системы, которое характеризуется ….. значением всех параметров в любой части системы»:
| А) | малым |
| Б) | отрицательным |
| В) | одинаковым |
| Г) | равным нулю |
21. Закончите определение: «Со статистической точки зрения энтропия является мерой..... в системе»
| А) | беспорядка |
| Б) | количества вещества |
| В) | порядка |
| Г) | массы |
22. Закончите формулировку закона возрастания энтропии: «В системе, не получающей энергии извне, самопроизвольные процессы всегда идут ……»
| А) | с уменьшением энтропии |
| Б) | до конца |
| В) | с выделением теплоты |
| Г) | с увеличением энтропии |
23. Вещество, в присутствии которого изменяется скорость химической реакции, но не входящее в состав её продуктов, называется............
| А) | сенсибилизатором |
| Б) | реагентом |
| В) | ингибитором |
| Г) | катализатором |
24. Выберите правильное математическое выражение для расчета энергии Гиббса:
А) G = HS - T
Б) G = HT + S
В) G = H + TS
Г) G = H - TS
 2020-06-10
2020-06-10 1225
1225








