1. В сосуде объемом 2 м3 находится смесь из 4 кг гелия и 2 кг водорода при температуре 27 °С. Определить давление и молярную массу смеси газов.
Дано: V = 2 м3, m 1 = 4 кг, M 1 = 4 · 10-3 кг/моль, m 2 = 2 кг,
М 2 = 2 · 10‑3 кг/моль, T = 300 К.
Найти: Р; М.
Решение. Воспользуемся уравнением Клапейрона - Менделеева, применив его к гелию и водороду:
p1V = m1RT/M1; (1)
p1V = m2RT/M2, (2)
где p 1 – парциальное давление гелия; m 1 – масса гелия; M 1 –его молярная масса; V – объем сосуда; Т – температура газа; R = 8,31 Дж/(моль·К) – молярная газовая постоянная; р 2 – парциальное давление водорода; m 2 – масса водорода; M 2 – его молярная масса. Под парциальным давлением р 1 и р 2понимается то давление, которое производил бы газ, если бы он только один находился в сосуде. По закону Дальтона давление смеси равно сумме парциальных давлений газов, входящих в состав смеси:
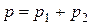 . (3)
. (3)
Из уравнения (1) и (2) выразим р 1 и р 2 и подставим в уравнение (3). Тогда
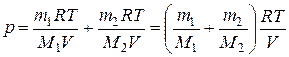 . (4)
. (4)
Молярную массу смеси газов найдем по формуле
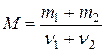 , (5)
, (5)
где v 1 и v 2 – число молей гелия и водорода соответственно. Число молей газов определим по формулам:
v 1 = m 1/ M 1; v 2 = m 2/ M 2.
Подставив это в (5), найдем
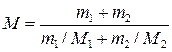 . (6)
. (6)
Подставив числовые значения в формулы (4) и (6), получим
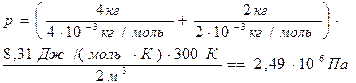
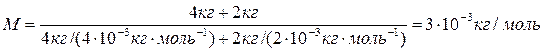 .
.
Ответ: р = 2,49×106 Па = 2,49 МПа; М = 3 · 10 – 3 кг/моль.
2. Чему равны средние кинетические энергии поступательного и вращательного движения молекул, содержащихся в 2 кг водорода при температуре 400 К?
Дано: m = 2 кг, T = 400 К, М = 2·10-3 кг/моль.
Найти: < ε пост>; < ε вр>.
Решение. Считаем водород идеальным газом. Молекула водорода – двухатомная, связь между атомами считаем жесткой. Тогда число степеней свободы молекулы водорода i = 5. В среднем на одну степень свободы приходится энергия < ε i> = kT /2, где k – постоянная Больцмана; Т - термодинамическая температура. Поступательному движению приписывается три (i = 3), а вращательному две (i = 2) степени свободы. Тогда энергия соответствующего движения одной молекулы
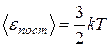 ;
; 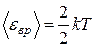 .
.
Число молекул, содержащихся в массе газа,
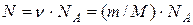 ,
,
где v – число молей; NA – постоянная Авогадро. Тогда средняя кинетическая энергия поступательного движения молекул водорода
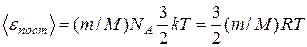 , (1)
, (1)
где R = kNA – газовая постоянная.
Средняя кинетическая энергия вращательного движения молекул водорода
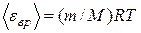 . (2)
. (2)
Подставив числовые значения в формулы (1) и (2), получим
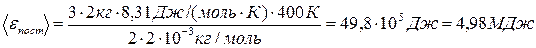 ,
,
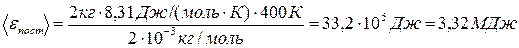
Ответ: < ε пост> = 4,98 МДж, < ε вр> = 3,32 МДж.
3. Вычислить удельные теплоемкости водорода при постоянном объеме cV и при постоянном давлении cP, считая газ идеальным.
Решение. Удельные теплоемкости идеальных газов выражаются формулами
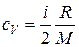 ,
, 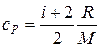 ,
,
где i – число степеней свободы молекулы газа, водород – двухатомный газ, поэтому для него i =5, М =0,002 кг/моль – молярная масса водорода.
Произведем вычисления:
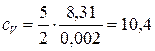 кДж/(кг·К);
кДж/(кг·К);
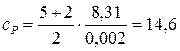 кДж/(кг·К).
кДж/(кг·К).
Ответ: сV=10,4 кДж/(кг·К), сP=14,6 кДж/(кг·К).
4. Определить коэффициенты диффузии и внутреннего тренияазота, находящегося при температуре 300 К и давлении 105Па.
Дано: r 0 = 1,25 кг/м3, М = 28·10-3 кг/моль, Т = 300 К, р = 105 Па, d = 3,l·10‑10 м.
Найти: D; h.
Решение. Коэффициент диффузии определяется по формуле
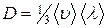 , (1)
, (1)
где 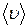 - средняя арифметическая скорость молекул, равная
- средняя арифметическая скорость молекул, равная
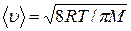 ; (2)
; (2)
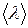 – средняя длина свободного пробега молекул, которая вычисляется по формуле
– средняя длина свободного пробега молекул, которая вычисляется по формуле
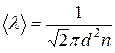 .
.
С учетом того, что давление p = nkT, получим
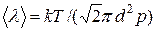 . (3)
. (3)
Подставив (2) и (3) в выражение (1), получим
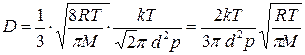 . (4)
. (4)
Коэффициент внутреннего трения
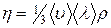 , (5)
, (5)
где r - плотность газа. Для нахождения r воспользуемся уравнением состояния идеального газа. Запишем его при нормальных условиях: Т 0 = 273 К, р = 1,01 · 10s Па, и для состояния в условии задачи:
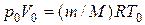 ;
; 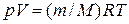 . (6)
. (6)
Учитывая, что r0 = m/Vo, r = m/V, получим
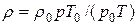 . (7)
. (7)
Коэффициент внутреннего трения газа может быть выражен через коэффициент диффузии (см. формулы (1) и (5)):
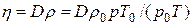 . (8)
. (8)
Подставив числовые значения в (4) и (8), получим
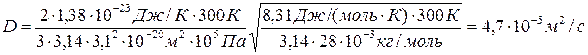
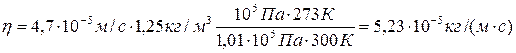 .
.
Ответ: D = 4,7 · 10-5 м2/с, h = 5,23 · 10-5 кг/(м · с).
5. Кислород массой 160 г нагревают при постоянном давлении от 320 до 340 К. Определить количество теплоты, поглощенное газом, изменение внутренней энергии и работу расширения газа.
Дано: m = 160 г = 16 · 10-2 кг, T 1 = 320 К, T 2 = 340К.
Найти: Q, D U; A.
Решение. Количество теплоты, необходимое для нагревания газа при постоянном давлении,
Q = mcp(T2-T1) = (m/M)Cp(T2-T1). (1)
Здесь ср и Cp = Mcp – удельная и молярная теплоемкости газа при постоянном давлении; М = 32 · 10-3 кг/моль – молярная масса кислорода. Для всех двухатомных газов
С p = 7/2 · R; С p = 3,5 · 8,31 Дж/(моль · К) = 29 Дж/(моль · К).
Изменение внутренней энергии газа находим по формуле
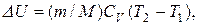 (2)
(2)
где С v – молярная теплоемкость газа при постоянном объеме.
Для двухатомных газов
C v = 5/2 R; C v = 2,5·8,31 Дж/(моль · К) = 20,8 Дж/(моль · К).
Работа расширения газа при изобарном процессе А = p·DV, гдеизменение объема газа DV = V2 –V1 можно найти из уравнения Клапейрона-Менделеева. При изобарном процессе
pV1 = (m/M)RT1; (3)
pV2 = (m/M)RT2. (4)
Почленным вычитанием выражения (4) из (3) находим
p(V2 -V1) = (m/M)R(T2 –T1),
следовательно,
A=(m/M)R(T2 –T1). (5)
Подставив числовые значения в формулы (1), (2) и (5), получим
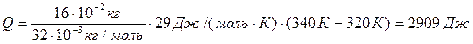 ;
;
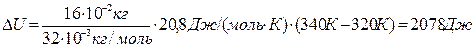 ;
;
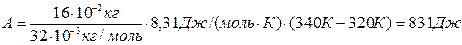
Ответ: Q = 2900 Дж; D U = 2080 Дж; А = 840 Дж.
6. Температура нагревателя тепловой машины 500 К. Температура холодильника 400 К. Определить КПД тепловой машины, работающей по циклу Карно, и полную мощность машины, если нагреватель ежесекундно передает ей 1675 Дж теплоты.
Дано: Т 1 = 500 К, Т 2 = 400 К, Q 1 = 1675Дж.
Найти: h, N.
Решение. Коэффициент полезного действия машины определяется по формуле
h = (Т1 – Т 2)/ Т 1 (1)
или
h = А / Q. (2)
Из выражений (2) и (1) находим
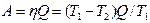 .
.
Произведем вычисления:
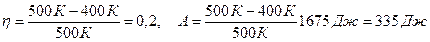 .
.
Эта работа совершается за 1 с, следовательно, полная мощность машины 335 Вт.
Ответ: h= 0,2; N = 335 Вт.
 2020-07-12
2020-07-12 122
122








